Общие свойства ферментов и факторы, влияющие на скорость биохимических процессов
Ферменты значительно повышают скорость химических реакций, которые в их отсутствие протекают очень медленно; при этом ферменты не расходуются и не претерпевают необратимых изменений.
Механизм ферментативной реакции может быть выражен следующим уравнением:
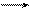
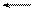 E + S ES → P + E, где
E + S ES → P + E, где
E – фермент, S – субстрат; ES – фермент-субстратный комплекс; P – продукты реакции
Ферментативная реакция состоит из двух стадий: на первой стадии происходит образование фермент-субстратного комплекса, переходному состоянию которого требуется более низкая энергия активации; на второй стадии этот комплекс распадается на продукты реакции и свободный фермент, который может взаимодействовать с новой молекулой субстрата. Таким образом, ферменты ускоряют химические реакции за счет того, что позволяют молекулам преодолевать активационный барьер на более низком энергетическом уровне.
Для проявления каталитической активности совершенно необходимо, чтобы все функциональные группы фермента располагались в пространстве строго определенным образом относительно друг друга, формируя активный центр фермента, который и обеспечивает взаимодействие с субстратом.
По химическому строению ферменты можно разделить на однокомпонентные (состоящие только из белка) и двухкомпонентные ферменты (состоящие из белковой части — апофермента и небелковой части — кофермента, участвующего в действии фермента в качестве обязательного кофактора). В результате ферментативных реакций коферменты, как правило, не подвергаются изменениям, однако при ряде последовательно протекающих реакций, кофермент может представлять собой субстрат для отдельных ферментов, хотя и регенерируется, в конечном счете, в исходной форме. Химическая природа коферментов, их функции в ферментативных реакциях и механизм действия чрезвычайно разнообразны. Так, например, в качестве коферментов могут выступать витамины и их производные.
В соответствии с химическим строением коферменты можно подразделить на следующие группы:
§ коферменты алифатического ряда (глютатион, липоевая кислота),
§ коферменты ароматического ряда (коэнзим Q — убихинон),
§ коферменты — гетероциклические соединения (производные витамина В6, В1, биотин (витамин Н), производные фолиевой кислоты),
§ коферменты — нуклеотиды и нуклеозиды (коэнзим А, НАД+, НАДФ+, ФАД, ФМН).
Ферменты как органические катализаторы белковой природы обладают рядом особенностей, которые отличают их от неорганических катализаторов.
Во-первых, это огромная сила каталитического действия. Ферменты в 108–1012 раз повышают скорость катализируемых реакций.
Во-вторых, это специфичность действия ферментов. Они катализируют строго определенные реакции. Только благодаря специфичности ферментативного катализа возможна строгая упорядоченность и взаимосвязь отдельных ферментативных реакций, лежащих в основе биологического обмена веществ в живой клетке.
По степени специфичности отдельные ферменты достаточно сильно различаются между собой. Различают следующие основные типы специфичности:
– абсолютная специфичность — фермент катализирует превращение только одного субстрата;
– групповая специфичность — фермент действует на группу родственных субстратов, обладающих определенным структурным сходством;
– специфичность по отношению к определенным типам реакций — такие ферменты проявляют наименьшую специфичность, они действуют независимо от того, какие группы присутствуют вблизи той связи, на которую направлено действие фермента;
– стереохимическая специфичность — фермент катализирует превращение только одной стереохимической формы субстрата.
Третьей особенностью ферментов является их лабильность. Это означает, что ферменты подвержены влиянию различных факторов и могут изменять свою активность под влиянием рН среды, температуры, при действии активаторов и ингибиторов и др. Лабильность или изменчивость ферментов обусловлена их белковой природой, сложной пространственной конформацией белковой молекулы.
Таким образом, ферментативный катализ существенно отличается от неферментативного. Скорость протекания биохимических процессов будет зависеть от ряда факторов: от химической природы реагирующих веществ, концентрации субстрата и фермента, температуры и рН среды, наличия различных эффекторов (активаторов и ингибиторов).
Вопросы, связанные с кинетикой ферментативных реакций, детально изложены в специальных разделах биохимии и энзимологии. Поэтому особое внимание будет уделено тем положениям, которые необходимы для грамотного подхода к работе с ферментами. Наличие фермента в растворе или экстракте можно определить исходя из скорости катализируемой им реакции, о которой судят либо по накоплению продуктов реакции, либо по убыли субстрата.
Для того чтобы правильно определить потенциальные возможности данного фермента как катализатора, нужно учитывать скорость ферментативной реакции в тот момент времени, когда наблюдается прямая пропорциональная зависимость между продуктами реакции и временем, то есть реакция идет по нулевому порядку. Такая скорость называется начальной скоростью ферментативной реакции и обозначается V0. На практике V0 определяют графическим методом: экспериментально строят кривую хода ферментативной реакции во времени. Начальная скорость определяется как тангенс угла наклона касательной, проведенной из начала координат к кривой хода ферментативной реакции.
Важнейшим фактором, определяющим скорость ферментативной реакции, является концентрация субстрата. Максимальная скорость реакции достигается при такой концентрации субстрата, когда все активные центры фермента насыщены субстратом и дальнейшее увеличение концентрации субстрата не приводит к увеличению скорости реакции.
При насыщающей концентрации субстрата, обеспечивающей Vmax , начальная скорость ферментативной реакции будет, в первую очередь, зависеть от концентрации фермента. Эта зависимость прямо пропорциональная, что свидетельствует о том, что начальная скорость является мерой количества фермента.
Влияние температуры на активность фермента, которое может быть легко изучено экспериментально, имеет очень сложный характер, так как обусловлено целым рядом факторов, а именно:
§ влиянием температуры на скорость расщепления комплекса ES на свободный фермент и продукт реакции;
§ влияние температуры на сродство фермента к субстрату;
§ влияние на теплоту ионизации, а, следовательно, на процессы ионизации всех компонентов реакции: самого фермента, субстрата, промежуточных и конечных продуктов реакции;
§ влияние на образование таких соединений как «фермент – активатор» или «фермент – ингибитор»,
§ влияние на процесс денатурации ферментного белка.
 Оптимальная температура, при которой наблюдается максимальная активность, для большинства ферментов находится в пределах 370-500С, но некоторые ферменты имеют температурный оптимум за пределами этой зоны. Резкое снижение скорости ферментативной реакции при температурах, превышающих оптимальную, связано, в первую очередь, с денатурацией ферментного белка. Поэтому очень важным показателем, характеризующим отношение фермента к температуре, является его термостабильность.
Оптимальная температура, при которой наблюдается максимальная активность, для большинства ферментов находится в пределах 370-500С, но некоторые ферменты имеют температурный оптимум за пределами этой зоны. Резкое снижение скорости ферментативной реакции при температурах, превышающих оптимальную, связано, в первую очередь, с денатурацией ферментного белка. Поэтому очень важным показателем, характеризующим отношение фермента к температуре, является его термостабильность.
Термостабильность фермента складывается их двух критериев: величины температуры и времени ее воздействия на фермент. Кроме того, на термостабильность различных ферментов могут оказывать влияние и такие факторы, как рН среды, ее солевой состав, защитное действие субстрата.
Для каждого фермента характерна определенная узкая область значений рН, при которой он проявляет максимальную активность.
Зависимость активности фермента от рН отражает способность важных для данного фермента протон-донорных или протон-акцепторных групп в активном центре фермента переходить в состояние с требуемой степенью ионизации при определенных значениях рН. Ход кривых будет зависеть и от других факторов, в частности, изменение рН среды изменяет состояние ионизации субстрата (если это заряженное вещество), комплексов ES и EP, в некоторых, например, окислительно-восстановительных реакциях, ионы Н+ сами могут принимать участие в реакции; помимо этого скорость денатурации ферментативного белка зависит от рН.
При экспериментальном изучении активности фермента от рН следует помнить, что рН-оптимум зависит: от состава среды (от природы используемого буфера); оптимум рН прямой и обратной реакции могут быть совершенно различными; при действии одного и того же фермента на различные субстраты рН-оптимумы также могут быть различными. Кроме понятия оптимума рН, очень важным является понятие рН-стабильности. Это тот диапазон рН, при котором фермент или ферментый препарат сохраняет свою активность в течение определенного периода времени. рН-стабильность также зависит от ряда факторов, среди которых, кроме уже названных, форма ферментного препарата, степень его очистки и др.
Все выше сказанное позволяет утверждать, что, варьируя температурный режим и изменяя рН, можно в какой-то мере регулировать каталитическую активность фермента.
Влияние активаторов и ингибиторов. Активаторами называют вещества, которые повышают активность ферментов. Хорошим примером таких соединений являются аминокислота цистеин и восстановленный глютатион, содержащие свободную SH-группу. Они активируют тиоловые ферменты. Кроме того, некоторые ферменты активируются металлами, которые либо участвуют в построении активного центра, либо стабилизируют пространственную конформацию ферментного белка и, тем самым, обеспечивают проявление каталитических функций.
Ингибиторами называют вещества, специфически снижающие активность ферментов. Снижение или полная потеря активности ферментов могут быть вызваны разного рода денатурирующими воздействиями, в этом случае правильнее употреблять термин «инактивация» фермента.
Существует ингибирование двух основных типов: необратимое и обратимое. Обратимое ингибирование, в свою очередь, бывает конкурентным и неконкурентным.
Конкурентный ингибитор конкурирует с субстратом на основе структурного сходства, связываясь с активным центром фермента с образованием неактивного комплекса фермент-ингибитор. Отличительная особенность конкурентного ингибирования состоит в том, что его можно устранить или ослабить, повысив концентрацию субстрата.
Одними из самых распространенных неконкурентных ингибиторов являются аллостерические ингибиторы. Присоединяясь не к активному, а к другому, так называемому аллостерическому центру молекулы фермента, ингибитор вызывает конформационные изменения в структуре активного центра, вследствие чего, становится невозможным образование комплекса фермент – субстрат.
Изучение взаимодействия ферментов с ингибиторами и активаторами ферментов позволяет получать ценные сведения о субстратной специфичности ферментов, природе функциональных групп активного центра, механизмах каталитической активности. Так как в качестве ингибиторов могут выступать конечные продукты реакции, различные промежуточные продукты метаболизма, нет сомнения в той огромной роли, которую выполняют ингибиторы в регуляции ферментативной активности. Это подтверждает и факт широкого распространения ингибиторов белковой природы. Кроме того, по принципу специфического ингибирования действуют многие лекарственные препараты, антибиотики, токсичные вещества, антиалиментарные факторы питания.
Специфические ингибиторы, встречающиеся в пищевом сырье и пищевых продуктах, присутствуют в качестве составляющих, как в традиционных рецептурах, так и в сложных композиционных составах новых, модифицированных продуктов питания. Поэтому нельзя не учитывать их влияние на активность отдельных ферментов и на биохимические процессы в целом, протекающие при хранении и переработке пищевого сырья.
Все это лишний раз говорит о множестве сложных проблем, которые встречаются в экспериментальной работе с ферментами и использовании ферментных препаратов на практике.
Дата добавления: 2020-10-01; просмотров: 733;











