Физикохимия дисперсных систем. Растворы ВМС
Актуальность темы.Окружающий мир – растительные и животные организмы, объекты неживой природы (почва, горные породы, спрессованные порошки и др.), продукты питания и т.д. – это дисперсионные системы разной степени организации. Так, например, среди биологических объектов к дисперсным системам с разными размерами частичек можно отнеси: эритроциты / 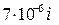 / крови человека, кишечную палочку /
/ крови человека, кишечную палочку / 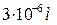 /, вирус гриппа /
/, вирус гриппа / 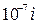 /. Как видно, что размеры частичек в этих системах отличаются на несколько порядков.
/. Как видно, что размеры частичек в этих системах отличаются на несколько порядков.
В крови, лимфе, спинномозговой жидкости и смешанной слюне ряд веществ, например, белки, липиды, фосфаты идр. находятся в коллоидном состоянии. В соответствии с составом и свойствами слюны можно предположить, что основной структурной коллоидной единицей (мицеллой) являются мицеллы фосфата кальция. Это связано, во-первых, с тем, что именно ионы 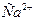 и
и 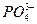 находятся в слюне в неравновесных концентрациях, причем содержание
находятся в слюне в неравновесных концентрациях, причем содержание 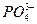 – ионов в 3 — 4 раза выше, чем ионов
– ионов в 3 — 4 раза выше, чем ионов 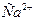 . Во-вторых, эти ионы способны к активному взаимодействию с образованием нерастворимого ядра мицеллы. Вероятный состав мицелл можно представить в следующем виде:
. Во-вторых, эти ионы способны к активному взаимодействию с образованием нерастворимого ядра мицеллы. Вероятный состав мицелл можно представить в следующем виде: 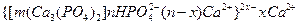 .
.
Не исключено,что структурированное состояние слюны позволяет совершенно с иных позиций рассматривать проблему взаимодействия слюны с зубами и тканями полости рта, а также устойчивости слюны, влияние на нее различных физиологических и патологических факторов. Их воздействие на слюну необходимо учитывать, прежде всего, с точки зрения влияния на состав мицелл и их устойчивость. Например, в щелочной среде состав мицелл фосфата кальция можно представить так: 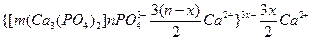 . Такая мицелла неустойчива, так как ионы
. Такая мицелла неустойчива, так как ионы 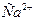 и
и 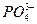 быстро взаимодействуют между собой, образуя выпадающий в осадок фосфат кальция. Такое явление наблюдается в полости рта при повышении рН слюны, когда резко активизируется процесс камнеобразования.
быстро взаимодействуют между собой, образуя выпадающий в осадок фосфат кальция. Такое явление наблюдается в полости рта при повышении рН слюны, когда резко активизируется процесс камнеобразования.
Что касается в кислой среде, то состав мицелл фосфата кальция выглядит так: 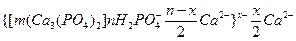 . Как видно, здесь заряд гранулы снизился вдвое, уменьшится диффузный слой, следовательно, и устойчивость мицеллы. Кроме того, ионы
. Как видно, здесь заряд гранулы снизился вдвое, уменьшится диффузный слой, следовательно, и устойчивость мицеллы. Кроме того, ионы 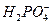 /дигидрофосфат/ такой мицеллы не участвуют в процессе реминерализации. Для поддержания мицеллы в устойчивом состоянии часть эмали зубов под влиянием ионов кислоты растворится, она будет нейтрализована, постепенно состав мицеллы восстановится, и вновь может начаться реминерализация растворившейся эмали.
/дигидрофосфат/ такой мицеллы не участвуют в процессе реминерализации. Для поддержания мицеллы в устойчивом состоянии часть эмали зубов под влиянием ионов кислоты растворится, она будет нейтрализована, постепенно состав мицеллы восстановится, и вновь может начаться реминерализация растворившейся эмали.
Значение коллоидной защиты для фармации и стоматологи чрезвычайно велико. Принцип коллоидной защиты используют при получении колларгола, золей серебра, золото и т.д. Частицы колларгола так хорошо защищены, что не коагулируют даже при высушивании. Белки крови защищают капельки жира, холестерин и др. гидрофобные вещества от коагуляции. Ослабление защитных функций белков крови приводит к отложению холестерина на стенках сосудов, образованию камней в почках и печени. Свертывание крови, слипание эритроцитов в так называемые «монетные столбики» представляют собой процессы, аналогичные коагуляции. В основе процесса растворения тромбов лежит явление пептизации. При потере слюной агрегативной устойчивости происходит осаждение муцина слюны на поверхности зубов, что тормозит реминерализацию эмали. Вполне вероятно, что понимание сущности всего этого процесса может открыть совершенно новые подходы к диагностике, профилактике и лечению стоматологических и др. заболеваний.
В настоящее время особый интерес представляет разработка моделей клеток, живых мембран, нервных клеток, действующих по законам коллоидной химии. Примером сочетания диализа и ультрафильтрации является аппарат «искусственная почка». Кроме того, электрокинетические явление, такое как электрофорез широко применяется в стоматологической практике для транспорта лекарственных препаратов через кожу, т.к. введение лекарственных препаратов через кожу создает депо, которое продолжительное время влияет на организм больного человека.
Современная жизнь практически невозможно без материалов на основе ВМС. Велико их значение в медицине, где они применяются для создания искусственных сосудов, разнообразных протезов, при изготовлении специальных, в том числе хирургических клеев. Антимикробные волокна, изготовленные на основе природных полимеров (целлюлозы) или синтетические ВМС (поливиниловый спирт) имеют свойства задерживать рост различных микроорганизмов и применяются в хирургической практике как шелковый материал. В технологии лекарств синтетические полимеры применяют как вспомогательные вещества при изготовлении различных лекарственных форм. К ним также принадлежат ВМС, которые способны пролонгировать действие лекарственных препаратов в организме, а также растворы полимеров, которые используют как крове- и плазмозаменители.
В целом, знания физико-химических свойств коллоидных систем необходимо для изучения ряда общемедицинских и клинических дисциплин, таких как терапия, клиническая лабораторная диагностика, кардиология, биохимия, фармакология, а также в практической деятельности врача – стоматолога.
Цели занятия: 1.Приобретение системные знания о коллоидно-дисперсных системах в зависимости от признаков классификации, о методах получения, очистки и об устойчивости дисперсных систем и умение применять эти знания к конкретным системам, встречающиеся в биологических объектах. 2. Экспериментальное получение коллоидных растворов и изучение их свойства и некоторые свойства ВМС.
Вопросы для подготовки к занятию.
1. Дисперсные системы (определение, классификация).
1.1.Лиофильные и лиофобные коллоидные системы (золи или лиозоли).
1.2.Методы получения коллоидных систем (конденсационные и диспергационные).
1.3.Методы очистки коллоидных систем. Вивидиализ. Гемодиализ и аппарат «Искусственная почка».
1.4.Свойства дисперсных систем: молекулярно-кинетические (броуновское движение, диффузия, осмотическое давление, седиментация); оптические (опалесценция, уравнение Релея, конус Тиндаля).
2. Понятие лиофобных золей.
2.1.Мицеллярная теория строения лиофобных золей (мицелла, ядро, ионогенная часть, гранула). Слюна как дисперсная система.
2.2.Агрегативная и кинетическая устойчивость коллоидных растворов, факторы устойчивости. Электрокинетический потенциал.
2.3.Электрокинетические явления в золях. Электрофорез. Электроосмос.
3. Коагуляция. Факторы, вызывающие её.
3.1.Порог коагуляции. Коагулирующая способность электролитов. Правило Щульце-Гарди.
3.2.Коллоидная защита, стабилизация коллоидных растворов. Биомедицинское значение коллоидной защиты.
4. Определение и классификация высокомолекулярных соединений (ВМС) – по происхождении, конфигурации молекулы, растворимости в воде, структуре.
4.1.Основные классы биополимеров: белки, нуклеиновые кислоты, полисахариды.
4.2.Изоэлектрическое состояние белков и методы определения изоэлектрической точки.
4.3.Особые свойства растворов ВМС (набухание, застудневание, вязкость, осмотическое давление).
4.4.Значение растворов ВМС для жизнедеятельности организма и применение биополимеров в медицине и фармации.
Базисные знания. Студент должен знать из курса химии: «Способы выражения концентрации вещества в растворе. Виды химической связи. Коллигативные свойства растворов (диффузия, осмос и др.). Электролиты сильные и слабые. Реакция среды и рН. Гомо- и гетерогенные системы. Адсорбция и её виды», из курса биологии и гистологии: «Строение клетки и клеточных мембран» и из курса физики: «Оптические явления –дифракция, интерференция, светорассеивание».
Дата добавления: 2020-07-18; просмотров: 555;











