УЛАВЛИВАНИЕ ЭНЕРГИИ СВЕТА БИОМОЛЕКУЛАМИ
Можно смело утверждать, что Жизнь на нашей планете обязана солнечному свету. Энергия света поглощается фотосинтезирующими организмами и запасается в виде химических связей органических соединений, а остальные обитатели Земли (возможно, лишь за исключением способных к хемосинтезу бактерий) используют энергию этих связей для того, чтобы осуществить в клетках окислительное или субстратное фосфорилирование.
Видимый свет представляет собой форму электромагнитного излучения с длиной волны 400—700 нм, и его происхождение обусловлено сложными процессами, происходящими на Солнце. Одним из результатов этих процессов является испускание энергии в виде квантов видимого света (фотонов), которые достигают земной поверхности. Энергия фотонов обратно пропорциональна их длине волны, и наибольшей энергией характеризуются фотоны с наименьшей длиной волны, соответствующей фиолетовому краю видимого спектра.
Способность вещества поглощать свет зависит от его атомной структуры. Когда фотон сталкивается с атомом или молекулой, способными поглощать свет данной длины волны, энергия фотона поглощается одним из электронов и атом или молекула переходят в более богатое энергией возбужденное состояние. Возбуждение длится 10-9 — 10-8 с, после чего молекула возвращается в первоначальное состояние, которое называется основным и характеризуется меньшей энергией, чем возбужденное. При возврате в основное состояние возбужденная молекула может терять свою энергию несколькими способами: 1) энергия может рассеиваться в виде тепла; 2) часть поглощенной энергии может немедленно испускаться в виде света (флуоресценция) или после некоторой задержки (фосфоресценция). Испускаемый при флуоресценции и фосфоресценции свет обычно характеризуется большей длиной волны и меньшей энергией, чем свет, вызвавший возбуждение молекулы. Кроме этого (3), поглощение света может вызывать фотохимические реакции, в которые способны вступать возбужденные молекулы.
Фотохимические реакции представляют собой диссоциацию на ионы или радикалы либо присоединение протонов, что может сопровождаться разрывом связей, реакции фотоприсоединения и фотоотщепления, а также изомеризации. Возбужденные молекулы способны превращаться в сильные окислители и восстановители и индуцировать соответствующие процессы по отношению к другим молекулам. Все перечисленные реакции с участием возбужденных светом молекул становятся возможными, поскольку с повышением энергии молекулы приобретают химические свойства, нехарактерные для их невозбужденных форм.
Фотохимические реакции приобретают особую роль, когда затрагивают жизненно важные для клетки структуры. Первостепенное значение в этом отношении играют нуклеиновые кислоты, азотистые основания которых, как известно, испытывают на себе фотодинамическое действие коротковолнового света. В результате различного рода фотохимических превращений (в первую очередь, образования пиримидиновых димеров) в составе ДНК появляется большое количество изменений, которые, не будучи репарированными, закрепляются в виде мутаций (глава 2).
С другой стороны, фотохимические реакции чрезвычайно важны для таких явлений, как фотосинтез и фоторецепция. Среди биологических молекул есть специализированные, способные в ответ на поглощение света обусловливать определенные процессы в клетках. Такими молекулами служат, в первую очередь, фотосинтетические пигменты, участвующие в запасании световой энергии в ходе фотосинтеза. В возбужденном состоянии молекулы хлорофилла способны инициировать фотоокисление молекул воды, что сопровождается транспортом возбужденных электронов по компонентам фотосистем. Другой класс светочувствительных биомолекул представлен зрительными фоторецепторами, которые в ответ на поглощение света генерируют нервный импульс. Фотохимическая реакция, запускающая данный процесс, состоит в изомеризации молекулы зрительного пигмента.
Фотосинтез
Фотосинтез представляет собой высокоэффективный процесс запасания энергии видимого света и трансформирования ее в энергию химических связей биологических молекул. Осуществляется данный процесс в клетках растений, водорослей и фототрофных бактерий, причем у большинства перечисленных организмов фотосинтез сопровождается использованием в качестве донора электронов воды и выделением молекулярного кислорода (уравнение 13.1). И только у аноксигенных бактерий, относящихся к классу Anoxyphotobacteria , вместо воды роль доноров электронов могут выполнять некоторые иные восстановленные соединения, например сероводород. При этом не происходит образования О2 (уравнение 13.2).
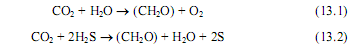
Данное наблюдение принадлежит Корнелису ван Нилю, который в 1931—1933 гг., будучи еще студентом-дипломником, исследовал особенности фотосинтеза у разных бактерий и сделал смелое предположение, перевернувшее взгляды исследователей на закономерности фотосинтеза. Исходя из выведенного им уравнения фотосинтеза для пурпурных серных бактерий (13.2), К. ван Ниль предположил, что не углекислота, а вода разлагается при фотосинтезе у растений, образуя молекулярный кислород, и предложил общее уравнение фотосинтеза (13.3):
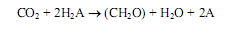
В последнем уравнении H2A представляет собой донор электронов, которым у оксигенных организмов служит вода, а у аноксигенных бактерий—другие вещества (сероводород, молекулярный водород, изопропанол и др.). При этом выделяется дегидрированный донор электронов (А) и происходит восстановление углекислоты до органического соединения (СН2О). Эти превращения и составляют суть процесса фотосинтеза.
Интересно отметить, что вода является очень плохим донором электронов и ни один из окислителей, которыми располагают живые организмы, не является достаточно мощным, чтобы отщепить от молекулы Н2О атомы водорода. Это становится возможным лишь в результате фотохимических превращений особых молекул хлорофиллов, которые становятся сильными окислительными агентами и приобретают способность окислять воду.
Процесс фотосинтеза требует обязательного участия мембран. У прокариот эту роль выполняют впячивания плазматической мембраны, а у эукариот — мембраны тилакоидов, расположенные в хлоропластах. Тилакоиды находятся в строме хлоропластов, образуя стопки (граны). Внутреннее содержимое тилакоидов называют люменом.
В мембранах тилакоидов располагаются компоненты транспорта электронов, сгруппированные в 2 фотосистемы, и АТР-синтаза. Фотосистемы используются для переноса электронов и сопряженного с ним перевода протонов в люмен, в результате чего на тилакоидной мембране создается протонный градиент. Энергия протонного градиента запускает синтез АТР, подобно тому, как это имеет место при окислительном фосфорилировании. Однако, в отличие от дыхательной цепи, в фотосистемах электроны движутся от плохого донора (молекулы воды) к плохому акцептору (NADP+), т. е. в противоположном по сравнению с дыханием направлении. Соответственно и энергия при таком направленном «вверх» потоке электронов должна затрачиваться. Действительно, для восстановления NADP+ электроны должны дважды возбудиться светом.
Характеристика компонентов фотосистем. Компоненты фотосистем представляют собой белковые комплексы, содержащие фоточувствительные молекулы (пигменты) и переносчики восстановительных эквивалентов.
Пигменты представлены в основном хлорофиллами, каротиноидами и фикобилинами. Основную роль в процессе фотосинтеза играет зеленый, содержащий ионы магния тетрапиррольный пигмент — хлоро-филл a (рис. 13.1). Этот хромофор представляет собой магнийпорфирин и похож по структуре на гем (железопорфирин). Однако у хлорофилла a имеются следующие основные отличия: с одним из пиррольных колец слито пятое, циклопентановое кольцо; одно из пиррольных колец частично восстановлено; одна из кислотных боковых цепей представляет собой эфир фитола—двадцатиуглеродного высокогидрофобного спирта. Остаток фитола придает молекуле хлорофилла амфифильные свойства и служит «якорем», с помощью которого хромофор может удерживаться в липидном бислое тилакоидной мембраны. При этом гидрофильная голова (магнийпорфирин) находится на поверхности мембраны, обращенной к водной фазе стромы, и расположена параллельно плоскости мембраны. Таким образом, достигается ориентация хлорофилла в хлоропластах, способствующая наиболее эффективному улавливанию световой энергии.
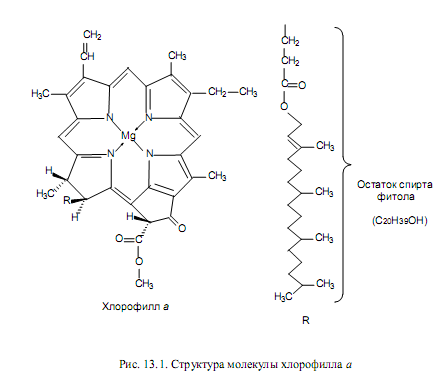
Другие хлорофиллы зеленых растений (b, c, феофитин), а также хлорофиллы некоторых водорослей и бактерий (хлоробиум-хлорофилл, бактериохлорофиллы) отличаются от хлорофилла a структурой заместителей у пиррольных колец, отсутствием иона магния (феофитин), спектрами поглощения. Существование в клетке хлорофиллов с разными спектрами поглощения позволяет увеличить диапазон улавливаемого излучения.
Каротиноиды и фикобилины служат вспомогательными пигментами. Они еще больше увеличивают спектр поглощаемой организмом энергии, а кроме того, защищают хлорофиллы от избытка света и от окисления кислородом, который выделяется при фотосинтезе. Каротиноиды — это желтые, оранжевые, красные или коричневые пигменты, сильно поглощающие в фиолетовой области спектра. В хлоропластах присутствуют две группы каротиноидов—каротины(углеводороды, бульшую часть которых составляют тетратерпены, подробно рассматриваются в главе 17) и ксантофиллы (по химическому строению сходны с каротинами, но содержат кислород). Фикобилины характерны для цианобактерий и хлоропластов красных водорослей.
Для более полного улавливания световой энергии пигменты в фотосистемах собраны с помощью белков в антенные комплексы. В каждом антенном комплексе насчитывается по несколько сотен молекул пигментов, и их основная функция состоит в передаче поглощенной энергии хлорофиллу а. Таким образом, можно сравнить антенный комплекс с воронкой, «загоняющей» энергию к хлорофиллу реакционного центра фотосистемы. Энергия возбуждения (экситон) передается от молекулы к молекуле посредством электрического поля возбужденного электрона (очевидно, возбужденный электрон в молекуле, поглотившей квант света, передает свою энергию близлежащей молекуле таким образом, что в той тоже возбуждается электрон).
Транспортирующие электроны компоненты фотосистем представлены комплексом цитохрома b/f (агрегат интегральных мембранных белков, содержащий два цитохрома: b563 и f), феофитином, мембраносвязанными пластохинонами (QA и QB), а также мобильными переносчиками, функции которых выполняют пластохинон QP, пластоцианин и ферредоксин. Пластохинон по структуре и функциям очень напоминает убихинон (рис. 12.1). Пластоцианин представляет собой белок с одним атомом меди, координационно связанным с боковыми цепями аминокислот: при переносе электрона Cu находится попеременно в степени окисленности +1 и +2. Ферредоксин является железосерным белком типа 4Fe, 4S2-, переносящим электроны. Цепь переносчиков замыкает фермент, транспортирующий электроны на NADP+.
Установлено, что фотосинтез требует участия двух фотосистем: II и I. Фотосистема II содержит в реакционном центре хлорофилл a, имеющий оптимум поглощения при 680 нм (Р680), а в реакционном центре фотосистемы I (Р700) содержится хлорофилл a с оптимумом поглощения 700 нм.
Световые реакции фотосинтеза. Процесс фотосинтеза условно можно разделить на 2 этапа: световые и темновые реакции. Световые реакции требуют участия видимого света и осуществляются в тилакоидных мембранах. Их итогом является восстановление NADP+ и синтез АТР. Темновые реакции могут осуществляться и в условиях отсутствия видимого света, в строме, и под ними обычно подразумевают восстановление СО2 при участии АТР и NADPH.
У растений фотосинтетический перенос электронов начинается с фотосистемы II. Энергия поглощенного света поступает от антенных комплексов к хлорофиллу a реакционного центра Р680 и переводит один из его электронов в возбужденное состояние. Возбужденный электрон сразу передается на расположенный рядом феофитин, а в молекуле хлорофилла появляется положительно заряженная «дырка» с очень высоким сродством к электрону, т.е. возникает положительно заряженный радикал Р680. «Дырка» очень быстро заполняется электроном, извлеченным из воды водорасщепляющим ферментом 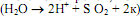 при участии ионов марганца. Возбужденный электрон мигрирует по цепи переносчиков (рис. 13.2) и достигает второй «дырки» в Р700 фотосистемы I, которая, в свою очередь, образовалась при переносе «горячего» электрона на электронный акцептор (по-видимому, пластохинон). Здесь электрон возбуждается вторично и далее по переносчикам фотосистемы I передается на NADP+ (рис. 13.2). Такое движение электронов по цепи переносчиков называется нециклическим потоком, или Z-схемой. Важной отличительной особенностью этого процесса является то, что электрон дважды возбуждается в реакционных центрах двух фотосистем, и поэтому его энергии хватает для восстановления NADP+.
при участии ионов марганца. Возбужденный электрон мигрирует по цепи переносчиков (рис. 13.2) и достигает второй «дырки» в Р700 фотосистемы I, которая, в свою очередь, образовалась при переносе «горячего» электрона на электронный акцептор (по-видимому, пластохинон). Здесь электрон возбуждается вторично и далее по переносчикам фотосистемы I передается на NADP+ (рис. 13.2). Такое движение электронов по цепи переносчиков называется нециклическим потоком, или Z-схемой. Важной отличительной особенностью этого процесса является то, что электрон дважды возбуждается в реакционных центрах двух фотосистем, и поэтому его энергии хватает для восстановления NADP+.
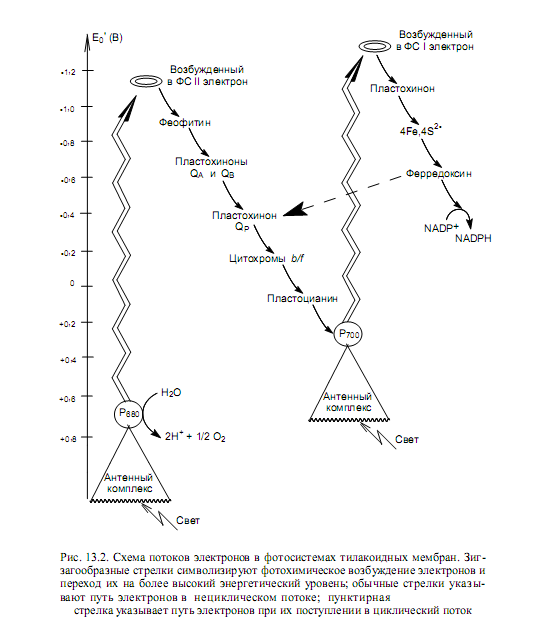
Реакцию образования NADPH катализирует ферредоксин-NADP+-редуктаза, содержащая FAD в качестве простетической группы. Следует отметить, что для восстановления никотинамидных кофакторов требуются гидрид-ионы: 2 электрона от двух молекул восстановленного ферредоксина конвергируют, а протон поступает из стромы.
Кроме образования NADPH, нециклический поток электронов обусловливает перенос протонов в люмен и создание на тилакоидной мембране электрохимического градиента. Это происходит на этапе переноса водорода от восстановленного пластохинона QP на комплекс цитохромов b/f, которые, как известно (глава 12), являются переносчиками электронов. Когда протоны, согласно закономерностям облегченной диффузии, выходят из люмена в строму, они используют каналы АТР-синтазы, и происходит синтез АТР. Этот механизм запасания энергии носит название фотофосфорилирование, и его принцип сходен с механизмом окислительного фосфорилирования.
Кроме описанного выше нециклического потока, в тилакоидных мембранах могут осуществляться циклические потоки электронов. В них электрон возбуждается только единожды, в реакционном центре фотосистемы I, и не происходит образования NADPH. Поток становится циклическим, когда электроны от ферредоксина передаются не на NADP+ , а обратно, к пластохинону QP (рис. 13.2, 13.3, пунктирные стрелки). Такое движение электронов обеспечивает клетку только АТР, но не NADPH. Циклический поток электронов преобладает при низких концентрациях NADP+ , что обусловлено накоплением в клетке NADPH.
На рис. 13.3 показано расположение компонентов фотосистем, их субстратов, а также продуктов. Можно видеть, что основные продукты световых реакций фотосинтеза — NADPH и ATP — накапливаются в строме, т. е. там, где они должны расходоваться в темновых реакциях.
Темновые реакции фотосинтеза. К темновым реакциям фотосинтеза относят фиксацию, т. е. восстановление и включение в состав органических соединений, СО2. У большинства фотосинтезирующих организмов этот процесс осуществляется в цикле Кальвина (цикл носит имя Мелвина Кальвина, получившего за его открытие Нобелевскую премию).
Цикл Кальвина условно можно разделить на три этапа: 1) карбоксилирование рибулозодифосфата; 2) восстановление 3-фосфоглицерата до альдегида; 4) регенерация рибулозодифосфата — акцептора СО2.
Углекислота, восстанавливаемая в цикле Кальвина, поступает в строму хлоропластов зеленых растений через устьица в листьях и зеленых стеблях, а в клетки водорослей и цианобактерий — в растворенном виде. Ключевой реакцией восстановления СО2 является карбоксилирование рибулозодифосфата.
Данную реакцию катализирует необычный фермент—рибулозодифосфаткарбоксилаза/оксигеназа, обладающая двумя активностями: карбоксилазной и оксигеназной (рис. 13.4).
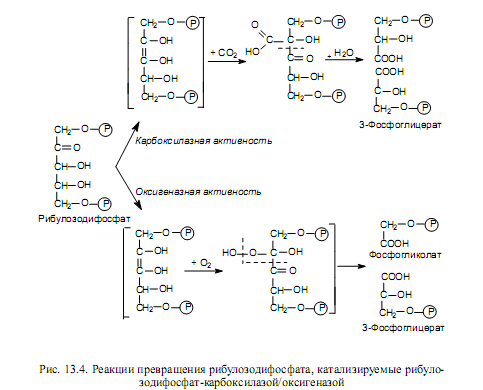
Оксигеназная активность реализуется в отсутствии СО2 и в присутствии О2, а продукты этой реакции участвуют в фотодыхании. Рибулозодифосфаткарбоксилаза/оксигеназа очень медленно работает: скорость ее катализа в сотни раз меньше, чем для большинства других ферментов. Поэтому в хлоропластах этот фермент может составлять до половины всего белка. Считается, что это самый распространенный на Земле белок, преобладающий в количественном отношении над другими белками. На уровне данного фермента осуществляется регуляция скорости цикла Кальвина.
Восстановление продуктов карбоксилазной реакции (2 молекул 3фосфоглицерата) происходит с участием фосфоглицераткиназы и глицеральдегид-3-фосфатдегидрогеназы. Обратные реакции, катализируемые этими ферментами, имеют место в гликолизе (рис. 9.3). В этом процессе затрачивается энергия АТР и восстановительные эквивалентны, поставляемые NADPH.
Регенерация рибулозодифосфата осуществляется в результате межмолекулярных перестроек с участием трансальдолаз и транскетолаз (принимают также участие в пентозофосфатных путях, описаны в главе 9). В превращения вступают 3 соединения: глицеральдегид-3-фосфат, образующийся из него в ходе изомеризации дигидроксиацетонфосфат, а также фруктозо-1,6-дифосфат, который образуется в реакции альдольной конденсации из двух триозофосфатов (см. Гликолиз, глава 9).
В результате описанных превращений из 6 молекул СО2 в ходе 6 оборотов цикла Кальвина синтезируется 1 молекула гексозы. При этом затрачивается 18 молекул АТР и 12 молекул NADPH (рис. 13.5). Таким образом, фиксация углекислоты обходится клетке очень дорого: на включение лишь одной молекулы СО2 в органическое соединение расходуется 3 молекулы АТР и 2 молекулы NADPH.
Цикл Кальвина изображают замкнутым, однако, как и в ЦТК, многие его промежуточные продукты используются в качестве предшественников для биосинтеза клеточных соединений. Так, 3-фосфоглицерат мо- жет превращаться в пируват (реакции гликолиза); эритрозо-4-фосфат —
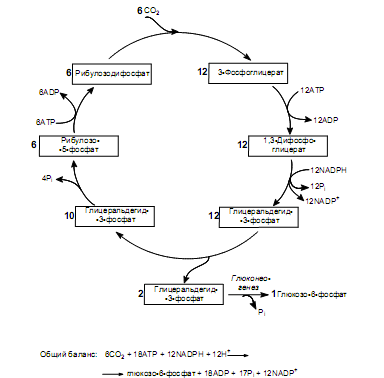
в ароматические аминокислоты; рибозо-5-фосфат — в нуклеотиды; гексозофосфаты — в полисахариды (последние три промежуточных соединения формируются на стадии межмолекулярных перестроек). Так же, как и в других циклах, существуют анаплеротические реакции, не позволяющие циклу прерываться.
Скорость цикла Кальвина строго регулируется, поскольку на фиксацию СО2 не должно расходоваться чересчур много клеточной энергии. Основной принцип регуляции цикла состоит в том, чтобы «подогнать» скорость фиксации СО2 к скорости световых реакций фотосинтеза, где образуются необходимые для фиксации АТР и NADPH. Поэтому, не смотря на то что цикл Кальвина не требует непосредственного участия видимого света, наиболее интенсивно он все же протекает в условиях освещения. Основной стадией, лимитирующей скорость фиксации углекислоты, является карбоксилирование рибулозодифосфата. Активность карбоксилазы значительно увеличивается при освещении, чему способствуют следующие причины:
1) карбоксилаза аллостерически активируется фруктозо-6-фосфатом и ингибируется фруктозо-1,6-дифосфатом. В свою очередь, содержание этих продуктов контролирует фермент фруктозо-1,6-дифосфатаза, которая активируется светом и катализирует расщепление фруктозодифосфата;
2) еще одним аллостерическим активатором карбоксилазы является NADPH, а его количество возрастает на свету при интенсивном нециклическом потоке электронов;
3) скорость рассматриваемой ферментативной реакции возрастает при повышении рН от 7 до 9. Фермент работает в строме, а ее защелачивание является следствием закисления люмена при создании протонного градиента на тилакоидной мембране;
4) карбоксилаза активируется ионами марганца, которые высвобождаются в строму при переносе протонов в люмен в процессе транспорта электронов.
Кроме этого, свет активирует еще один фермент цикла Кальвина — глицеральдегид-3-фосфат-дегидрогеназу, который, очевидно, меняет свою специфичность (от NADH к NADPH) под действием света.
С4 -путь фиксации СО2. Описанный выше процесс включения СО2 в состав 3-фосфоглицерата (результат карбоксилазной реакции рибулозодифосфат-карбоксилазы/оксигеназы) называется С3-путем, а растения, в которых он осуществляется — С3-растениями. В то же время существует альтернативный С4-путь (цикл Хэтча—Слэка), отличающийся присутствием дополнительной начальной стадии — фиксации СО2 в составе четырехуглеродного соединения (оксалоацетата). Эту реакцию катализирует фосфоенолпируваткарбоксилаза — фермент, работающий гораздо быстрее, чем рибулозодифосфат-карбоксилаза/оксигеназа. В результате у С4-растений углекислота включается в состав оксалоацетата намного эффективнее, чем у С3-растений в состав 3-фосфоглицерата. Однако С4-путь требует дополнительных стадий и затрат энергии: на фиксацию одной молекулы СО2 здесь затрачивается 5 молекул АТР вместо 3 в С3-пути (рис. 13.6). Тем не менее, С4-растения (кукуруза, сахарный тростник, сорго, многие сорняки, произрастающие в умеренной зоне и др.) растут го-
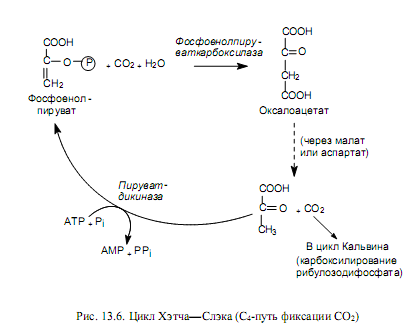
раздо быстрее, чем С3-растения (пшеница, рожь, овес, рис и др.). Причиной такого несоответствия служит фотодыхание — расточительный процесс, характерный для всех С3-растений и практически отсутствующий у С4 - растений.
Фотодыхание. Этот процесс обязан существованию оксигеназной активности рибулозодифосфат-карбоксилазы/оксигеназы. Молекулярный кислород конкурирует с СО2 за активный центр данного фермента, и часть рибулозо дифосфата превращается в фосфогликолат (рис.13.4). Этого не происходит у С4-растений, поскольку большинство их имеет своей родиной тропические страны, где высокое испарение влаги заставило растения выработать механизм закрывания устьиц, через которые ткани вентилируются газами, в самые жаркие часы дня (при максимальном солнечном освещении). Чтобы такой механизм не привел к снижению скорости фиксации СО2, растения запасают углекислоту в составе малата или аспартата (образуются из оксалоацетата в цикле Хэтча—Слэка), а затем расходуют по мере надобности (реакции декарбоксилирования). В этом случае концентрация СО2 в зеленых частях растений всегда находится на высоком уровне и отсутствует конкуренция О2 за активный центр фермента, поскольку молекулярный кислород поступает в клетки в ограниченных количествах при закрывании устьиц.
Субстратом фотодыхания служит гликолат, который образуется при дефосфорилировании фосфогликолата. При фотодыхании (в отличие от митохондриального дыхания, тоже характерного для растений в темноте) потребление О2 и выделение СО2 не связано с запасанием энергии, наоборот, здесь расходуются восстановительные эквиваленты и ATP, а фиксированный в цикле Кальвина углерод бесполезно теряется в виде СО2. Показано, что фотодыхание может приводить к реокислению и выделению до 50% углерода, фиксированного в цикле Кальвина. До сих пор не разгадана целесообразность этого столь неэкономного и ограничивающего эффективность роста растений процесса.
Последовательность событий фотодыхания изображена на рис.13.7. Можно видеть, что отдельные стадии этого процесса осуществляются в разных органеллах. Итогом фотодыхания является образование одной
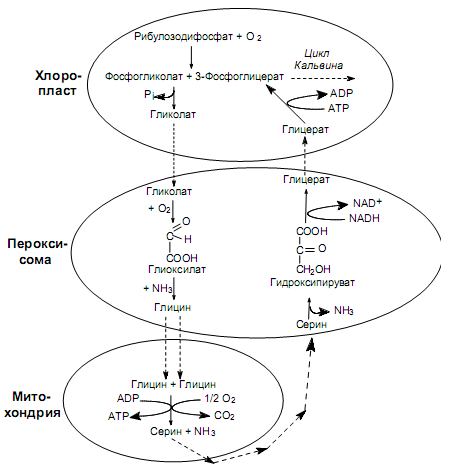
молекулы фосфоглицерата (3 атома «С») из двух молекул гликолата (4 атома «С»), а участие кислорода приводит к окислению четвертого атома углерода в углекислоту. По-видимому, назначение сложной последовательности превращений в фотодыхании состоит в том, чтобы вернуть в цикл хотя бы часть углерода из гликолата, который накапливается в избытке.
При фотодыхании происходит потеря одного атома углерода из каждых четырех, причем следует учитывать, что на фиксацию этого атома углерода уже затрачена энергия в цикле Кальвина. Кроме этого, при окислении глицина и дезаминировании серина выделяется аммиак, на включение которого в состав аминокислот снова придется затрачивать энергию. В результате фотодыхание снижает потенциальную урожайность С3-растений на 30—40%.
Дата добавления: 2016-05-30; просмотров: 3048;











