Примеры решения задач. Выразить состав полученного раствора всеми возможными способами
Задача 1. 50 г водного раствора FeCl2 с моляльностью 1,97 моль/кг с плотностью 1,332 г/см3 смешали со 150 мл 5 масс. % раствора FeCl2 с плотностью 1,038 г/см . Выразить состав полученного раствора всеми возможными способами.
Дано:
Раствор 1: Раствор 2:
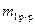 =50r
=50r 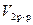 = 150 мл
= 150 мл
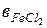 =1,97моль/кг
=1,97моль/кг 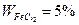
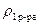 = 1,332 г/см3
= 1,332 г/см3 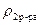 = 1,038 г/см3
= 1,038 г/см3
в = ? W = ? x = ?
Решение:
Для каждого раствора найдем массу FeCl2 и Н20.
Раствор 1: 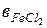 = 1,97 моль/кг, то есть на 1 кг воды приходится 1,97 моль FeCl2,
= 1,97 моль/кг, то есть на 1 кг воды приходится 1,97 моль FeCl2,
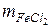 = l,97×MFeCl2 = 1,97∙127,5 =251 г;
= l,97×MFeCl2 = 1,97∙127,5 =251 г; 
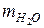 = 1000 г ; mp.pa= 1251 г
= 1000 г ; mp.pa= 1251 г
1251 г (р-ра) - 251г FeCl2 ;
50 г р-ра -  х FеCl2
х FеCl2
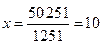 г.
г.
Итак, в растворе 1: 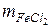 = 10 г;
= 10 г;
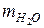 = 50 – 10 = 40 г.
= 50 – 10 = 40 г.
Раствор 2: m р.ра =r∙V = 1,038 ∙ 50 =156 г; 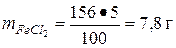
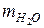 = 156-8= 148 г
= 156-8= 148 г
Раствор 3: m р-pa = 50 + 156 = 206 г ; 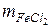 =10 + 8=18г mH2O =40+ 148 = 188 г
=10 + 8=18г mH2O =40+ 148 = 188 г
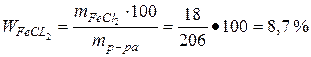
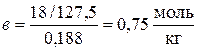
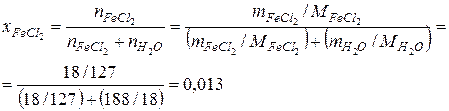
Рассчитать молярную концентрацию нет возможности, поскольку неизвестна плотность полученного раствора.
Задача 2.При 100 °С тетрахлорэтилен имеет давление насыщенного пара 400 мм.рт.ст., а бромбензол - 196 мм.рт.ст. при 100 °С. Найти состав раствора, кипящего при 100 °С под давлением 360 мм.рт.ст. и состав насыщенного пара над раствором. Считать раствор идеальным.
Дано:
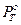 =400 мм.рт.ст.
=400 мм.рт.ст.
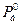 = 196 мм.рт.ст.
= 196 мм.рт.ст.
t = 100 °С
Pобщ = 360 мм.рт.ст.
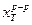 = ? хтпар = ?
= ? хтпар = ?
Решение:
Кипение наступает тогда, когда внешнее давление и давление насыщенного пара равны. Следовательно, 360 мм.рт.ст. - это и внешнее давление и общее давление насыщенного пара над раствором.
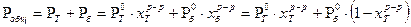
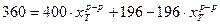
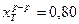 ;
; 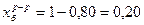
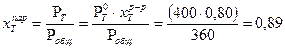
Задача 3.
При 25 °С константа распределения йода между водой и амиловым спиртом равна 0,00435. Сколько граммов иода останется в трех литрах водного раствора (С = 1,3 г/л) после двухкратной экстракции амиловым спиртом, если всего израсходовано 400 мл спирта?
Дано:
К = 0,00435 = 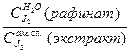
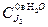 =1,3г/л
=1,3г/л
п = 2
V= 3 л
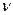 = 400/2 = 200 мл = 0,2 л
= 400/2 = 200 мл = 0,2 л
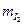 = ?
= ?
Решение:
Экстрагентом является амиловый спирт. Следовательно, данная константа распределения является обратной, требуемой в уравнении для расчета эффективности экстракции:
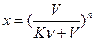
Рассчитываем константу распределения:
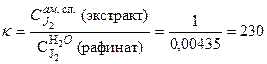
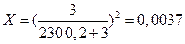 - доля йода, оставшегося в рафинате.
- доля йода, оставшегося в рафинате.
Масса растворенного йода в исходном растворе:
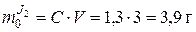
m = m0×x = 3,9 0,0037 = 0,014 г - масса йода, оставшегося в рафинате
ЭЛЕКТРОХИМИЯ
Дата добавления: 2016-06-22; просмотров: 2991;











