Результаты расчетов температурных инверсий по уравнению Ван-дер-Ваальса
Для основных газов.
| Газ | N2 | Ar | Воздух | H2 | He | O2 | Ne |
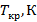
| 126,26 | 150,7 | 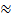 133 133
| 33,2 | 5,2 | 154,8 | 44,45 |

| 3,398 | 4,86 | 3,769 | 1,28 | 0,227 | 5,11 | 2,721 |
 , К , К
| 820,07 | 978,9 | 863,8 | 33,8 | 288,71 | ||
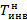 , К , К
| 105,84 | 126,3 | 117,5 | 27,7 | 4,36 | 130,0 | 37,26 |
 , МПа , МПа
| 30,58 | 43,78 | 33,9 | 11,7 | 2,03 | 46,0 | 24,5 |
Введение в низкотемпературное разделение газовых смесей методом ректификации.
Все низкотемпературные газы за исключением гелия получаются из воздуха.
При рассмотрении воздуха как газовой смеси используется бинарная модель N2- О2, либо тройная N2- О2-Ar.
При рассмотрении N2- О2, Ar присоединяют к азоту. В дальнейшем при извлечении других компонентов воздуха также рассматривают бинарные и тройные смеси.
Например, получившийся N2 как смесь N2- Ne, а для получения Ne – смесь Ne-He.

Рисунок 168. Схема ВРУ.
Рассмотрим только бинарную смесь. Состав газовой смеси будем выражать в мольных долях:
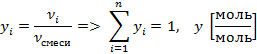
Бинарная смесь: 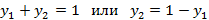
В смеси жидкостей также используют мольные доли.

Бинарная смесь: 
Кривая упругости компонентов бинарной смеси 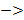 зависимость p(T).
зависимость p(T).
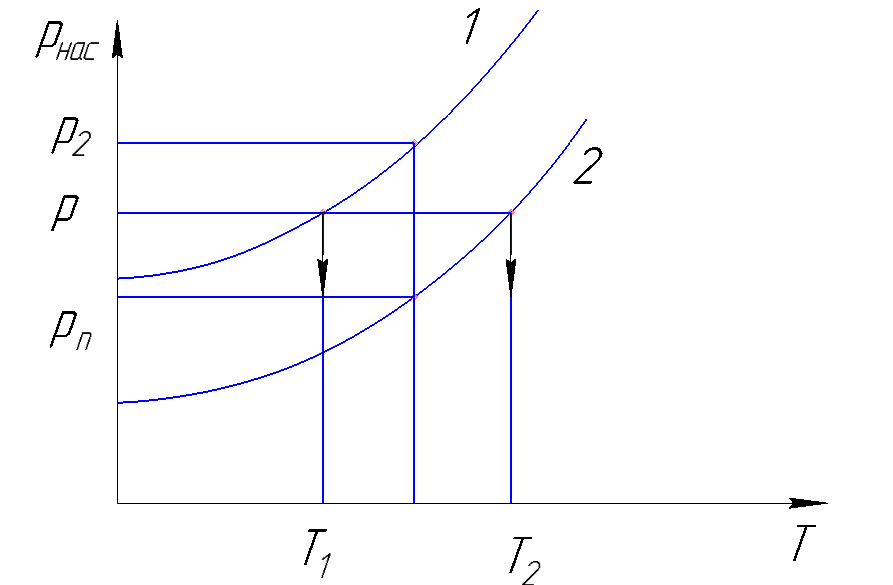
Рисунок 169. Кривая упругости компонентов бинарной смеси в pT координатах.
Поскольку при одинаковом давлении первый компонент имеет более низкую температуру кипения, то его называют низкокипящим компонентом смеси, а второй – высококипящим компонентом.
При одинаковой температуре высококипящий компонент имеет более низкое давление, а низкокипящий - более высокое.
Разность давлений является основной движущей силой стремления перейти компоненту из жидкого состояния в парообразное и наоборот. В этом свойстве заключена применимость метода низкотемпературной ректификации для разделения газовых смесей.
Характеристикой разделения бинарных газовых смесей является коэффициент летучести равный отношению давлений низкокипящего компонента к давлению высококипящего компонента при одинаковой температуре:

Если 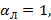 то данную смесь разделить методом низкотемпературной ректификации невозможно. Чем больше
то данную смесь разделить методом низкотемпературной ректификации невозможно. Чем больше  , тем легче разделить смесь.
, тем легче разделить смесь.
Дата добавления: 2016-06-22; просмотров: 1984;











