Функциональная система поддержания КЩС в организме
Понятие кислотно-щелочного состояния. pH (водородный) показатель
Соотношение кислоты и щелочи в каком-либо растворе называется кислотно-щелочным состоянием (КЩС). Тело человека имеет определенное кислотно-щелочное соотношение, характеризуемое pH (водородным) показателем (power Hidrogen – «сила водорода”), который показывает число водородных атомов в данном растворе.
· Значение показателя pH зависит от соотношения между положительно заряженными ионами (формирующими кислую среду) и отрицательно заряженными ионами (формирующими щелочную среду).
· Организм человека постоянно стремится уравновесить это соотношение, поддерживая строго определенный уровень pH. При нарушенном балансе могут возникать множество серьезных заболеваний.
· При pH равном 7,0 говорят о нейтральной среде.
· Чем ниже уровень pH – тем среда более кислая (от 6,9 до 0).
· Щелочная среда имеет высокий уровень pH (от 7,1 до 14,0).
Функциональная система поддержания КЩС в организме
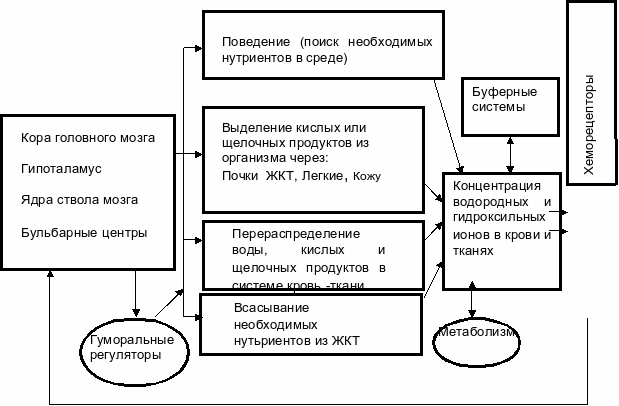
Кислотно-основное состояние поддерживается мощными гомеостатическими механизмами. В их основе лежат особенности физико-химических свойств буферных систем крови и физиологические процессы, в которых принимают участие системы внешнего дыхания, почки, печень, желудочно-кишечный тракт и др.
Буферные системы — это биологические жидкости организма. Роль буферных систем заключается в поддержании нормального рН крови.
Буферная система представляет собой смесь слабой кислоты и ее соли, образованной сильным основанием.
Попадание в плазму сильной кислоты вызывает реакцию буферных систем, в результате которой сильная кислота превращается в слабую. То же происходит и при действии на биологические жидкости сильного основания, которое после взаимодействия с буферными системами превращается в слабое основание.
В результате указанных процессов изменения рН либо не наступают, либо являются минимальными.
Все эти системы имеются в крови, где с их помощью поддерживается рН=7,4, несмотря на поступление в кровь из кишечника и тканей значительного количества кислот и небольшого оснований.
Поддержание постоянства активной реакции крови обеспечивается буферными системами, к которым относятся:
1. Бикарбонатная буферная система [угольная кислота — Н2СО3, бикарбонат натрия — NаНСО3)]- основной буфер межклеточной жидкости и крови, образуется в почках и облегчает выведение H+.
2. Фосфатная буферная система [одноосновный (NаН2РО4) и двухосновный (Nа2НРО4) фосфат натрия] - облегчает выведение Н+в канальцах почек. Основная роль состоит в регуляции КОС внутри клеток (особенно почек), поддерживает в крови «регенерацию» гидрокарбонатной системы.
3. Буферная система белков плазмы - главный внутриклеточный буфер. В кислой среде она связывает ионы водорода, в щелочной среде — отдает.
4. Буферная система гемоглобина [гемоглобин — калиевая соль гемоглобина] - играет основную роль в транспорте СО2от тканей к легким, начинает действовать в течении нескольких минут.
Дата добавления: 2016-05-28; просмотров: 5194;











