Радиационно–химические процессы
Химические процессы, протекающие в веществе и материалах под действием ионизирующего излучения, называются радиационно-химическими.
Поток частиц или квантов электромагнитного излучения высокой энергии (Е>~50 эВ), вызывающий в веществах образование ионов, называется ионизирующим излучением.
Ионизирующее излучение подразделяется на корпускулярное: поток электронов ( 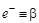 ), протонов (
), протонов ( 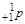 ), ядер гелия (
), ядер гелия ( 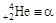 ) и т.п., и электромагнитное: g-излучение и рентгеновское излучение.
) и т.п., и электромагнитное: g-излучение и рентгеновское излучение.
Ионизирующее излучение возникает в результате распада ядер радиоактивных изотопов (радионуклидов): a-частицы – дважды ионизованные атомы гелия; b-частицы – электроны; g-излучение – кванты электромагнитного излучения. Оно также может генерироваться ускорителями заряженных частиц, например электронов, протонов, или рентгеновскими установками.
Для количественных оценок радиационно-химических процессов необходимо знать величину поглощенной в веществе энергии ионизирующего излучения. Энергия ионизирующего излучения, поглощенная веществом, в пересчете на единицу его массы называется поглощенной дозой (D). В системе СИ она измеряется в Греях [1Гр = 1 Дж/кг]. Доза, получаемая за единицу времени, называется мощностью поглощенной дозы (РD), измеряется в Гр/с. Зная величину мощности дозы и время облучения, можно рассчитать поглощенную дозу.
Под действием ионизирующего излучения в веществе образуются высокоактивные частицы: ионы, радикалы, возбужденные молекулы, которые вступают в различные химические реакции между собой и со средой. Образование высокоактивных частиц в результате взаимодействия частиц потока ионизирующего излучения с атомами и молекулами вещества является первичным актом радиационно-химического процесса. Необходимо отметить, что вследствие большой энергии проходящая через вещество частица излучения может произвести ионизацию значительного числа атомов.
Рассмотрим основные механизмы взаимодействия частицы излучения с одним атомом.
Основными механизмами первичного акта взаимодействия в случае поглощения кванта электромагнитного излучения являются фотоэффект, комптоновское рассеяние и образование электрон-позитронных пар. Вероятность протекания первичного акта по тому или иному механизму будет зависеть от энергии излучения (Ehn) и заряда ядра (Z) атомов.
Фотоэффект – процесс, в результате которого энергия кванта излучения полностью передается электрону, который выбивается из атома. Фотоэффект играет существенную роль для квантов с малой энергией (Ehn< 0,1 МэВ) при взаимодействии с атомами имеющими Z > 20.
Комптоновское рассеяние (Compton) – процесс, в котором фотон (квант излучения) в результате упругого столкновения с электроном атома теряет часть своей энергии и изменяет направление движения, а из атома выбивается электрон отдачи. Взаимодействие по механизму эффекта Комптона преобладает в широкой области энергий фотонов (~0,1 МэВ < < Ehn< ~10 МэВ) и поэтому является основным механизмом первичного акта взаимодействия электромагнитного ионизирующего излучения с веществом.
Образование электрон-позитронных пар – процесс превращения g-кванта в кулоновском поле ядра или электрона в пару электрон-позитрон. Заметную роль этот процесс играет при больших энергиях g-кванта (Ehn> 10 МэВ).
Основным механизмом первичного акта взаимодействия заряженных частиц является электромагнитное взаимодействие с электронами вещества (ионизация и возбуждение атомов). По этому механизму частицы теряют до ~90% своей энергии. Кроме того они теряют энергию при изменении своей скорости в кулоновском поле ядра в виде тормозного рентгеновского излучения. Отметим, что рассмотренные механизмы имеют место не только для первичных заряженных частиц, но и для вторичных, возникающих при ионизации.
В зависимости от вида (электромагнитное или корпускулярное) и энергии, а также химического состава вещества, с которым оно взаимодействует, частицы ионизирующего излучения будут проникать на различную глубину. Как правило, электромагнитное излучение проникает в вещество на большую глубину, чем заряженные частицы. Кроме того, продукты первичных актов взаимодействия будут сконцентрированы вдоль пути прохождения частицы через вещество. Эти обстоятельства приводят к тому, что развитие дальнейших процессов протекает в неравновесных условиях.
Независимо от типа ионизирующего излучения, в результате первичных актов его взаимодействия с веществом образуются промежуточные частицы: сольватированные электроны (электроны, образовавшие ассоциаты с молекулами жидкости), ионы и ион-радикалы, свободные радикалы и атомы, возбужденные молекулы. Как правило, при обычных условиях эти частицы обладают высокой реакционной способностью и поэтому являются короткоживущими. Они быстро (за время порядка 10-14 – 10-7 с) взаимодействуют между собой и с молекулами среды с образованием стабильных продуктов.
Суммарный процесс, включающий как первичные акты взаимодействия, так и вторичные химические реакции, называют радиолизом. Энергетической характеристикой радиолиза является радиационно–химический выход G(X) – величина, показывающая число частиц (молекул, ионов, радикалов и т.д.), образующихся или расходующихся в веществе при поглощении 100 эВ энергии ионизирующего излучения.
Пример.Под действием ионизирующего излучения в воде протекают следующие основные реакции (радиолиз воды)
1. Образование возбужденных молекул (H2O*), ионы и электроны (1):
1. 2H2O ® H2O* + H2O+ + е-.
2. Образование промежуточных нестабильных частиц за счет: диссоциации возбужденных молекул воды (2), рекомбинации ионов с образованием возбужденных молекул и их последующей диссоциацией (3), гидратации электронов (4), ион-молекулярных реакций (5):
2. H2O* ®H· + OH·.
3. H2O+ + е- ® H2O* ®H· + OH·.
4. H2O + е- ®H· + OH-.
5. H2O+ + H2O ® H3O+ + OH·.
3. Образование стабильных продуктов радиолиза воды: газообразного водорода (6) и перекиси водорода (7):
6. H· + H· ® H2.
7. OH· + OH· ® H2O2.
Если система замкнута, газообразный водород принимает участие в обратных реакциях (8, 9). После определенной дозы облучения в системе устанавливается равновесие, концентрация стабильных продуктов в воде не увеличивается:
8. H2 + OH· ® H2O + H·.
9. H2O2 + H·® H2O + OH·.
Радиационно-химический выход продуктов радиолиза воды (pH = 7) при облучении g-радиацией: G(-H2O)=3,64; G(H2)=0,42; G(H2O2)=0,71; G(H*)= 2,80.
В случае если система открытая и газообразные продукты реакции уходят из раствора, то за счет реакций
H2O2 + OH·® H2O + HO2·, HO2· + HO2· ® H2O2 + O2
происходит образование эквивалентной смеси газообразного водорода и кислорода ("гремучий газ") и суммарное уравнение радиолиза имеет вид
2H2O ®2 H2 + O2.
Для описания процесса радиолиза в твердом теле пользуются зонной моделью. Ионизирующее излучение приводит к образованию электронов (е) и дырок (р). Электроны и дырки, мигрируя по кристаллической решетке, во-первых, могут рекомбинировать. Образующиеся при этом возбужденные частицы могут излучать избыточную энергию в виде кванта света (люминесценция) или передавать решетке в виде тепловых колебаний. Во-вторых, электроны и дырки могут взаимодействовать с решеткой с образованием дефектов различной структуры. Например, образовывать дефекты, поглощающие видимый свет (центры окраски), в результате чего твердое тело окрашивается. Так, в щелочно-галоидных кристаллах анионная вакансия (Va), захватившая электрон, образует дефект, который называется F-центр (1); межузельный (HI) и решеточный ионы галогена (HG), захватившие дырку, образуют Vк-центр (2):
1. Va+ е–® F.
2. HI + HG + p® Vк.
Макрокинетика
При рассмотрении кинетики гомогенных реакций считается, что выполняются два условия. Во-первых, при протекании процесса концентрация реагирующих частиц в каждой точке объема в любой момент времени одинакова, т. е. скорость реакции достаточно мала по сравнению с процессами диффузии; во-вторых, температура во всех точках системы одинакова и не меняется в ходе реакции, т. е. система находится в состоянии термического равновесия. Считается, что процесс осуществляется в равновесных условиях, т. е. время воздействия на систему (время изменения концентрации реагирующих веществ) много больше, чем время релаксационных процессов (время выравнивания концентрации и температуры в реакционном объеме за счет массо- и теплопереноса).
В отдельных случаях скорость химической реакции сравнима или больше скорости процессов массопереноса. Тогда кинетика реакции будет определяться законами диффузии. Такие процессы называются диффузионно–контролируемыми. Если в процессе химического превращения отдельные части реакционного объема в результате протекания химических реакций имеют различную температуру, изменяющуюся во времени, то говорят о протекании неизотермических процессов. Очевидно, что неравенство температур в отдельных частях реакционного объема связано с неравенством концентраций реагентов.
Макрокинетика (макроскопическая кинетика) изучает законы протекания химических реакций в реальных системах в их взаимосвязи с физическими процессами переноса массы вещества и теплообмена, такими как диффузия, конвекция, теплопередача.
При описании любых химических реакций необходимо учитывать процессы переноса вещества и теплообмена внутри системы, но во многих случая их влиянием на кинетику можно пренебречь. В то же время описание гетерогенных процессов, горения и взрыва возможно только с привлечением макрокинетических представлений.
Дата добавления: 2020-02-05; просмотров: 719;











