Теоретические основы процесса обжига
ОБЖИГ ЦИНКОВЫХ КОНЦЕНТРАТОВ
Первой металлургической операцией в производстве цинка любым методом является обжиг цинковых концентратов с целью перевода сульфидных соединений цинка в окисленные. В процессе обжига сера удаляется с печными газами в виде сернистого ангидрида, а находящиеся в огарке окислы цинка могут быть в дальнейшем выщелочены по гидрометаллургической технологии слабыми растворами серной кислоты для получения сульфатного цинкового раствора или восстановлены углеродом до металла при пирометаллургическом (дистиляционном) способе.
Существует несколько разновидностей обжига. При производстве цинка пирометаллургическим методом концентраты вначале подвергают неполному (до 10 -12% серы) окислительному обжигу на порошок, а затем спекают полуобожженный материал на агломерационных машинах. При этом стремятся нацело удалить серу из концентрата и превратить обожженный материал в пористый крупнокусковый продукт - агломерат. Стремление удалить серу при обжиге как можно полнее объясняется тем, что при последующем восстановлении и возгонке цинка каждый 1 % серы в агломерате уносит с собой в отвальный продукт (раймовку) 2% цинка, чем значительно снижает извлечение металла в товарную продукцию.
При гидрометаллургическом способе получения цинка к обожженному концентрату предъявляются более жесткие требования, поэтому обжиг концентратов в этом производстве преследует следующие цели:
1) перевести в окислы максимальное количество сульфидов металлов (огарок должен содержать минимальное количество сульфидной серы);
2) оставить в обожженном продукте небольшое (заданное) количество сульфатной серы, обычно в пределах 3 - 4%, для компенсации потерь серной кислоты в процессе производства;
3) получить как можно меньше нерастворимых в серной кислоте ферритов цинка;
4) не допустить образования большого количества силикатов свинца и цинка, затрудняющих отстаивание и фильтрацию растворов;
5) получить обожженный продукт в виде тонкого порошка с большой реакционной поверхностью.
При этом необходимо также обеспечить максимальную концентрацию сернистого ангидрида в обжиговых газах и улавливание возгонных цветных и редких металлов.
Таким образом, обжиг цинковых концентратов в гидрометаллургии является окислительно - сульфатизирующим.
Окисление сульфидов кислородом воздуха протекает по экзотермической необратимой реакции:
| MeS + 1.5 O2 = MeO + S O2 + Q | (1) |
При нагревании сульфидов в воздухе при определенной температуре скорость реакции достигает такой величины, при которой в результате выделения тепла в ходе реакции дальнейший процесс окисления может протекать без подвода тепла извне. Эта температура называется температурой воспламенения сульфидов и зависит от рода сульфида и крупности его зерен.
Скорость процесса окисления твердого сульфида кислородом воздуха определяется условиями диффузии газов через корку окислов, покрывающую внутреннюю, неизменившуюся часть сульфида. Внутрь зерна диффундирует кислород, навстречу ему - сернистый газ. По мере окисления сульфида корка окислов постепенно утолщается, условия диффузии газов ухудшаются, и скорость реакции замедляется. Отсюда следует, что с увеличением размера зерна время, необходимое для полного окисления сульфида, значительно возрастает.
Так можно представить процесс окисления одного зерна сульфида. На практике обжигу подвергают цинковый концентрат, состоящий из большой массы сульфидных зерен. Поэтому продолжительность обжига зависит еще и от условий подвода кислорода воздуха к каждому зерну сульфида и отвода от него сернистого газа. По этой причине механические многоподовые обжиговые печи являлись наименее производительными агрегатами. Концентрат располагался в них на подах слоем 50 – 100 мм, и доступ воздуха к зернам сульфидов, находящимся внутри слоя, был затруднен.
Перегребание слоя специальным механизмом и пересыпка концентрата с пода на под несколько ускоряли процесс окисления сульфидов, но в целом этот способ обжига как малопроизводительный устарел и больше не применяется. Для обжига на поду были характерны также низкая концентрация сернистого ангидрида в обжиговых газах, трудность регулирования температуры, затраты углеродистого топлива и тяжелые условия во время горячих ремонтов печей.
При более интенсивном способе обжига во взвешенном состоянии сухой цинковый концентрат распыляется сверху воздушной горелкой в рабочее пространство обжиговой печи с раскаленными стенками, в результате чего создается огромная поверхность для взаимодействия распыленного концентрата с кислородом воздуха. При этом зерно сульфида находится в потоке горячих газов, содержащих кислород, что обеспечивает более высокую скорость окисления сульфидов.
При обжиге в кипящем слое раскаленный толстый (1000 - 1500 мм) слой обжигаемого материала непрерывно продувается воздухом через большое количество отверстий в подине печи. При этом в слое создаются интенсивные вихревые потоки, обеспечивающие быстрое распределение свежей массы концентрата по всему объему реакционной части печи и высокие скорости окисления сульфидов.
Обжиг сульфидных цинковых концентратов ведут при избытке воздуха. Поэтому в отходящих из печи газах наряду с SO2 и N2 находится довольно значительное количество кислорода. При интенсивных способах обжига, (во взвешенном состоянии и в кипящем слое) избыток воздуха меньше, а степень использования кислорода выше, благодаря чему концентрация сернистого ангидрида в газах больше.
Выше были изложены лишь основные вопросы теории окисления сульфидов. Для понимания происходящих при обжиге цинковых концентратов процессов необходимо знать поведение всех компонентов концентрата при обжиге.
Соединения цинка
В сульфидных цинковых концентратах цинк представлен главным образом сфалеритом (ZnS) и марматитом (mZnS · nFeS). Coгласно оксидной теории обжига окисление сернистого цинка протекает по реакциям
| 2ZnS + 3O2 = 2ZnO + 2SO2 ; | (2) |
2SO2+ O2 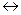 2O3 ; 2O3 ;
| (3) |
ZnO + SO 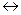 ZnSO4 . ZnSO4 .
| (4) |
Как следует из реакций (2) - (4), эта теория предполагает сначала образование окиси цинка, а затем уже при соответствующих условиях сульфата. По сульфатной теории вначале образуется сульфатцинка, а окись является продуктом последующего разложения сульфата под действием температуры, как это показано следующими уравнениями реакции:
| ZnS + 2O2 = ZnSO4 ; | (5) |
ZnSO4 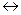 ZnO+ So3 ; ZnO+ So3 ;
| (6) |
2SO3 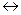 2SO2 +O2 . 2SO2 +O2 .
| (7) |
Сульфатная теория не исключает, однако, и возможности образования сульфата цинка по вторичной реакции:
ZnO + SO3 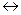 ZnSO4 . ZnSO4 .
| (8) |
Обе теории согласуются с данными практики в том, что в результате окисления сульфида цинка в обжиговой печи одновременно образуются окись и сульфат цинка, сернистый и серный ангидриды. Соотношение указанных продуктов окисления сульфида цинка в твердой и газовой фазах определяется условиями проведения обжига и, в частности, температурой процесса, избытком воздуха, наличиемкатализаторов и другими факторами. Реакция окисления сульфида цинка с образованием окиси
| 2ZnS + 3O2 = 2ZnO + 2SO2 + 460050 Дж | (9) |
идет самопроизвольно при температурах, превышающих температуру воспламенения ZnS. Последняя, по данным различных исследователей, находится в пределах 550 - 615°С. Сравнительно высокая по отношению к другим сульфидам температура воспламенения ZnS и слабая способность крупных зерен сульфида цинка к декриптации затрудняют процесс обжига цинковых концентратов и в большей степени требуют создания условий, способствующих ускорению реакции окисления. Такими условиями являются малая величина зерна, высокая температура процесса, достаточный избыток воздуха, полнота контакта зерна сульфида цинка скислородом.
Цинковые флотационные концентраты представляют собой тон-коизмельченный материал с размером частиц 60 - 70% - 0,074 мм, что вполне удовлетворяет первому условию и обеспечивает при других благоприятных факторах высокую скорость окисления сульфидов, если концентраты хорошо подготовлены к обжигу.
С повышением температуры скорость окисления резко возрастает. Вместе с тем температура процесса для каждого вида концентрата определяется его химическим и вещественным составом, так как с повышением температуры наряду с основной реакцией окисления сульфида цинка протекают побочные и вторичные реакции, ухудшающие показатели обжига и качества огарка. В связи с этим оптимальная температура процесса зависит также и от рода аппарата, в котором ведут обжиг. В печах кипящего слоя она допускается выше, чем в многоподовых механических печах, и поддерживается в пределах 900-1000° С.
Быстрое окисление сульфида цинка происходит лишь при достаточном избытке воздуха, когда обеспечивается поддержание необходимой концентрации кислорода на поверхности зерен и эвакуация газообразных продуктов обжига из слоя материала или зоны взаимодействия реагирующих веществ. В то же время чрезмерный избыток воздуха приводит к снижению концентрации сернистого ангидрида в обжиговых газах, так как последние разбавляются азотом, поступающим с воздухом в зону реакции в значительно большем количестве, чем кислород. Обжиг в печах с кипящим слоем позволяет достигать высоких показателей окисления сульфидов при минимальном избытке воздуха.
Важнейшим фактором форсированного обжига цинковых концентратов является тесный и непрерывный контакт зерен сульфида с кислородом воздуха. Наилучшие условия для этого созданы в печах кипящего слоя, благодаря чему производительность и показатели работы этих агрегатов значительно выше, чем печей иного типа. В процессе взаимодействия соединений цинка с кислородом одновременно с окислением сульфидов до окиси протекают и другие реакции, имеющие важное значение для получения высококачественного огарка или для последующих технологических переделов и гидрометаллургического производства цинка. К ним относятся реакции ферритообразования, сульфатообразования и получения силикатов цинка, растворимых в слабой серной кислоте.
Ферритообразование
При наличии в цинковых концентратах минерала марматита или сульфидов железа в процессе обжига образуется метаферрит цинка ZnO·Fe2O3, который не растворяется в слабой серной кислоте и остается неизменным в остатке от выщелачивания огарка, снижая тем самым прямое извлечение цинка в раствор. Количество образующегося метаферрита цинка тем больше, чем выше содержание железа в цинковом концентрате. Поэтому перед обогатительными фабриками всегда стоит задача снижения содержания железа в продуктах цинковой флотации, а действующий отраслевой стандарт ограничивает его содержание в цинковых концентратах следующими пределами:
| Марка концентрата | КЦ1 | КЦ2 | КЦ3 | КЦ4 |
| Допустимое содержание железа, % |
Если сульфиды цинка и железа присутствуют в концентрате в виде марматита (mZnS∙nFeS), т. е. в изоморфной кристаллической форме, то каждая массовая часть железа нацело связывает в феррит при окислительном обжиге 0,58 массовой части цинка. В случае, если сульфид железа находится в структурно-свободном состоянии (пирит) или связан с другим сульфидом (халькопирит), степень ферритообразования будет определяться температурой процесса и полнотой контакта соединений железа и цинка.
Предупредить образование феррита цинка при температуре выше 650° С практически невозможно, однако он может частично разрешаться сернистым и серным ангидридами. Поэтому для снижения ферритообразования необходимо при обжиге создавать условия, способствующие повышению концентрации в газовой фазе сернистого и серного ангидридов и разъединению соединений цинка и железа. В печах для обжига в кипящем слое создаются эти условия, однако снизить заметно степень ферритообразования при этом практически не удается.
Сульфатообразование
Длительной практикой установлено,что в обожженном концентрате необходимо оставлять 3 - 4% сульфатной серы. Недостаток водорастворимых сульфатов в огарке вызывает повышенный расход серной кислоты, идущей на пополнение ее убыли в гидрометаллургическом цикле, а избыток их приводит к чрезмерному увеличению удельного веса растворов и ухудшению отстаивания пульпы. В обоих случаях это нежелательно, так как при этом увеличиваются затраты на производство, а себестоимость цинка возрастает. Поэтому условия обжига цинковых концентратов выбирают из расчета получения в огарке указанного выше количества сульфатной серы.
В процессе обжига возможно образование сульфатов цинка, железа, меди, свинца, кадмия, кальция, магния, марганца и других металлов. Часть этих сульфатов (FeSO4, CuSO4) разлагается при температуре выше 600° С. Сульфаты кальция, магния, свинца и цинка устойчивы при более высоких температурах (800 - 1200° С). Следовательно, не все образующиеся при обжиге сульфаты будут находиться в обожженном материале. Об устойчивости сульфатов в процессе обжига можно судить по температуре их разложения, приведенной в табл. 3.
Технологов интересует в первую очередь сульфат цинка, количество которого получается в огарке больше по сравнению со всеми остальными сульфатами.
Согласно существующим теориям, процесс образования сульфата цинка протекает по следующим реакциям:
ZnS + 2O4 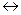 ZnSO4; ZnSO4;
| (10) |
ZnO + SO3 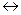 ZnSO4 ; ZnSO4 ;
| (11) |
2SO3 + O2 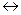 2SO3 . 2SO3 .
| (12) |
Для образования сульфата цинка по уравнению (10) достаточно обеспечить взаимодействие сульфида цинка с кислородом воздуха. В печи кипящего слоя для этого имеются благоприятные условия. Свежая порция сульфидного цинкового концентрата, попадая в раскаленный кипящий слой и нагреваясь до температуры обжига, непосредственно вступает в тесный контакт с воздушным дутьем. Однако высокая температура процесса (900 - 1000° С) вызывает разложение образовавшегося сульфата цинка. Поэтому большее содержание водорастворимого цинка наблюдается в циклонной пыли, состоящей из наиболее тонких частиц обожженного концентрата, быстро выносимых потоком газов из зоны высоких температур.
Образование сульфата цинка по реакции (11) тесно связано с условиями протекания реакции (12). При 500°С сернистый ангидрид в присутствии кислорода воздуха окисляется до серного, а выше 600° С реакция идет в обратном направлении, в сторону разложения серного ангидрида на сернистый газ и кислород. При наличии в зоне реакции (12) катализаторов, например окислов железа и меди, способствующих разложению молекулы кислорода на два активных атома, образование серного ангидрида ускоряется. При повышенных содержаниях железа и меди в цинковом концентрате сульфатизация окиси цинка возможна также за счет SO3, выделяющегося при разложении сульфатов железа и меди.
Таблица 3
Температура разложения сульфатов, ° С [4]
| Сульфаты | Начало разложения | Энергичное разложение | Продукт разложения |
| FeSO4 | Fe2O3·2SO3 | ||
| Fe2O3·2SO3 | Fe2O3 | ||
| Al2(SO4)3 | Al2O3 | ||
| ZnSO4 | 3ZnO·2SO3 | ||
| 3ZnO·2SO3 | ZnO | ||
| CuSO4 | 2CuO·SO3 | ||
| 2CuO·SO3 | CuO | ||
| PbSO4 | 6PbSO·5SO3 | ||
| 6PbSO·5SO3 | 2PbSO·SO3 | ||
| MgSO4 | MgO | ||
| MnSO4 | Mn2O4 | ||
| CaSO4 | - | CaO | |
| CdSO4 | - | 5CdO·SO3 | |
| 5CdO·SO3 | - | CdO |
В печах кипящего слоя имеются надлежащие условия и для образования сульфата цинка по реакции (11), так как концентрация сернистого ангидрида и кислорода в газовой фазе достаточна для получения серного ангидрида. Препятствием для оставления в огарке необходимого количества сульфата цинка служит, как и в случае реакции (10), быстрое разложение его при высокой температуре обжига. Как следует из табл. 3, разложение ZnSO4 начинается при 702° С и протекает энергично при температуре 720 - 767°С. С повышением температуры скорость диссоциации резко увеличивается и при 850° С она в 17 раз выше, чем при 750° С [4]. В связи с этим добиться оставления некоторой части сульфата цинка в обожженном продукте можно только путем сокращения продолжительности пребывания частиц концентрата в зоне высоких температур.
Теория и практика обжига цинковых концентратов в кипящем слое позволяет сделать следующее заключение об условиях образования и разложения сульфата цинка:
1. Образование сульфатного цинка при обжиге происходит как путем прямого окисления сульфида цинка, так и посредством вторичной реакции сульфатизации окиси цинка серным ангидридом.
2. Значительные количества сульфата цинка можно получить только при пониженных температурах обжига (не выше 700 °С). Получение некоторого количества вся дорастворимого цинка в огарке при высоких температурax (900 - 1000 °С) возможно лишь при кратковременном пребывании материала в печи.
3. Процессу сульфатообразования цинка способствует содержание в обжигаемых цинковых концентратам соединений железа и меди.
4. Для протекания вторичной реакции образования сульфата цинка решающее значение имеет концентрация сернистого ангидрида и кислорода в газовой фаза а также наличие катализаторов.
Дата добавления: 2016-06-05; просмотров: 3979;











