Принципы построения периодической системы элементов
Явление периодичности с позиций современного строения атомов объясняется тем, что через определённое число элементов появляются элементы с аналогичной электронной структурой. Например, рассмотрим элементы 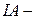 группы:
группы:
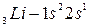 .
.
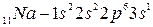 .
.
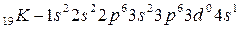 .
.
Периодическая система состоит из периодов, рядов и групп.
Период – горизонтальный ряд элементов, имеющий одинаковое число энергетических уровней (электронных слоёв), номер периода совпадает со значением главного квантового числа 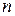 внешнего уровня (слоя). Периодов в системе
внешнего уровня (слоя). Периодов в системе 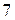 , их них
, их них 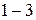 короткие,
короткие, 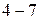 длинные, которые имеют чётные и нечётные ряды (таблица
длинные, которые имеют чётные и нечётные ряды (таблица  ). Каждый период начинается типичным металлом (щелочным элементом), имеющим электронную конфигурацию
). Каждый период начинается типичным металлом (щелочным элементом), имеющим электронную конфигурацию 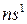 , а при переходе слева направо происходит постепенное ослабление металлических и нарастание неметаллических свойств; заканчивается период благородным газом
, а при переходе слева направо происходит постепенное ослабление металлических и нарастание неметаллических свойств; заканчивается период благородным газом 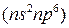 .
.
По вертикали периодическая система подразделяется на восемь групп, которые делятся на главные – 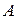 , состоящие из
, состоящие из 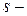 и
и 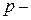 элементов, и побочные –
элементов, и побочные – 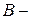 подгруппы,содержащие
подгруппы,содержащие 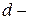 и
и 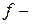 элементы. Подгруппа
элементы. Подгруппа 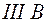 , кроме
, кроме 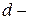 элементов, содержит по
элементов, содержит по 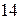
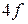 и
и 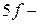 элементов. Это семейства лантаноидов и актиноидов соответственно. Главные подгруппы содержат на внешнем электронном слое одинаковое число электронов, которое равно номеру группы.
элементов. Это семейства лантаноидов и актиноидов соответственно. Главные подгруппы содержат на внешнем электронном слое одинаковое число электронов, которое равно номеру группы.
В главных подгруппах валентные электроны (электроны, способные образовывать химические связи) расположены на 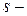 и
и 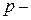 орбиталях внешнего энергетического уровня, в побочных – на
орбиталях внешнего энергетического уровня, в побочных – на 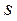 -орбиталях внешнего и
-орбиталях внешнего и 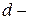 орбиталях предвнешнего слоя. Для
орбиталях предвнешнего слоя. Для 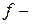 элементов валентными являются
элементов валентными являются 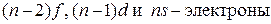 , где
, где 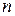 равно
равно 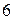 или
или 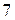 для лантаноидов и актиноидов соответственно.
для лантаноидов и актиноидов соответственно.
Дата добавления: 2016-06-05; просмотров: 3107;











