Фокально-сегментарный гломерулосклероз (ФСГС)
В последние несколько десятилетий отмечается рост частоты ФСГС во всем мире.
Морфологическая картина. Характерно наличие склероза (гиалиноза) в некоторых капиллярных петлях в части клубочков. Наличие даже одного клубочка с сегментарным склерозом дает основание диагностировать ФСГС. В начале изменения появляются в юкстамедуллярных клубочках, затем этот процесс распространяется по всему корковому слою. Пораженная долька клубочка часто срастается с капсулой Боумена (синехия). При ЭМ выявляется фокальное слияние ножек подоцитов в клубочках без склероза, а в склерозированных зонах подоциты на ГБМ могут отсутствовать (отрыв подоцитов от ГБМ и слущивание их в просвет канальцев). ГБМ, будучи «липкой», адгезирует к соседним капиллярным петлям или капсуле Боумена, чем и объясняется образование синехий и солидификация капиллярных петель. При ИГХ имеет место отложение IgM и С3 в склерозированных участках. Изменения в тубулоинтерстициальном пространстве соответствуют выраженности поражения клубочков. При длительном течении ФСГС или при тяжелых его вариантах выявляются атрофия канальцев, интерстициальный фиброз, лимфогистиоцитарные инфильтраты, пенистые клетки в канальцах и в интерстиции, резорбция протеиновых (гиалиновых) капель в канальцевом эпителии, гиалиноз артериол. Различаются несколько вариантов ФСГС:
1) неуточненная форма (когда ФСГС трудно отнести к одному из нижеперечисленных вариантов);
2) клеточный вариант: в пораженных дольках наблюдается гиперклеточность, связанная с пролиферацией эндотелиальных клеток, моноцитов и наличием нейтрофильных лейкоцитов. Кроме того, могут присутствовать гиалин и/или фибрин. Вся картина более характерна для фокально-сегментарного пролиферативного ГН;
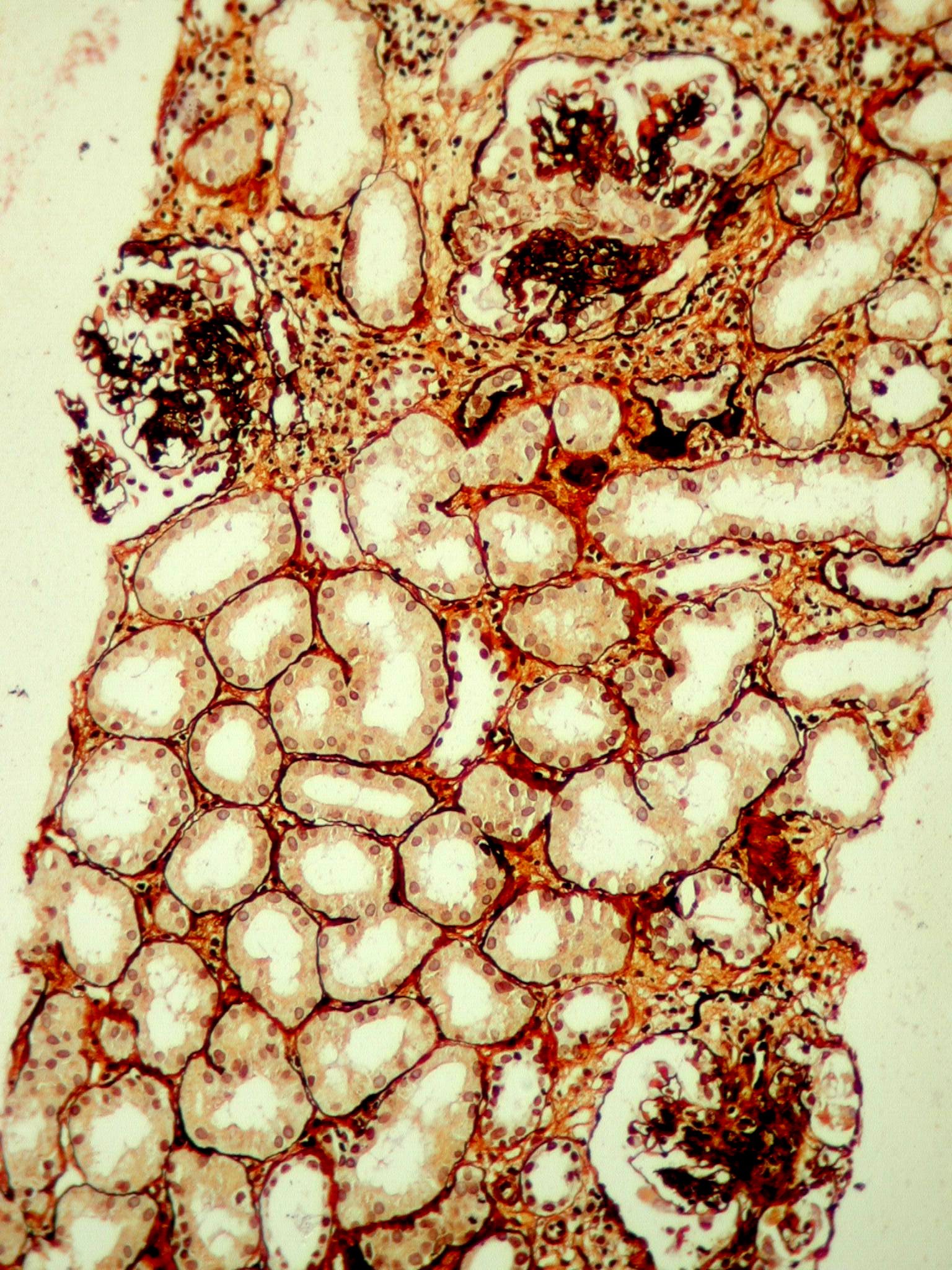
3) коллабирующий вариант: коллапс петель клубочка, обусловленный неконтролируемой пролиферацией подоцитов. (рис. 4.4А);
4) верхушечный вариант: самый благоприятный по течению, сегментарный склероз расположен у тубулярного полюса клубочка. Отдельные петли клубочка пролабируют в каналец (рис. 4.4В);
5) перихилярный вариант: склеро-/ гиалиноз в области впадения приводящей артериолы в клубочек с частичным гиалинозом самой артериолы. Характерен для вторичного ФСГС на фоне артериальной гипертензии, ожирения и сахарного диабета;
6) Clq-нефропатия: диффузные и глобальные депозиты C1q в мезангии с ФСГС.
А
В
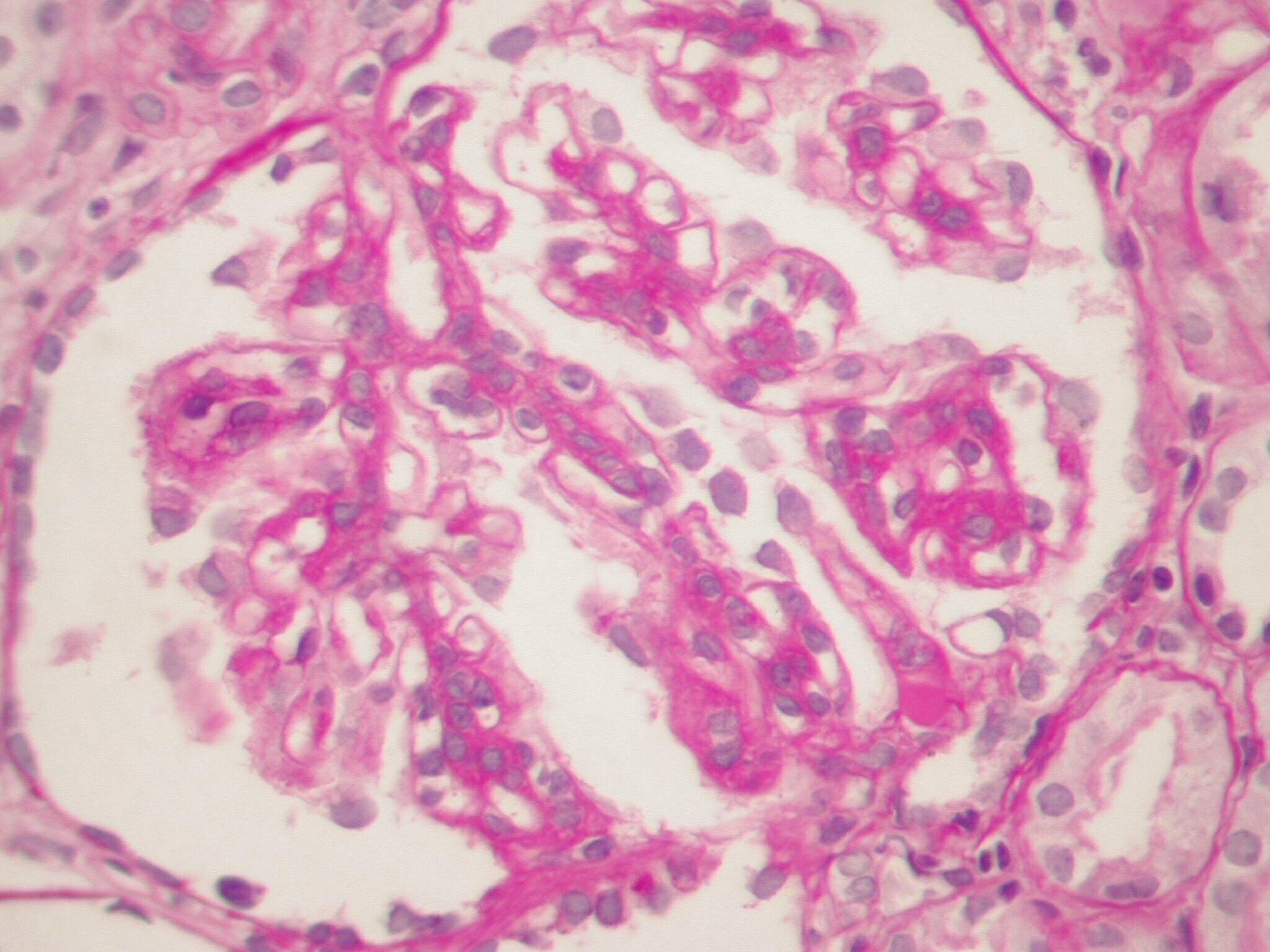
Рисунок 4.4. Фокально-сегментарный гломерулосклероз (Микрофотографии – О.А.Воробьева, Санкт-Петербург, 2007). А. Коллабирующий вариант: коллапс петель клубочка (справа), обусловленный неконтролируемой пролиферацией подоцитов, серебро-метенамин по Джонсу, х100. Мальчик А., 15 лет, нефротический + нефритический синдром. В. Верхушечный вариант (справа). Солидификация капиллярных петель, обращенная в область проксимального канальца, PAS х 400. Мальчик Т., 7 лет, нефротический синдром, стероид-резистентный вариант
Патогенетические механизмы ФСГС.
Выделяют идиопатический, вторичный и генетический варианты ФСГС.
В основе идиопатического предполагают участие тех же патогенетических механизмов с нарушением Т-клеточного иммунитета, что и при нефротическом синдроме с минимальными изменениями. В настоящее время идиопатический ФСГС как у детей, так и у взрослых рассматривают как стадию одного заболевания (переход БМИ в ФСГС, часто – верхушечный вариант) [10]. Причины сегментарного склерозирования отдельных клубочков связывают с иными циркулирующими факторами (suPAR и другие). Определенная роль отводится протеинурии как таковой, вызывающей гиперфильтрацию в клубочках, ведущую к повреждению капилляров, их коллапсу и склерозу. Существенная роль принадлежит подоцитам, в частности их митохондриальной дисфункции. Помимо этого может наблюдаться так называемая подоцитопения, когда количество подоцитов на ГБМ уменьшается за счет их апоптоза, индуцированного ангиотензином II и проапоптотическими цитокинами, а также за счет отрыва «живых» подоцитов от ГБМ в мочевое пространство. На участках, лишенных подоцитов, происходит интенсивная потеря белка, более того, возникают синехии с капсулой, что является характерным признаком ФСГС и одной из причин склероза и спадения капилляров.
Классифицирование ФСГС должно начинаться с исключения всех причин вторичного ФСГС. Это имеет важное терапевтическое значение. Вторичный ФСГС может развиться при инфекциях (ВИЧ, ВГВ и С), системных воспалительных и аутоиммунных болезнях, лимфопролиферативных заболеваниях, длительной артериальной гипертензии, рефлюкс-нефропатии. Появлением ФСГС может осложниться ожирение и другие метаболические нарушения. Причиной ФСГС могут быть лекарства (героиновая нефропатия, интерферон-α, анаболические стероиды), практически любые состояния, сопровождающиеся уменьшением количества функционирующей почечной паренхимы.
Вторичный ФСГС может быть стадией прогрессирования любой гломерулопатии, но при этом должны наблюдаться гистопатологические признаки первичной болезни в отличие от идиопатического варианта ФСГС. Генетические варианты ФСГС разбираются ниже.
Клиническая картина
ФСГС проявляется прежде всего протеинурией различной степени выраженности, вплоть до развернутого НС. НС в дебюте заболевания чаще встречается у детей, чем у взрослых. Сочетание с микрогематурией может отмечаться у 40-50% больных, у небольшой части (до 5%) заболевание протекает с эпизодами макрогематурии. АГ несколько чаще выявляется у взрослых, чем у детей. У части больных уже при первом обследовании может быть снижение СКФ. При вторичных формах ФСГС отеки встречаются значительно реже, даже при наличии протеинурии нефротического уровня и гипоальбуминемии (кроме случаев ВИЧ-ассоциированной и героиновой нефропатий).
Морфологически при вторичном ФСГС выявляется перихиллярный вариант, гломеруломегалия, характерно фокальное сглаживание ножек подоцитов в отличие от диффузных изменений при идиопатическом ФСГС.
Течение и прогноз. При отсутствии лечения ФСГС прогрессирует с развитием терминальной стадии хронической почечной недостаточности (тХПН). У пациентов с протеинурическим вариантом ФСГС прогноз относительно более благоприятен. ТХПН может наступить через десятки лет от дебюта заболевания. Предикторами неблагоприятного течения заболевания являются следующие факторы:
• персистирующая массивная протеинурия;
• нарушение функций почек в момент выявления заболевания;
• коллабирующий вариант ФСГС;
• распространенное повреждение (атрофия канальцев, склероз более 20%).
Существенным предиктором длительного сохранения функций почек при ФСГС с НС является достижение ремиссии, полной (у взрослых - протеинурия менее 0,3 г/сут) или частичной (протеинурия 0,3-3,5 г/сут) [6]. При достижении ремиссии 5-летняя выживаемость составляет 100% даже у больных с коллабирующим вариантом ФСГС. В целом, при достижении ремиссии терминальная стадия ХПН развивается менее чем у 15% пациентов.
У детей течение идиопатического ФСГС принципиально не отличается от такового у взрослых; тем не менее имеются сообщения о лучшем ответе на терапию и лучшей почечной выживаемости у больных с дебютом заболевания в возрасте менее 12 лет.
Лечение
Целью лечения при ФСГС является сохранение функций почек пациента в течение как можно более длительного времени и купирование активных проявлений НС. Даже частичная ремиссия обеспечивает существенное улучшение исходов.
1.Используются общие принципы лечения любой протеинурии:
• Диета с ограничением соли (менее 3г/сут), ограничением белка (0,8-2,0 г/кг) с адекватным калоражем
• ИАПФ (фозиноприл, периндоприл и др.) или БРА (лозартан, вальсартан и др.)
• Антагонист альдостерона (спироналактоны в малой дозе 12,5-25 мг/сут).
2.Иммуносупрессивная терапия проводится только при идиопатическом ФСГС.
· В качестве инициальной терапии рекомендуются глюкокортикостероиды (ГКС), которые назначаются у взрослых как минимум 4 недели (дозы как при БМИ) до достижения полной ремиссии. Стероидрезистенность устанавливается при отсутствии ремиссии через 16 недель (при удовлетворительной переносимости ГКС). После достижения ремиссии дозу ГКС снижают постепенно в течение 6 месяцев, при стероид-резистенности – отмена ПЗ в течение 6 недель.
· У пациентов (у детей и взрослых) с ФСГС при определении стероид-резистенности или при наличии противопоказаний или непереносимости высоких доз ГКС (диабет, психические заболевания, тяжелый остеопороз) в качестве терапии первой линии, проводится лечение ингибиторами кальцинейрина (ИКН): циклоспорином А (ЦсА), при непереносимости ЦсА - такролимусом.
Механизм действия циклоспорина А заключается в том, что он вызывает спазм приводящей артериолы клубочков и снижение проницаемости ГБМ для белка, что также может снижать протеинурию, независимо от его иммуносупрессивной активности. Терапия ЦсА, проводится в дозе 3-5 мг/кг/сут (микроэмульсионная форма) в двух равно разделенных дозах в течение не менее 6 месяцев. Целевая С0 концентрация – 100-200 нг/мл.
В случае достижения ремиссии продолжают в течение как минимум 12 месяцев, далее с попыткой медленной отмены со снижением дозы ЦсА на 25% каждые 2 месяца. При отсутствии ремиссии в течение 6 месяцев лечение следует прекратить. Рекомендуется комбинировать с малыми дозами ГКС. Лечение иАПФ или БРА является обязательным в отличие от БМИ.
Использование ЦсА при ФСГС ограничено нефротоксичностью препарата: на фоне терапии возможно повышение уровня креатинина крови, АГ, при морфологическом исследовании – очаги атрофии почечных канальцев, усиление фиброза интерстиция, артериолосклероз. При этом клинически функции почек могут оставаться сохранными, Считается, что токсическое действие его более выражено в случае распространенных склеротических изменений в клубочках и интерстиции, уже существующих к началу терапии нарушениях функций почек (повышенного уровня креатинина), а также превышении дозы ЦсА>5,5 мг/кг/сут. Большинство исследователей рекомендуют проведение повторной нефробиопсии через 2—3 года от начала лечения ЦсА с целью контроля его побочных эффектов.
· Такролимусв дозе 0,1-0,2 мг/кг/сут в два приема (целевой уровень – 5-10 нг/мл). При ФСГС такролимус (FK506) обладает сходным с ЦсА механизмом действия и меньшей нефротоксичностью. Он может индуцировать ремиссию у части, но не у всех больных, резистентных к другим видам лечения – ГКС и ЦсА.
· Мофетила микофенолатв дозе по 750-1000 мг 2 раза в день в течение 6 месяцев и более. Отсутствие нефротоксичности выгодно отличает микофенолат мофетила (ММФ) – селективный иммуносупрессивный препарат, угнетающий пролиферацию лимфоцитов и моноцитов, а также нарушающий адгезию активированных лимфоцитов к эндотелиальным клеткам. Имеются сообщения о его эффективности в сочетании со стероидами и ингибиторами АПФ у больных с различными первичными гломерулопатиями, в том числе и ФСГС. KDIGO (2012) рекомендуют ММФ и высокие дозы дексаметазона при непереносимости ЦсА у больных с ФСГС.
· По применению РитуксимабаприФСГС пока недостаточно рандомизированных исследований, хотя остается многообещающим препаратом.
· Изучается эффективность и других препаратов (ACTH, абатасепт –CTLA-4).
· Возврат ФСГС в почечном трансплантате происходит в 30% случаев. ФСГС, развивающийся в трансплантате, требует интенсивного лечения комбинацией пульсов МП, плазмафереза.
Проводим следующий клинический случай из детской практики.
Мальчик Г., 6 лет, при первом поступлении болен 1 год. В дебюте неполный нефротический синдром без отеков, с протеинурией 2,8 г/л, СОЭ 28 мм/ч. Лечился по месту жительства преднизолоном 40 мг/с в течение 8 недель, ремиссия НС достигнута только на 6-й неделе лечения. I рецидив развился на фоне снижения дозы ПЗ до 10 мг/48ч и на фоне пневмонии. Терапевтический индукционный курс ПЗ и пульс-терапия метилпреднизолоном №2 эффекта не дали, сохранялась протеинурия 6,6 г/л.
При поступлении отмечается обострение НС с анасаркой, АД 110/80 мм.рт.ст., умеренный экзогенный гиперкортицизм, СОЭ 74 мм/ч, гипохромная анемия, протеинурия 8,5 г/с и эритроцитурия 20-22 в п/зр. Проведена чрескожная пункционная биопсия левой почки.
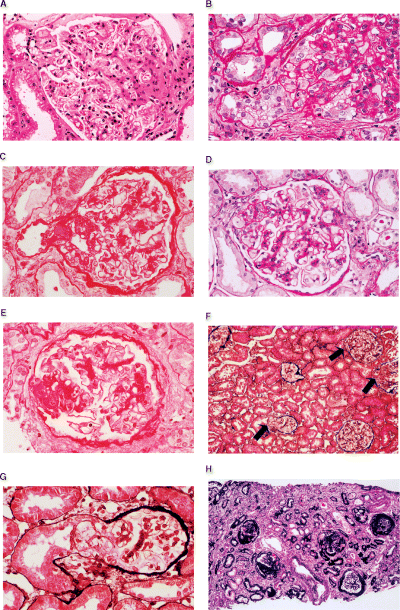 При световой микроскопии в препарате среди имеющихся 16 клубочков в 4 (25%) – сегментарный склероз капиллярных петель у тубулярного полюса клубочков с пенистыми клетками в зоне склероза. В 2 других клубочках имеется легкая мезангиальная пролиферация. Три клубочка выглядят увеличенными в размерах. Остальные клубочки не изменены. Канальцы – диффузные дегенеративные изменения, легкая атрофия. Интерстиций – легкий фокальный фиброз. Артерии и артериолы не изменены (рис. 4.5А).
При световой микроскопии в препарате среди имеющихся 16 клубочков в 4 (25%) – сегментарный склероз капиллярных петель у тубулярного полюса клубочков с пенистыми клетками в зоне склероза. В 2 других клубочках имеется легкая мезангиальная пролиферация. Три клубочка выглядят увеличенными в размерах. Остальные клубочки не изменены. Канальцы – диффузные дегенеративные изменения, легкая атрофия. Интерстиций – легкий фокальный фиброз. Артерии и артериолы не изменены (рис. 4.5А).
А
В
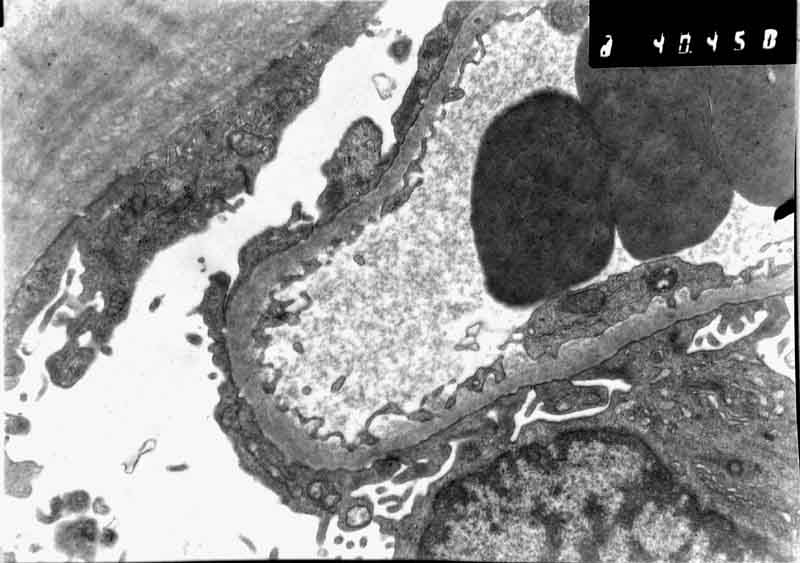
Рисунок 4.5. Верхушечный вариант фокально-сегментарного гломерулосклероза у ребенка Г., 6 лет (Микрофотографии – А.В.Суханов, Москва, 2004 г.)
А – Сегментарная окклюзия просветов капилляров клубочка с увеличением мезангиального матрикса и гиалинозом. Адгезия к капсуле Боумена в области перехода в проксимальный каналец. ШИК-реакция х250
В – Диффузное сглаживание ножек подоцитов. Электронная микроскопия х4000
При иммунофлюоресцентном исследовании отмечалось свечение IgM, С3 в мезангии и по периферии капиллярных петель 2+. При электронной микроскопии отмечается диффузное сглаживание малых ножек подоцитов (рис. 4.5В). Депозитов иммунокомплексного типа нет. Базальная мембрана капиллярных петель не утолщена. Имеется участок сегментарного склероза капиллярных петель в районе выхода проксимального канальца. В интерстиции имеются пенистые клетки.
Морфологическое заключение: Фокальный сегментарный гломерулосклероз, верхушечный вариант.
Клинико-морфологический диагноз: Стероид-резистентный нефротический синдром, с фокально-сегментарным гломерулосклерозом, верхушечным вариантом. Хроническая болезнь почек, I стадия.
В лечение подключена интенсифицированная схема лечения: циклоспорин А (Сандиммун Неорал) в терапевтической дозе 150 мг/м2/с, преднизолон 20мг/48ч, иАПФ. На фоне лечения через 2 месяца развилась полная ремиссия нефротического синдрома, длившаяся 1 год. В последующем по месту жительства – рецидивы нефротического синдрома почти ежегодно вследствие недостаточной дозы циклоспорина А. До 2014 года лечение пульсами МП, увеличение дозы циклоспорина приводило к полной ремиссии. Использовалось сочетание ЦсА с ММФ и иАПФ. Повторная биопсия противопоказаний к ЦсА не обнаружила. До настоящего времени СКФ остается нормальной. Но в 2014 году все вышесказанное лечение не приводило к ремиссии. Начато лечение Ритуксимабом.
Следующий клинический случай. Пациентка Г., 24лет (1990 г.р.)
Дебют в начале августа 2014г. с появления отеков на нижних конечностях до паховой складки. Повышение САД до 160 мм.рт.ст. В июне 2014г – солнечная инсоляция. Лечение – антибиотики, симптоматическое. Настоящая госпитализация в КазНИИ Кардиологиии и внутренних болезней – плановая, для проведения биопсии почки по поводу нефротического синдрома. Наследственный анамнез: по материнской линии – АГ. Состояние средней степени тяжести, за счет симптомов гипергидратации. Выраженные отеки. ЧСС 74 в мин. АД 132/70 мм.рт.ст.
Лабораторные и инструментальные исследования:
ОАК (20.08.14г-05.09.14г): Hb- 117-119 г/л, эритроциты- 4,7-4,95*1012/л, Ht- 37,4%, L- 4,1-6, *109/л, Тромбоциты-330,0 *109/л. СОЭ-21-60мм/ч.
ОАМ (21.08.14г-05.09.14г): цвет-с\ж, уд. вес – 1025-1015 , проз- полн, белок++++ 10-5,1г/л, pН-6.0, лейкоциты- нет, бактерии+, кровь++, 50 rbc\мкл
Биохимические исследования крови (21.08.14г-03.09.14г): креатинин - 46-63мкмоль/л, общий белок – 37-42г/л, мочевина - 6,7-3,7ммоль/л, глюкоза-4,5ммоль/л, Na-134,4-144,1ммоль/л, К-5-5,1ммоль/л.
Коагулограмма(20.08.2014): АЧТВ-24,3, ПТВ-20,1, ПТИ-87,3, МНО-1,60.
ИФА на гепатиты (27.08.2014): гепатит С (суммарные антитела) отрицательно, HBsAg отрицательно.
ЭКГ (20.08.2014): Ритм синусовый с ЧСС 75 в мин., регулярный. Гипертрофия ЛЖ. Нарушение процессов реполяризации.
Эхо-КГ (21.08.2014): КСР 27.1, КДР 44.4, ТЗСЛЖ 7.5, ТМЖП 8.7, ПЖ 11.3, Доа-25.6, ЛП 25.6, ДО-89 мл, СО 27 мл, УО 52 мл, ФВ 69%. Сократительная способность левого желудочка удовлетворительная. Дополнительная хорда в полости левого желудочка.
Дата добавления: 2017-10-04; просмотров: 7144;











