Транспорт в почечных канальцах
Транспорт через эпителиальные трубочки в общем виде рассмотрен в разделе «Трансклеточная проницаемость» главы 4 и проиллюстрирован на рис. 4–9 и 26–7. В этом разделе разобрано канальцевое (трансэпителиальное) перемещение конкретных веществ, т.е. их реабсорбция (из просвета канальцев в интерстиций и далее в околоканальцевые кровеносные капилляры) и секреция (из просвета капилляров в интерстиций и далее в просвет канальцев).
Na+
Из поступающих в организм при сбалансированной диете 120 ммоль Na+ лишь 15% удаляется через потовые железы и ЖКТ, а 85% экскретируется с мочой. Каждые сутки почки отфильтровывают 25 500 ммоля и реабсорбируют 25 400 ммоля Na+, что примерно эквивалентно полутора килограммам поваренной соли. Поскольку вода пассивно перемещается между компартментами вслед за Na+ (и сопутствующим Cl–), ясно, сколь большое значение имеют почки для поддержания объёма жидкостей организма и их осмоляльности.
· Градиент реабсорбции (рис. 26–9А). Реабсорбция Na+ (также CI–) наибольшая в проксимальном извитом канальце, постепенно уменьшается в проксимо–дистальном направлении и наименьшая в собирательных протоках.
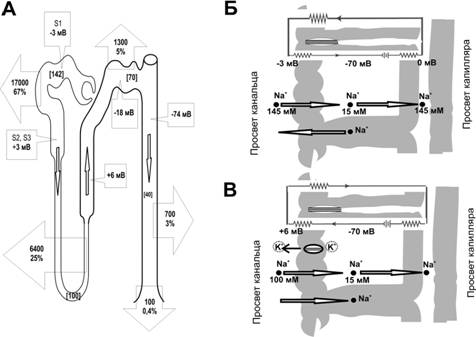
Рис. 26–9. РЕАБСОРБЦИЯ НАТРИЯ [2]. А. Реабсорбция Na+ в разных отделах почечных канальцев. Стрелки в просвете канальцев — направление движения фильтрата. Концентрация Na+ в просвете проксимального извитого канальца, петли Хенле, дистального извитого канальца нефрона и в собирательных трубочках и протоках приведена в миллимолях (мМ, в прямых скобках). Количество реабсорбируемого Na+ в сутки (миллимоль/сут и % от отфильтрованного Na+) приведено внутри стрелок, направленных из просвета канальца. Указана также трансэпителиальная разность электрохимического потенциала (DmNa, мВ).Б. Механизм транспорта Na+ в проксимальном извитом канальце (сегмент S1). Реабсорбция Na+ из просвета канальца в интерстиций показана стрелками, направленными слева направо (трансклеточный путь). Na+ входит в клетку по его концентрационному градиенту (приведены значения концентрация Na+ в миллимолях), но выходит из клетки в интерстиций против градиента концентрации. В нижней части рисунка показано обратное движение Na+ по парацеллюлярному пути, частично замкнутому плотными контактами (показаны в верхней части рисунка). В верхней части рисунка дана электрическая схема зарядов в разных частях канальца, из которой следует неизбежность движения катионов в просвет канальца по парацеллюлярному пути. В. Механизм реабсорбции Na+ в толстом отделе петли Хенле. Реабсорбция Na+ из просвета канальца в интерстиций показана стрелками, направленными слева направо (трансклеточный путь). Na+ входит в клетку по его концентрационному градиенту, но выходит из клетки в интерстиций против градиента концентрации. В нижней части рисунка показана реабсорбция Na+ по парацеллюлярному пути, частично замкнутому плотными контактами (показаны в верхней части рисунка). В верхней части рисунка дана электрическая схема трансэпителиальной стенки, из которой следует неизбежность движения катионов из просвета канальца по парацеллюлярному пути. Положительный заряд на канальцевой поверхности эпителия зависит от работы множества калиевых каналов, по которым из цитозоля в просвет канальца поступает K+.
· Пути и направление транспорта. Через стенку почечного канальца транспорт Na+ и Cl– (как и транспорт других ионов и воды) происходит как трансклеточно (сквозь клетку), так и по околоклеточному (парацеллюлярному) пути (рис. 26–7 и 26–9Б,В).
à Трансклеточный путь. Na+ последовательно проходит через верхушечную плазматическую мембрану в цитозоль и далее через боковые и базальные (базолатеральные) плазматические мембраны в интерстиций и через стенку капилляра в кровь. Скорость и объём транспорта зависят от разности электрохимического потенциала (DmNa) между просветом канальца и интерстицием, но в значительно большей степени от переносчиков, ионных каналов и насосов, встроенных в верхушечную и базолатеральную плазматическую мембрану.
à Околоклеточный путь. Na+ перемещается не через эпителиальную клетку, а по пространствам между соседними эпителиальными клетками. При этом скорость и объём пассивного перемещения, а также его направление определяются градиентом трансэпителиального электрохимического потенциала (DmNa), а также характеристиками плотных контактов между соседними клетками.
¨ Движущая сила пассивного транспорта электролита X по околоклеточному пути (в том числе Na+) — разность электрохимического потенциала (DmX) по обе стороны эпителия. При этом положительные значения mNa (см. рис. 26–7 и эквивалентную электрическую схему на рис. 26–9Б) на поверхности эпителия со стороны канальца способствуют пассивной реабсорбции Na+, а отрицательные, напротив, движению Na+ из интерстиция в просвет канальца. Именно поэтому по околоклеточному пути реабсорбция Na+ происходит только в сегментах S2 и S3 проксимальных канальцев и в толстом колене петли Хенле (см. рис. 26–9В), тогда как во всех остальных отделах почечных канальцев — в обратном направлении, то из интерстиция в просвет канальца.
¨ Na+ может также перемещаться против градиента mNa, увлекаемый потоками воды (вода перемещается вследствие активного транспорта Na+) из просвета канальца в пространства между клетками.
· Механизмы канальцевого переноса Na+ через верхушечную и базолатеральную плазмолемму различны в силу того обстоятельства, что существенно отличается внеклеточная (внутриканальцевая и интерстициальная) и внутриклеточная [Na+]. При реабсорбции Na+ пассивно входит в цитозоль через верхушечную плазмолемму, так как внутриклеточная [Na+] существенно ниже внутриканальцевой (15 мМ против 142–40 мМ в разных отделах канальцев, см. рис. 26–9А,Б). В то же время через базолатеральную клеточную мембрану Na+ активно выкачивается из клетки, так как внеклеточная, т.е. интерстиция [Na+] существенно выше внутриклеточной (145 мМ против 15 мМ, см. рис. 26–9Б).
à Выход Na+ из клетки в интерстиций на всём протяжении почечных канальцев обеспечивает Na+,K+–АТФаза. Этот энергозависимый от окислительного фосфорилирования процесс столь велик, что значительное потребление кислорода почками (до 10% от всего потребления O2 организмом) в первую очередь и преимущественно обеспечивает работу базолатеральной Na+,K+–АТФазы.
à Вход Na+ в клетку
¨ Проксимальный каналец. Вход Na+ по электрохимическому градиенту реализует несколько типов электрогенных котранспортёров, одновременно с Na+ переносящих в клетку против их электрохимического или только концентрационного градиента глюкозу, аминокислоты, фосфаты, сульфаты, лактат, другие моно-, а также дикарбоновые кислоты. В то же время в просвет канальцев через электронейтральный Na+-H+–ионообменник поступает H+. В начальном отделе проксимального канальца (сегмент S1, см. рис. 26–9Б) около трети реабсорбированного Na+ по околоклеточному пути пассивно поступает обратно в просвет канальца (обратная утечка Na+).
¨ Тонкий отдел петли. Транспорт Na+ как в нисходящем, так и в восходящем отделах происходит пассивно по околоклеточному пути.
¨ Толстый отдел петли Хенле (рис. 26–9В). Реабсорбция Na+ происходит как по трансклеточному, так и по околоклеточному пути.
Ä Трансклеточный путь. Na+ поступает в цитозоль через Na+-H+–ионообменник и Na+/K+/Cl–‑котранспортёр (переносит в клетку на каждый ион Na+ 1 ион K+ и 2 иона Cl–). Активность этого сочетанного переноса ингибируют мочегонные средства группы т.н. «петлевых диуретиков» (например, фуросемид и буметанид).
Ä Околоклеточный путь. Особенность толстого отдела петли Хенле, как и сегментов S2 и S3 проксимального извитого канальца, заключается в положительном заряде на канальцевой поверхности эпителия (см. рис. 26–9В). В результате создаётся направленная из просвета канальцев электродвижущая сила для диффузии катионов (Na+, K+, Ca2+ и Mg2+) по околоклеточному пути. Поскольку проницаемость стенки толстого отдела петли Хенле для воды низка, то поток катионов из просвета канальца приводит к тому, что канальцевая жидкость становится гипоосмотичной.
¨ Дистальный извитой каналец. Реабсорбция Na+ происходит по трансклеточному пути. В канальцевую плазмолемму встроены Na+/Cl–‑котранспортёры, чувствительные к тиазидным диуретикам.
¨ Собирательная трубочка. Na+ поступает из просвета канальца в цитозоль главных клеток при помощи натриевых каналов, чувствительных к диуретику амилориду.
¨ Собирательный проток. Здесь происходит минимальная (около 3%) реабсорбция Na+.
· Регуляция канальцевого транспорта Na+ осуществляется по следующим направлениям: автоматическая коррекция реабсорбции в проксимальных и дистальных канальцах вследствие изменений почечного кровотока (следовательно, фильтрации) и влияние на реабсорбцию в дистальном и отчасти в проксимальном отделах нефрона, а также в петле Хенле и особенно в собирательных трубках и протоках гуморальных и нервных факторов, увеличивающих или уменьшающих канальцевый транспорт Na+.
à Изменения почечной гемодинамики непосредственно сказываются на СКФ (см. выше «Регуляция почечного кровотока и фильтрации»). В свою очередь реабсорбция Na+ линейно и прямо пропорционально зависит от объёма отфильтрованного Na+, что полностью справедливо для проксимального и отчасти для дистального отделов нефрона, реабсорбирующих более 70% всего отфильтрованного Na+ (67% + 5%, рис. 26–9А). Этот механизм в проксимальных канальцах практически не зависит от нервных и гормональных влияний. Другими словами, параметры реабсорбции Na+ в проксимальных и дистальных канальцах автоматически подстраиваются к параметрам фильтрации Na+: увеличение фильтрации увеличивает реабсорбцию Na+, а уменьшение фильтрации уменьшает объём реабсорбированного Na+. Как видим, этот механизм существенно важен для поддержания постоянства объёма внеклеточной жидкости в организме. В то же время реабсорбция Na+ в дистальном и отчасти в проксимальном отделах нефрона, а также в петле Хенле и особенно в собирательных трубках и протоках находится под контролем ряда гуморальных факторов.
à Факторы, увеличивающие реабсорбцию Na+, т.е. приводящие к задержке Na+ и воды в организме: альдостерон, вазопрессин (АДГ) и влияния симпатического отдела нервной системы.
¨ Альдостерон стимулирует реабсорбцию Na+ в собирательных трубочках и протоках, что составляет лишь 3% отфильтрованного Na+, но заведомо больше ежедневного поступления Na+ в организм. Под влиянием альдостерона происходит увеличение транскрипции генов, кодирующих натриевые и калиевые каналы апикальной и Na+,K+–АТФазу базолатеральной поверхности главных клеток.
¨ Аргинин вазопрессин (АДГ), взаимодействуя со связанными с Gs-белком рецепторами, что приводит к увеличению внутриклеточной концентрации цАМФ и дальнейшим эффектам на белки–мишени, стимулирует реабсорбцию Na+ в толстом отделе петли Хенле и в собирательных трубочках и протоках.
Ä В толстом отделе петли Хенле происходит активация Na+/K+/Cl–-транспортёра и K+‑каналов верхушечной поверхности клеток, что способствует формированию гипертонического интерстиция.
Ä В главных клетках увеличивается количество открытых натриевых каналов верхушечной поверхности эпителия.
Ä Суммарный эффект вазопрессина (АДГ) на мочеобразовательную функцию почек — образование концентрированной мочи, т.е. задержка в организме воды. Этот эффект достигается увеличением проницаемости для воды стенки собирательных трубок и протоков, в результате вода выходит из просвета этих канальцев в гипертонический интерстиций.
¨ Норадреналин, освобождаемый из терминалей симпатического отдела нервной системы, через a–адренергические рецепторы активирует Na+,K+–АТФазу базолатеральной и Na+-H+–ионообменник апикальной поверхности клеток канальцев.
à Факторы уменьшающие реабсорбцию Na+, т.е. приводящие к усилению диуреза и потенциально могущие привести к потере Na+ и обезвоживанию организма: атриопептин, Пг, брадикинин, дофамин и эндогенный ингибитор Na+,K+–АТФазы.
¨ Атриопептин (посредством стимуляции рецепторной гуанилатциклазы и увеличения внутриклеточной концентрации цГМФ) подавляет активность катионных каналов на верхушечной поверхности клеток собирательных протоков. Кроме того, атриопептин косвенно уменьшает реабсорбцию Na+, увеличивая СКФ, перфузию почек, секрецию ренина и вазопрессина (АДГ).
¨ Эндогенный ингибитор Na+,K+–АТФазы. Активность Na+,K+‑АТФазы, взаимодействуя с участком связывания K+, подавляет сердечный гликозид уабаин (этот стероид содержится в древесине Acocanthera ouabaio и в семенах Strophanthus gratus, его эффект аналогичен действию гликозидов наперстянки). При увеличении поступления в организм поваренной соли, а также у больных с повышенным АД вырабатывается эндогенный ингибитор Na+,K+‑АТФазы, подавляющий её активность в собирательных протоках, что способствует выведению Na+ из организма.
¨ Простагландин E2 и брадикинин, действуя через протеинкиназу C и фосфорилируя Na+‑каналы на канальцевой поверхности эпителия, подавляют реабсорбцию Na+.
¨ Дофамин через D1- и D2-рецепторы увеличивают внутриклеточную концентрацию цАМФ, что приводит к подавлению активности Na+,K+‑АТФазы базолатеральной и Na+-H+–ионообменника апикальной поверхности клеток канальцев.
· Гипонатриемия и гипернатриемия
à Гипонатриемия. Гипонатриемией называют состояния, при которых концентрация натрия в сыворотке крови имеет значения ниже 135 мЭкв/л. Различают изотоническую и гипотоническую гипонатриемию.
¨ Изотоническая гипонатриемия (псевдогипонатриемия) возникает при переходе воды из внутриклеточной жидкости во внеклеточную. Переход обусловлен наличием осмотически активных частиц (например, глюкозы) в жидкости внеклеточного пространства. При этом концентрация натрия в сыворотке крови уменьшается за счёт гемодилюции (разведения крови). Другими словами, не происходит абсолютного снижения содержания натрия в организме, и значения осмоляльности внеклеточной жидкости остаются нормальными или даже выше нормы.
¨ Гипотоническая гипонатриемия (истинная гипонатриемия) возникает при абсолютном снижении натрия в организме и начинает приобретать клиническое значение, когда концентрация натрия в сыворотке крови становится менее 125 мЭкв/л, а осмоляльность сыворотки — ниже 250 мОсм/кг.
à Гипернатриемия — повышение концентрации натрия в крови выше 155 мЭкв/л. При гипернатриемии увеличение осмоляльности внеклеточной жидкости вызывает движение воды из клеток, что приводит к их обезвоживанию.
CI–
Реабсорбция Cl– происходит как по трансклеточному, так и по околоклеточному пути. Объёмы реабсорбции Cl– в разных отделах почечных канальцев практически такие же, как и для Na+ (см. рис. 26–9Б). Cl– поступает в цитозоль против концентрационного градиента путём обмена внеклеточного Cl– на внутриклеточные анионы. Выход Cl– в интерстиций по всему протяжению почечных канальцев обеспечивают Cl–‑каналы, а в проксимальном отделе нефрона дополнительно K+/Cl–-контранспортёр.
· Проксимальные канальцы. Особенность разных сегментов (S1, S2, S3) проксимальных канальцев состоит в том, что канальцевая поверхность эпителия в сегменте S1 заряжена отрицательно, а сегментов S2 и S3 — положительно. Поэтому по околоклеточному пути, как и для Na+, в сегментах S2 и S3 происходит движение Cl– из канальцев в интерстиций, но в сегменте S1 — утечка Cl– в просвет канальца из интерстиция. Транспорт Cl– из канальца в цитозоль против концентрационного градиента происходит за счёт встроенных в апикальную плазмолемму молекул антипортов, обменивающих внеклеточный Cl– на внутриклеточные анионы (оксалаты, HCO3–, OH– и др.).
· Толстый отдел петли Хенле. Реабсорбция Cl– происходит только по трансклеточному пути: вход Cl– из канальца в клетку осуществляют Na+/K+/Cl–‑котранспортёры, перемещающие на каждый ион Na+ 2 иона Cl–.
· Дистальный каналец. Вход Cl– в клетку из просвета канальца происходит за счёт Na+/Cl–‑котранспортёра.
· Собирательные трубочки и протоки. Главные клетки реабсорбируют Cl– по околоклеточному пути, а вставочные клетки типа b переносят Cl– в цитозоль при помощи Cl-HCO3-ионообменника.
Вода
Реабсорбция воды по всему протяжению почечных канальцев происходит только пассивно. Из 170 л отфильтрованной воды в проксимальных канальцах реабсорбируется 67%, в петле Хенле — 15%, от 10 до 15% — в собирательных трубках и протоках, не происходит реабсорбции воды в дистальном канальце нефрона. Реабсорбцию воды обеспечивают мембранные водные поры — аквапорины разных типов. Различные ЛС (диуретики), подавляя реабсорбцию Na+, увеличивают экскрецию и Na+, и воды, тем самым уменьшая в организме объём внеклеточной жидкости.
· Диуретики. Ниже приведены характеристики наиболее распространённых диуретиков.
Ú Ацетазоламид (мишень — карбоангидраза проксимальных извитых канальцев).
Ú Допамин (мишень — Na-H-ионообменник проксимальных извитых канальцев), стимуляторы: ангиотензин II, симпатическая стимуляция, a–адренергические агонисты; ингибитор: дофамин.
Ú Петлевые (фуросемид, буметанид, этакриновая кислота). Мишень: Na,K,Cl‑котранспортёр толстого сегмента петли Хенле, стимулятор — альдостерон, ингибитор — ПгE2.
Ú Тиазидные (мишень — Na,Cl‑котранспортёр дистальных извитых канальцев), стимулятор — альдостерон.
Ú Амилорид, триамтерен, спиронолактон (мишень — Na‑каналы собирательных трубочек), стимулятор — альдостерон.
Ú Амилорид (мишень — управляемые цГМФ катионные каналы), стимулятор — альдостерон, ингибитор — натриуретический пептид (атриопептин).
Ú Осмотические (например, маннитол). Мишени — аквапорины разных отделов почечных канальцев, стимулятор — вазопрессин.
· Аквапорины (AQP) — семейство мембранных пор для воды (рис. 26–10). Идентифицировано 10 аквапоринов. AQP3, AQP7 и AQP9 дополнительно проницаемы для глицерола и других небольших молекул, а AQP0, AQP1, AQP2, AQP4, AQP5 — только для воды. AQP1 появляется в эритроцитах после рождения практически одномоментно с формированием способности почки концентрировать мочу (вероятно, AQP1 способствует регидратации эритроцитов, обезвоженных в гипертонической среде капилляров мозговой части почки). Экспрессия AQP1 происходит в почке (проксимальные извитые канальцы и тонкий отдел петли Хенле) плода, начиная со второго триместра беременности. Полной экспрессии этот водный канал достигает после рождения, что связывают со способностью почки концентрировать мочу. AQP2 экспрессируется только в собирательных трубочках почки. Активность этого канала регулирует вазопрессин (АДГ), увеличивая реабсорбцию воды из просвета трубочек в межклеточное пространство. AQP3 — водный канал базолатеральных мембран собирательных трубочек почки. AQP4 экспрессируется в клетках эпендимной выстилки сосудистого сплетения желудочков и водопровода мозга, в синтезирующих вазопрессин нейросекреторных нейронах гипоталамуса. AQP4 расценивают как осморецептор.
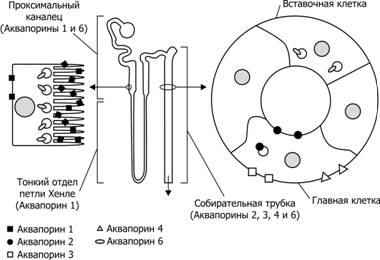
Рис. 26–10. Аквапорины в почке [11]. Аквапорин 1 (AQP1) экспрессируется в апикальной и базолатеральной мембране клеток проксимального канальца нефрона и нисходящей тонкой части петли Хенле, формируя каналы с высокой проницаемостью для воды. AQP2 главных клеток собирательных трубочек сосредоточен внутри везикул и транспортируется в апикальную мембрану в присутствии вазопрессина. AQP3 и AQP4 расположены в базолатеральной мембране главных клеток собирательных трубочек AQP6 содержится во внутриклеточных везикулах клеток проксимального канальца и во вставочных клетках собирательных трубочек.
K+
Почки ежесуточно отфильтровывают 800 мМ K+, хотя с пищей поступает около 100 мМ, а экскретируется с мочой примерно 90 мМ. Происходит также секреция K+. Таким образом, поддержание калиевого баланса организма происходит при сочетании фильтрации, реабсорбции и секреции. В проксимальном отделе нефрона происходит массовая реабсорбция K+ (80%), а в дистальных — в зависимости от поступления калия в организм — этот катион либо реабсорбируется, либо экскретируется.
Реабсорбция калия происходит во всех отделах почечных канальцев, в том числе в проксимальных канальцах (80%), петле Хенле (10%) и в более дистальных канальцах (10%).
· При низком содержании калия в диете все почечные канальцы реабсорбируют K+, при этом в экскретируемой моче остаётся не более 3% от отфильтрованного калия. Однако, при длительной недостаточности калия в диете возможно развитие опасной гипокалиемии.
· При нормальном или повышенном содержании калия в диете к реабсорбции присоединяется регулируемая секреция калия, происходящая в собирательных трубочках и протоках.
· Механизмы транспорта K+
Ú Проксимальный отдел нефрона и тонкое восходящее колено петли Хенле: реабсорбция происходит в основном по околоклеточному пути пассивной диффузией.
Ú Толстое восходящее колено петли Хенле. Часть калия реабсорбируется пассивно по околоклеточному пути, так как базолатеральная мембрана проницаема и для K+ и для Cl–. Примерно половина K+ входит в клетку активно — при помощи расположенного апикально Na/K/Cl–котранспортёра (вторичный активный транспорт) — мишени петлевых диуретиков (фуросемид, буметанид), блокирующих транспорт калия.
Ú Собирательные трубочки корковой части. Главные клетки секретируют K+, а вставочные клетки реабсорбируют этот катион (H+,K+–насос в апикальной части клеток, K+‑канал в базальной части).
Ú Собирательные протоки мозговой части реабсорбируют K+ пассивно.
· Регуляция секреции K+. Увеличивают секрецию калия диуретики, низкая[CI–] в просвете канальцев, альдостерон.
Мочевина
Мочевина — конечный продукт катаболизма аминокислот — образуется в печени из NH4+, её концентрация в крови (азот мочевины) — 2,5–8,32 ммоль/л. Все 100% мочевины фильтруется в почках, экскретируется с мочой около 40% отфильтрованной мочевины (ежесуточно 20–35 г). В почках мочевина и реабсорбируется (проксимальный отдел нефрона и собирательные протоки), и секретируется (тонкая часть петли Хенле), в итоге почку покидает венозная кровь, содержащая 5% от поступившей в почки мочевины (рис. 26–11).
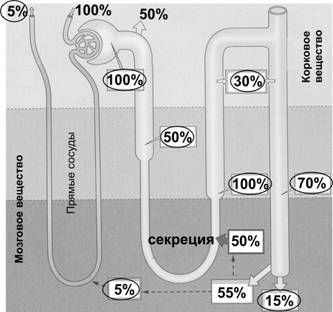
Рис. 26–11. Транспорт мочевины между канальцами, интерстицием и кровеносными сосудами [2]. Значения в овалах — содержание (в %) от отфильтрованного (100%).
· Проксимальный отдел нефрона. Мочевина реабсорбируется простой диффузией по околоклеточному (частично трансклеточному) пути.
· Тонкая часть петли Хенле. Здесь при помощи облегчённой диффузии происходит секреция мочевины (транспортёр UT2).
· Дистальные канальцы нефрона и собирательные трубочки реабсорбируют мочевину по механизму облегчённой диффузии: транспортёр UT1 переносит мочевину в клетку, транспортёр UT4 выводит мочевину из клетки. Аргинин вазопрессин (АДГ) стимулирует активность UT1, но не UT4.
Глюкоза
Концентрация глюкозы в плазме крови натощак — 4–5,5 мМ (3,58–6,05 ммоль/л, 85–115 мг%). В почках глюкоза отфильтровывается полностью и практически полностью и активно (против концентрационного градиента) реабсорбируется в начальных отделах проксимального отдела нефронов. Секреции глюкозы нет, поэтому с мочой экскретируются следовые количества этого сахара. Глюкоза поступает в эпителий канальцев посредством активного сочетанного транспорта с Na+ (электрогенныеконтранспортёрыSGLT), а покидает клетки облегчённой диффузией через Na+–независимые транспортёры GLUT.
Порог экскреции глюкозы с мочой — 250 мг% (~14 мМ). При дальнейшем увеличении концентрации глюкозы в плазме крови экскреция линейно возрастает. Поскольку порог экскреции значительно выше нормальной концентрации глюкозы (~5,5 мМ), и организм тщательно поддерживает этот параметр, здоровые лица не экскретируют глюкозу с мочой. Даже при сахарном диабете глюкозурия не появляется до превышений порога экскреции.
Аминокислоты. Концентрация L-аминокислот в крови около 2,4 мМ. Это преимущественно всосавшиеся в ЖКТ аминокислоты. В почках отфильтровываются все аминокислоты, 98% — всасывается в проксимальных извитых канальцах по трансклеточному пути при помощи различных Na+–зависимых котранспортёров и Na+-независимой облегчённой диффузии, выход аминокислот в межклеточное пространство происходит по механизму облегчённой диффузии.
Дата добавления: 2016-06-05; просмотров: 3381;











