Как возникают э. д. с. и ток в гальваническом элементе?
 Один из электродов гальванического элемента (обычно цинковый) постепенно изнашивается (растворяется), если элемент дает в течение длительного времени электрический ток. Поэтому можно предполагать, что возникновение э. д, с. гальванического элемента стоит в связи с процессом растворения металла. Действительно, исследование обнаруживает, что при погружении металла в разведенную кислоту начинается процесс его растворения. При этом, однако, в раствор переходят не нейтральные атомы металла, а его положительные ионы, избыточные же электроны остаются в металле и заряжают его отрицательно (рис. 118). Однако этот процесс растворения очень скоро приостанавливается, ибо по мере увеличения концентрации ионов в растворе начинает все большую роль играть обратный процесс: ионы, окружающие электрод, в своем тепловом движении налетают на электрод и выделяются на нем, нейтрализуясь избыточными электронами, остающимися в металле. Вскоре устанавливается равновесие: число ионов, переходящих в раствор за некоторое время, становится равным числу ионов, осаждающихся из раствора за то же время. Этому равновесному состоянию соответствует определенная разность потенциалов между металлом и раствором, характерная для природы металла и растворителя. Возникающая разность потенциалов, конечно, не зависит от размеров погруженной части металла, ибо указанное равновесие устанавливается у каждого участка поверхности, соприкасающегося с раствором.
Один из электродов гальванического элемента (обычно цинковый) постепенно изнашивается (растворяется), если элемент дает в течение длительного времени электрический ток. Поэтому можно предполагать, что возникновение э. д, с. гальванического элемента стоит в связи с процессом растворения металла. Действительно, исследование обнаруживает, что при погружении металла в разведенную кислоту начинается процесс его растворения. При этом, однако, в раствор переходят не нейтральные атомы металла, а его положительные ионы, избыточные же электроны остаются в металле и заряжают его отрицательно (рис. 118). Однако этот процесс растворения очень скоро приостанавливается, ибо по мере увеличения концентрации ионов в растворе начинает все большую роль играть обратный процесс: ионы, окружающие электрод, в своем тепловом движении налетают на электрод и выделяются на нем, нейтрализуясь избыточными электронами, остающимися в металле. Вскоре устанавливается равновесие: число ионов, переходящих в раствор за некоторое время, становится равным числу ионов, осаждающихся из раствора за то же время. Этому равновесному состоянию соответствует определенная разность потенциалов между металлом и раствором, характерная для природы металла и растворителя. Возникающая разность потенциалов, конечно, не зависит от размеров погруженной части металла, ибо указанное равновесие устанавливается у каждого участка поверхности, соприкасающегося с раствором.
Заметим, что при соприкосновении с электролитами большинство металлов заряжается отрицательно. В элементе Вольты, например, и медь и цинк переходят в раствор в виде положительных ионов и оба электрода заряжаются отрицательно. Но избыток отрицательного заряда и соответственно разность потенциалов между кислотой и медью меньше, чем между кислотой и цинком. Поэтому для того чтобы использовать образовавшуюся разность потенциалов между металлом и растворителем, мы должны погрузить в растворитель еще один электрод из другого материала.
 Действительно, если в серную кислоту погрузить два цинковых электрода, то потенциал каждого из них будет на одну и ту же величину ниже потенциала раствора, а следовательно, между обоими цинковыми электродами разность потенциалов окажется равной нулю и прибор не будет действовать в качестве гальванического элемента. Но если второй электрод сделан из другого материала, то разность потенциалов между ним и раствором будет иной, чем для первого из электродов. Следовательно, между двумя различными электродами обнаруживается разность потенциалов, зависящая как от природы растворителя, так и от природы обоих электродов.
Действительно, если в серную кислоту погрузить два цинковых электрода, то потенциал каждого из них будет на одну и ту же величину ниже потенциала раствора, а следовательно, между обоими цинковыми электродами разность потенциалов окажется равной нулю и прибор не будет действовать в качестве гальванического элемента. Но если второй электрод сделан из другого материала, то разность потенциалов между ним и раствором будет иной, чем для первого из электродов. Следовательно, между двумя различными электродами обнаруживается разность потенциалов, зависящая как от природы растворителя, так и от природы обоих электродов.
Поляризация электродов. При замыкании элемента Вольты на внешнюю цепь, содержащую амперметр, легко заметить, что показания амперметра не остаются постоянными, а непрерывно делаются все меньше и меньше. Через несколько минут после замыкания сила тока падает в несколько раз. Таким образом, элемент Вольты оказывается непригодным для получения постоянного тока. В чем же заключается причина уменьшения тока?
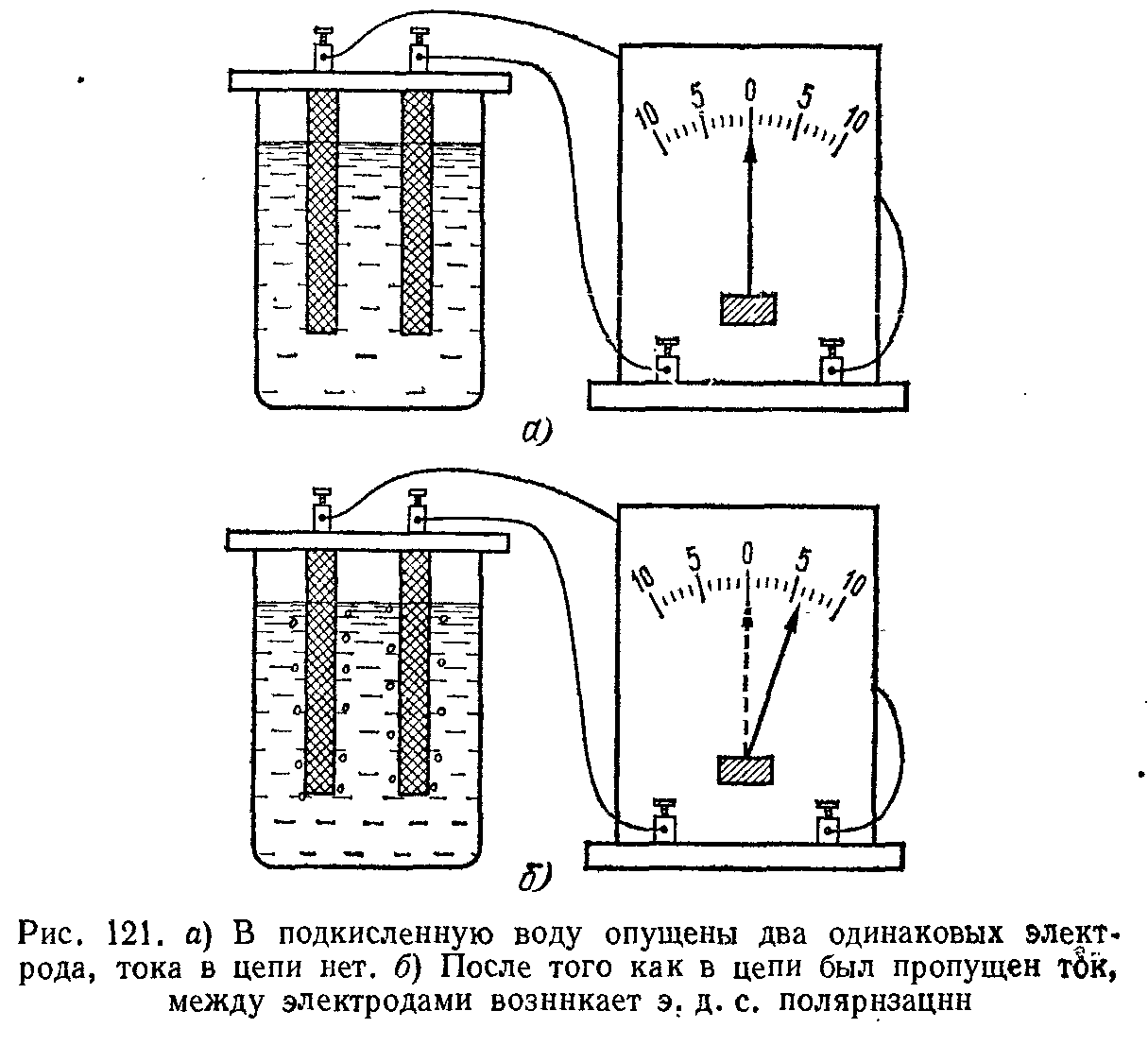
Ответ на этот вопрос мы находим в следующем опыте. Опустим в подкисленную воду два одинаковых электрода, например платиновых или угольных (рис. 121, а), и при соединим их к амперметру. Амперметр не покажет никакого тока, что и неудивительно, так как мы уже знаем, что между двумя одинаковыми электродами (уголь - уголь) даже в растворе электролита не возникает разности потенциалов. Отсоединим теперь эти угольные электроды от амперметра и подключим их к гальваническому элементу или какому-нибудь иному генератору тока. Сразу же начнется электролиз серной кислоты, и на одном из электродов будет выделяться водород, а на другом — кислород, получающийся при вторичной реакции между выделяющимися группами S04 и водой:
2S04 + 2Н20 - 2H2S04 + О2.
Если отключить электроды от элемента, то они остаются покрытыми пузырьками соответствующих газов.
Присоединим теперь электроды снова к амперметру (рис. 121,6). В этом случае в цепи появляется заметный ток, текущий от «кислородного» электрода к «водородному» «водородный» электрод играет роль отрицательного полюса. Возникший ток, однако, быстро ослабевает; одновременно с этим исчезает и газ на электродах, и когда пропадают последние следы газа, то прекращается и ток.
Объяснение этого опыта заключается в том, что после электролиза оба электрода делаются неодинаковыми: один из них покрывается слоем кислорода, а другой — водорода. Поэтому и потенциалы обоих электродов относительно раствора тоже становятся различными, и между ними возникает разность потенциалов, так что угольные электроды делаются подобными полюсам гальванического элемента. По этой причине описанное явление получило название поляризации, а возникающая при этом э. д. с.— э. д. с. поляризации.
Теперь нетрудно понять, почему элемент Вольты обладает плохими качествами. Мы знаем, что внутри элемента также течет ток, причем положительные ионы, в частности ионы водорода, перемещаются от отрицательного полюса (цинка) к положительному (меди). Поэтому на положительном полюсе выделяется водород и возникает дополнительная э. д. с. поляризации, стремящаяся вызвать ток противоположного направления. Появление э. д. с. поляризации и есть основная причина ослабления тока.
Отметим, что выделение газов на электродах нежелательно еще и по другой причине. Газы, выделившиеся на электродах, не проводят электричества. Поэтому появление на электродах пузырьков ;газа уменьшает поверхность соприкосновения металла и электролита и, следовательно, увеличивает внутреннее сопротивление элемента и этим также способствует ослаблению тока.
Из сказанного следует, что поляризация в гальванических элементах весьма нежелательна. Поэтому при конструировании гальванических элементов всегда стараются создать деполяризацию, т. е. такие процессы, которые, по возможности, устранили бы поляризацию.
Деполяризация в гальванических элементах. Основным материалом, для отрицательных электродов в современных элементах является цинк. При этом электролит подбирают таким образом, чтобы переходящие в раствор положительные ионы цинка, соединяясь с имеющимися там отрицательными ионами электролита, давали с последними растворимое соединение без выделения газа. Так, например, если электролитом является раствор H2S04, то при растворении цинка образуется растворимая соль ZnS04. Таким образом, задача деполяризации сводится только к устранению водорода на положительном электроде.
В настоящее время применяют исключительно химическую деполяризацию. Ее сущность заключается в том, что в элемент вводят какой-либо сильный окислитель, который вступает в химическую реакцию с водородом, выделяющимся у положительного электрода, и этим предотвращает его выделение в газообразном состоянии.
Вопросы к тексту:
1. Какие вещества называются электролитами?
2. Какой процесс называется электролизом?
3. Что такое элементарный электрический заряд?
4. Чему равен элементарный электрический заряд?
5. Запишите первый закон Фарадея.
6. Дайте определение химического эквивалента вещества.
7. По какой формуле находится химический эквивалент вещества?
8. Что показывает химический эквивалент вещества?
9. Запишите второй закон Фарадея.
10. Чему равна постоянная Фарадея?
11. Какие частицы называются ионами?
12. Что представляет собой ток в электролитах?
13. Что такое электролитическая диссоциация?
14. Почему не все растворы проводят электрический ток?
15. Для градуировки каких амперметров используется электролитический способ?
16. С именами каких ученых связано открытие гальванического элемента? Какой вклад внес каждый из них?
17. Какое явление было использовано для построения гальванического элемента?
18. Сформулируйте правило Вольта
19. Что происходило бы ,если бы правило Вольта не соблюдалось?
20. Объясните, почему в замкнутой цепи, состоящей из проводников 1-го класса не идет электрический ток?
21. Что называют элементом Вольта?
22. Какие проводники является проводниками 1 класса?
23. Какие проводники являются проводниками 2 класса?
24. Какие элементы содержит любой гальванический элемент?
25. Какой процесс называется равновесием?
26. Почему при соприкосновении с электролитами все металлы заряжаются отрицательно?
27. Объясните, почему элемент Вольта обладает плохими качествами?
28. Почему поляризация в гальванических элементах является негативным фактором?
29. Зачем нужна деполяризация в гальванических элементах?
Прикладная физика
Аккумуляторы.Явление поляризации, вредное в гальванических элементах, находит, однако, и полезное применение. В 1895 г. Планте показал, что э. д. с. поляризации можно, использовать для практического получения электрического тока. Он построил элемент с двумя свинцовыми электродами, погруженными в раствор серной кислоты. Элемент в таком виде не обладает еще э. д. с, так как оба его электрода одинаковы. Если, однако, через такой элемент пропускать известное время ток, то на его электродах выделяются продукты электролиза, которые вступают в химическую реакцию с электродами. Благодаря этому электроды оказываются различными по химическому составу, и появляется определенная э. д. с.— именно, э. д. с. поляризации, равная приблизительно 2 В. Элемент в таком состоянии является уже сам источником тока и при замыкании на какую-либо цепь может создавать в ней в течение некоторого времени электрический ток. Таким образом, для появления э. д. с. в элементе Планте через него необходимо пропускать в течение известного времени ток от постороннего источника. Этот процесс называется зарядкой элемента.
 Элемент Планте и ему подобные, использующие явление поляризации, называются вторичными элементами или аккумуляторами, так как в них можно запасать (аккумулировать) энергию. После израсходования энергии аккумулятора его можно вновь зарядить пропусканием тока и повторять этот процесс много раз.
Элемент Планте и ему подобные, использующие явление поляризации, называются вторичными элементами или аккумуляторами, так как в них можно запасать (аккумулировать) энергию. После израсходования энергии аккумулятора его можно вновь зарядить пропусканием тока и повторять этот процесс много раз.
Устройство современного свинцового аккумулятора показано на рис. 124.
Он состоит из ряда положительных и отрицательных пластин, находящихся в банке с водным раствором (15—20%) серной кислоты. Все положительные пластины соединены между собой, так же как и все отрицательные, благодаря чему в небольшом сосуде можно иметь большую площадь электродов, разделенных тонким слоем электролита, т. е. иметь элемент с чрезвычайно малым внутренним сопротивлением.
Отрицательные пластины состоят из чистого металлического свинца, поверхность которого сделана мелкопористой для увеличения действующей площади электродов (губчатый свинец). Положительные пластины имеют более сложное строение, показанное на рис. 125. При их изготовлении сначала отливают (или штампуют) раму из свинца, снабженную многими ячейками наподобие пчелиных сотов, и в них впрессовывают специальную массу, состоящую из окислов свинца и связующих веществ. Различные аккумуляторы характеризуются максимальным количеством электричества, которое можно получить от них без новой зарядки. Это количество электричества принято выражать в ампер-часах (А-ч) и называть емкостью аккумулятора. Так, например, переносные аккумуляторы, применяющиеся для автомобилей, имеют обычно емкость 40 А-ч. Это значит, что они могут давать ток 1 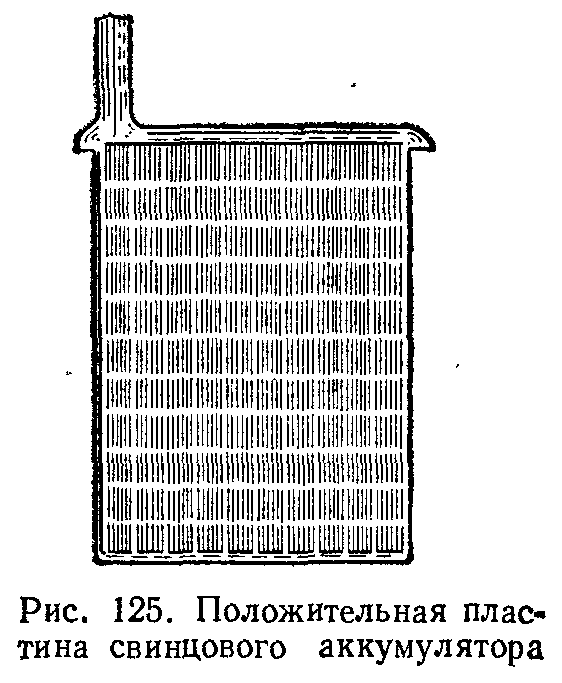 А в течение 40 ч или ток 2 А в течение 20 ч и т. д. При этом, конечно, разрядный ток не должен превышать некоторой максимальной силы (для свинцового аккумулятора приблизительно 1 А на каждый квадратный дециметр поверхности положительных пластин), так как в противном случае пластины быстро разрушаются. Чем больше площадь пластин аккумулятора, тем больше продуктов электролиза может быть удержано на пластинах, а значит, и тем больший заряд можно получить от аккумулятора при разрядке, т. е. тем больше его емкость. Аккумуляторы играют в современной электротехнике важную роль. Так, например, на электрических станциях с неравномерной нагрузкой часто устанавливают, кроме генераторов постоянного тока, еще и батареи аккумуляторов (буферные аккумуляторы). При малой нагрузке станции часть энергии, вырабатываемой генераторами, расходуется на зарядку аккумуляторов, а в периоды большой нагрузки эти аккумуляторы питают сеть параллельно с генераторами. Электростанции, использующие энергию ветра, всегда бывают снабжены аккумуляторами, которые заряжаются в те периоды, когда имеется ветер, а затем уже расходуют запасенную энергию по мере надобности и независимо от метеорологических условий.
А в течение 40 ч или ток 2 А в течение 20 ч и т. д. При этом, конечно, разрядный ток не должен превышать некоторой максимальной силы (для свинцового аккумулятора приблизительно 1 А на каждый квадратный дециметр поверхности положительных пластин), так как в противном случае пластины быстро разрушаются. Чем больше площадь пластин аккумулятора, тем больше продуктов электролиза может быть удержано на пластинах, а значит, и тем больший заряд можно получить от аккумулятора при разрядке, т. е. тем больше его емкость. Аккумуляторы играют в современной электротехнике важную роль. Так, например, на электрических станциях с неравномерной нагрузкой часто устанавливают, кроме генераторов постоянного тока, еще и батареи аккумуляторов (буферные аккумуляторы). При малой нагрузке станции часть энергии, вырабатываемой генераторами, расходуется на зарядку аккумуляторов, а в периоды большой нагрузки эти аккумуляторы питают сеть параллельно с генераторами. Электростанции, использующие энергию ветра, всегда бывают снабжены аккумуляторами, которые заряжаются в те периоды, когда имеется ветер, а затем уже расходуют запасенную энергию по мере надобности и независимо от метеорологических условий.
Аккумуляторы широко применяют на всех подводных судах (кроме подводных судов с атомным двигателем). При надводном плавании аккумуляторы заряжаются от генератора постоянного тока, а при погружении под воду все механизмы приводятся в движение исключительно от аккумуляторов. Аккумуляторы с успехом применяются в электрических грузовых тележках, так называемых электрокарах, которые должны работать короткие промежутки времени и делать частые остановки и на которых поэтому невыгодна установка двигателей внутреннего сгорания, непрерывно поглощающих топливо; в автомобилях (зажигание в моторах, освещение); для питания рудничных ламп и еще во многих важных промышленных машинах и приборах. Очень широко распространены аккумуляторы в лабораторной практике, где они являются хорошими источниками постоянного тока, а также в радиотехнике.
Несмотря на большие преимущества аккумуляторов, которые во многих случаях вытеснили гальванические элементы, последние все еще имеют ряд важных применений: в качестве эталонов напряжения (нормальные элементы), для питания радиоприемников, карманных фонарей, микрокалькуляторов и т. п.
Закон Омадля замкнутой цепи.Закон Ома для участка цепи, позволяет вычислить ток, если известно сопротивление участка и напряжение на его концах. Очень часто, однако, приходится решать задачи, в. которых напряжение на концах участка цепи не задано, но зато известны сопротивления всех частей цепи и э. д. с. источника, питающего цепь. Как найти в этом случае силу тока?
Рассмотрим всю замкнутую электрическую цепь, включая и источник тока, и выясним на опыте, от чего зависит ток в этой цепи. Замкнем источник тока, например элемент Даниеля, на внешнюю цепь, содержащую амперметр и реостат, и будем перемещать движок реостата, меняя тем самым сопротивление внешней цепи. Мы обнаружим, что с уменьшением сопротивления внешней цепи ток будет увеличиваться.
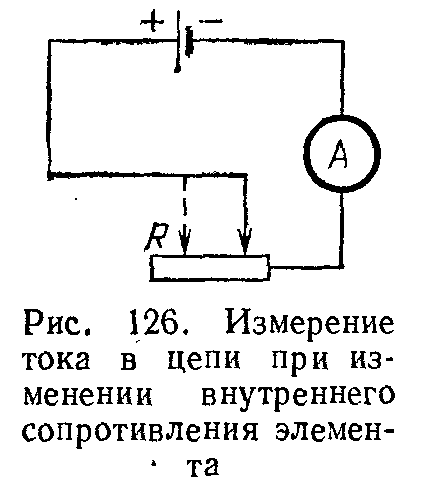 Установим теперь реостат так, чтобы сопротивление внешней цепи было незначительным, и будем изменять глубину погружения цинковой пластины элемента. Ток будет увеличиваться по мере погружения пластины.
Установим теперь реостат так, чтобы сопротивление внешней цепи было незначительным, и будем изменять глубину погружения цинковой пластины элемента. Ток будет увеличиваться по мере погружения пластины.
Для понимания этого результата вспомним, что напряжение на разомкнутом элементе, т. е. его э. д. с, совершенно не зависит от геометрических размеров и формы элемента. Следовательно, при изменении глубины погружения пластины э. д. с. источника не меняется. В чем же причина изменения тока?
Ток идет как по внешней цепи, так и внутри источника. Но сам источник представляет тоже определенное сопротивление току. Это сопротивление носит название внутреннего сопротивления источника. В гальванических элементах оно слагается из сопротивления его электродов и главным образом из сопротивления столба электролита между ними. Погружая цинковую пластину на различную глубину, мы изменяем сечение этого столба и вместе с ним внутреннее сопротивление элемента. Мы видим, что сила тока зависит также от внутреннего сопротивления источника тока.
Полную цепь можно рассматривать как последовательное соединение сопротивления внешней цепи и внутреннего сопротивления источника тока. Полное сопротивление цепи представляет собой сумму внутреннего сопротивления источника и сопротивления внешней цепи. Заменим элемент каким-либо другим, имеющим такое же внутреннее сопротивление, но другую э. д. с. Мы обнаружим, что ток при этом изменится.
Таким образом, ток в цепи зависит от э. д. с. источника и от полного сопротивления цепи.
Количественный закон, связывающий эти величины, представляет закон Ома для замкнутой цепи: ток в цепи, содержащей источник тока, прямо пропорционален э. д. с. источника и обратно пропорционален полному сопротивлению цепи.
Если обозначить э. д. с. источника через E, его внутреннее сопротивление через r, сопротивление внешней цепи через R, а ток через I, то закон Ома представится следующей формулой:
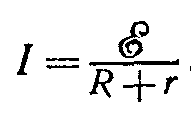
Мы видим, что ток, который способен дать источник, зависит не только от э. д. с. источника и сопротивления внешней цепи, но еще и от внутреннего сопротивления. Сказанное относится, конечно, не только к гальваническим элементам, но и к любым источникам тока, например к аккумуляторам или генераторам постоянного тока.
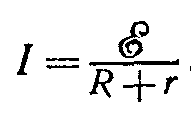 Напряжение на зажимах источника тока и э, д. с. Измерения показывают, что напряжение на зажимах источника тока, замкнутого на внешнюю цепь, зависит от силы отбираемого тока (от «нагрузки») и изменяется с изменением последнего. Пользуясь законом Ома, мы можем сейчас разобрать этот вопрос точнее. Из формулы: получаем
Напряжение на зажимах источника тока и э, д. с. Измерения показывают, что напряжение на зажимах источника тока, замкнутого на внешнюю цепь, зависит от силы отбираемого тока (от «нагрузки») и изменяется с изменением последнего. Пользуясь законом Ома, мы можем сейчас разобрать этот вопрос точнее. Из формулы: получаем 
где R — сопротивление внешней цепи, а г — внутреннее сопротивление источника. Но к внешней цепи мы вправе применить закон Ома для участка цепи:
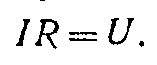
 Здесь U — напряжение во внешней цепи, т.е. разность потенциалов на зажимах источника. Оно может быть выражено с учетом этих двух формул, следующей формулой:
Здесь U — напряжение во внешней цепи, т.е. разность потенциалов на зажимах источника. Оно может быть выражено с учетом этих двух формул, следующей формулой:
Видно, что при замкнутой цепи напряжение U на зажимах источника тока всегда меньше э.д.с. Напряжение U зависит от силы тока I и только в предельном случае разомкнутой цепи, когда сила тока I=0, напряжение на зажимах равно э.д.с.
Уменьшение напряжения на зажимах источника при наличии тока I легко наблюдать на опыте. Для этого нужно замкнуть какой-либо гальванический элемент на реостат и подключить к зажимам элемента вольтметр (рис. 127).
 Перемещая движок реостата, можно видеть, что чем меньше сопротивление внешней цепи, т.е. чем больше ток, тем меньше напряжение на зажимах источника. Если сопротивление внешней цепи сделать очень малым по сравнению с внутренним сопротивлением источника («вывести» реостат), т. е. сделать «короткое замыкание», то напряжение на зажимах делается равным нулю.
Перемещая движок реостата, можно видеть, что чем меньше сопротивление внешней цепи, т.е. чем больше ток, тем меньше напряжение на зажимах источника. Если сопротивление внешней цепи сделать очень малым по сравнению с внутренним сопротивлением источника («вывести» реостат), т. е. сделать «короткое замыкание», то напряжение на зажимах делается равным нулю.
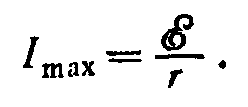 Что же касается тока, то он при коротком замыкании достигает своего максимального значения Imax. Сила этого «тока короткого замыкания» получается из закона, если в нем положить R=0 (т. е. пренебречь сопротивлением R по сравнению с r) :
Что же касается тока, то он при коротком замыкании достигает своего максимального значения Imax. Сила этого «тока короткого замыкания» получается из закона, если в нем положить R=0 (т. е. пренебречь сопротивлением R по сравнению с r) :
Таким образом, ток короткого замыкания зависит не только от э.д.с., но также и от внутреннего сопротивления источника. Поэтому короткое замыкание представляет различную опасность для разных источников тока. Короткие замыкания гальванического элемента сравнительно безвредны, так как при небольшой э. д. с. элементов их внутреннее сопротивление велико, и поэтому токи короткого замыкания малы. Такие токи не могут вызвать серьезные разрушения, и поэтому к изоляции проводов в целях, питаемых элементами (звонки, телефоны и т. п.), не предъявляют особо высоких требований. Иное дело силовые или осветительные цепи, питаемые мощными генераторами. При значительной э. д. с. (100 и более вольт) внутреннее сопротивление этих источников ничтожно мало, и поэтому ток короткого замыкания может достигнуть огромной силы. В этом случае короткое замыкание может привести к расплавлению проводов, вызвать пожар и т. д. Поэтому к устройству и изоляции таких цепей предъявляют строгие технические требования, которые ни в коем случае нельзя нарушать без риска вызвать опасные последствия. Такие цепи всегда снабжаются предохранителями и притом нередко в различных местах: общий предохранитель (при главном вводе), групповые и штепсельные предохранители.
Соединение источников тока.Очень часто источники тока соединяют между собой для совместного питания цепи. Составим цепь гальванических элементов так, чтобы положительный полюс каждого предыдущего элемента соединялся с отрицательным полюсом последующего (рис. 130).

Если цепь составлена, например, из элементов Вольты, то медный электрод каждого элемента имеет потенциал на 1,1В выше, чем цинковый электрод того же элемента. Медный и цинковый электроды двух соседних элементов соединены проводником и, следовательно, имеют одинаковый потенциал. Поэтому разность потенциалов между медью второго элемента и цинком первого будет уже 1,1 + 1,1=2,2 В,
При последовательном соединении проводников их сопротивления складываются. Поэтому и внутреннее сопротивление батареи из последовательно соединенных источников равно сумме внутренних сопротивлений отдельных источников.
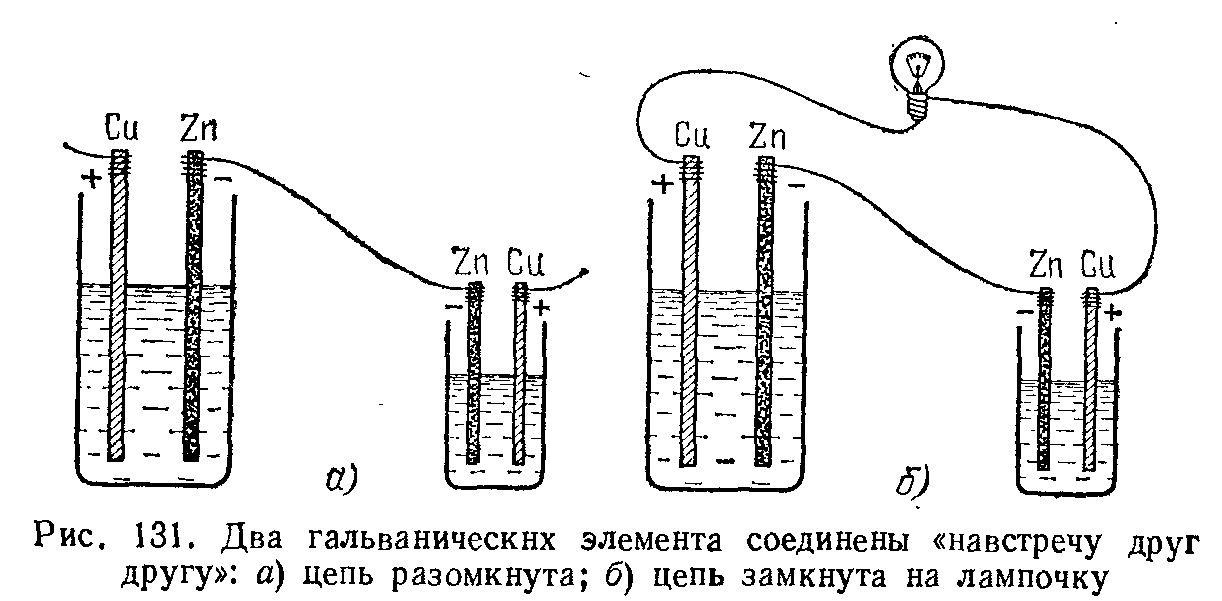 Наоборот, соединяя одноименные полюсы двух элементов одинакового типа (включение «навстречу друг другу», рис. 131, а), мы не получаем, между крайними полюсами ни напряжение гальванических элементов совершенно не зависит от их размеров; оно определяется только материалом пластин и применяемой жидкостью.
Наоборот, соединяя одноименные полюсы двух элементов одинакового типа (включение «навстречу друг другу», рис. 131, а), мы не получаем, между крайними полюсами ни напряжение гальванических элементов совершенно не зависит от их размеров; оно определяется только материалом пластин и применяемой жидкостью.
Если мы соединим проводником два свободных одноименных полюса элементов, соединенных «навстречу друг другу» (рис. 131, б), то в образовавшейся замкнутой цепи тока не будет, если э. д. с. обоих элементов равны, так как в этом случае результирующая э. д. с, равная разности обеих э. д. с. отдельных элементов, равна нулю. Если же э. д. с. этих.элементов различны, то результирующая э. д. с. не равна нулю, и в цепи будет идти ток. Источником этого тока будет элемент с большей э. д. с, а элемент с меньшей э. д. с. будет представлять собой для него просто нагрузку (электролитическую ванну).
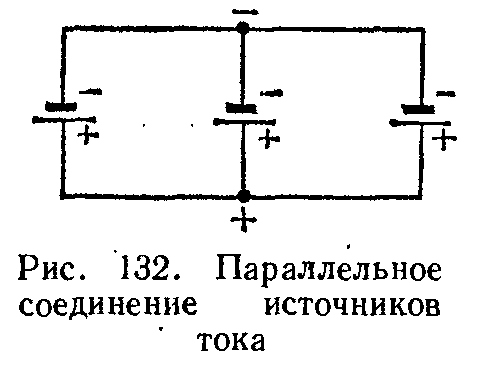 Соединим теперь между собой все положительные и все отрицательные полюсы двух или нескольких элементов или иных источников тока и присоединим внешнюю цепь (нагрузку) к общим зажимам составленной таким образом батареи элементов (рис. 132). Такое соединение источников тока для совместного питания одной и той же цепи называют параллельным.
Соединим теперь между собой все положительные и все отрицательные полюсы двух или нескольких элементов или иных источников тока и присоединим внешнюю цепь (нагрузку) к общим зажимам составленной таким образом батареи элементов (рис. 132). Такое соединение источников тока для совместного питания одной и той же цепи называют параллельным.
Если все параллельно соединенные элементы имеют одинаковые э. д. с, то такова же будет и э. д. с. всей батареи. Если же эти элементы имеют различные э. д. с, то э. д. с. батареи равна наибольшей из э. д. с. параллельно соединенных элементов.
Между этими двумя случаями есть, однако, существенное различие. Если э. д. с. всех элементов одинаковы, то при разомкнутой внешней цепи ток через цепь, состоящую только из элементов, идти не будет, и ни один из этих элементов не будет расходоваться. Если же э. д. с. их различны, то и при разомкнутой внешней цепи более сильные элементы, будут посылать ток через более слабые и изнашиваться. При работе такой батареи на внешнюю цепь также часть тока от более сильных элементов будет ответвляться и идти через более слабые. Это невыгодно, и потому на практике всегда соединяют параллельно только элементы с одинаковой э. д. с.
Сопротивление параллельно соединяемых элементов может быть одинаковым или различным. Общее сопротивление батареи, которое мы можем вычислить по формуле для определения параллельно соединенных сопротивлений, всегда меньше, чем сопротивление каждого из элементов в отдельности. В частности, внутреннее сопротивление батареи из п элементов с одинаковым внутренним сопротивлением в п раз меньше, чем сопротивление отдельного элемента.
Идеальный газ
Реальный газ — достаточно сложная система. Простейшая физическая модель реального газа — идеальный газ.
Под моделью в физике понимают не увеличенную или уменьшенную копию реального объекта. Физическая модель — это упрощенная схематическая копия исследуемой реальной системы. Модель должна отражать наиболее существенные, наиболее характерные свойства системы. В модели газа принимаются во внимание лишь те основные свойства молекул, учет которых необходим для объяснения закономерностей поведения реального газа в определенных интервалах давления и температуры.
В молекулярно-кинетической теории идеальным газом называют газ, состоящий из молекул, взаимодействие между которыми пренебрежимо мало.Иными словами, предполагается, что средняя кинетическая энергия молекул идеального газа во много раз больше потенциальной энергии их взаимодействия. Именно данная модель реального газа приводит к уравнению состояния (3.9.9). Поэтому термодинамическое определение идеального газа как газа, подчиняющегося уравнению состояния Менделеева—Клапейрона, находится в полном соответствии с приведенным выше молекулярно-кинетическим определением идеального газа.
Реальные газы ведут себя подобно идеальному газу при достаточно больших разрежениях, т. е. когда среднее расстояние между молекулами во много раз больше их размеров.В этом случае силами притяжения между молекулами можно пренебречь. Силы их отталкивания проявляются в течение ничтожно малых промежутков времени при столкновениях молекул друг с другом.
Дата добавления: 2017-05-02; просмотров: 3995;











