Типы кристаллических решеток
Наименьший объем кристаллической решетки, который характеризует расположение атомов в кристалле, называют элементарной кристаллической ячейкой (рис. 4). Перемещая элементарную кристаллическую ячейку вдоль трех пространственных осей, можно получить кристалл любой величины, так же как из одинаковых кирпичиков строятся разные по величине и архитектуре здания.
 |
Рис. 4. Элементарная кристаллическая ячейка:
пространственное изображение (а) и схема (б)
По форме элементарных ячеек все кристаллические материалы подразделяются на 7 кристаллических систем. Любую из них можно охарактеризовать шестью параметрами: тремя линейными (размерами a, b и c ячейки по трем осям координат) и тремя угловыми (углами a, b и g между этими отрезками).
Межатомные расстояния измеряются в нанометрах (нм) или ангстремах (Å). 1 нм = 10-9 м; 1 нм = 10 Å. Размеры элементарных ячеек металлов составляют от 2 до 6 Å, или от 0,2 до 0,6 нм.
У металлов чаще всего встречаются три типа кристаллических решеток из 14 возможных:
Кубическая система Гексагональная система
a = b = c, a = b = g = 90° а = b ¹ с, a = b = 90°, g = 120°

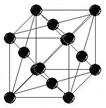
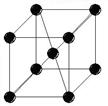
1) объемно-центрированная 2) гранецентрированная 3) гексагональная
кубическая решетка (ОЦК) кубическая решетка (ГЦК) плотноупакованная
решетка (ГПУ)
Такие решетки имеют следующие металлы:
Cr, Mo, W, V, Ta, Nb, Fea Cu, Ni, Ag, Au, Pb, Pt, Mg, Co, Zn, Cd, Be,
Al, Feg Zr, Tia
На изображении ГПУ решетки показаны три соседних элементарных ячейки, чтобы было понятно, почему эта решетка называется гексагональной. Одна из ячеек выделена жирными линиями и штриховкой.
 |
Гексагональная решетка является плотноупакованной только в случае, когда отношение c/a = 1,633, или близко к этому значению. Для такой плотной укладки атомов в решетке центры атомов второго слоя должны располагаться над центрами лунок между атомами первого слоя и т. д. (рис. 5).
Рис. 5. Плотная укладка атомов в ГПУ решетке
Плотность упаковки
Плотность упаковки элементарных частиц в кристалле определяется двумя параметрами:
1) координационным числом – числом ближайших соседей, т. е. атомов, равноудаленных от данного. В ОЦК решетке координационное число K8, что легко увидеть на изображении элементарной ячейки; в ГЦК решетке – K12, что очевидно при рассмотрении 8 соседних элементарных ячеек; в ГПУ решетке – тоже K12, а в простой кубической – K6;
2) коэффициентом компактности – отношением объема атомов, приходящихся на одну ячейку, к ее объему:
Vат/Vяч = 0,52 в простой кубической решетке,
Vат/Vяч = 0,68 в ОЦК решетке,
Vат/Vяч = 0,74 в ГЦК решетке и ГПУ решетке.
Обратите внимание на то, что между атомами (ионами) в металле всегда имеются поры: шары не могут заполнить весь объем.
Дата добавления: 2017-02-13; просмотров: 2744;











