Электродные потенциалы и электродвижущие силы
Если металлическую пластинку опустить в воду, то катионы металла на ее поверхности гидратируются полярными молекулами воды и переходят в жидкость. При этом электроны, в избытке остающиеся в металле, разряжают его поверхностный слой отрицательно. Возникает электростатическое притяжение между перешедшими в жидкость гидратированными катионами и поверхностью металла. В результате этого в системе устанавливается подвижное равновесие:
Ме + m Н2О 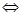 Ме(Н2О) n+m + ne-
Ме(Н2О) n+m + ne-
в растворе на металле
где n - число электронов, принимающих участие в процессе.
На границе металл — жидкость возникает двойной электрический слой, характеризующийся определенным скачком потенциала — электродным потенциалом. Абсолютные значения электродных потенциалов измерить не удается. Электродные потенциалы зависят от ряда факторов (природы металла, концентрации, температуры и др.). Поэтому обычно определяют относительные электродные потенциалы в определенных условиях - так называемые стандартные электродные потенциалы (Е°).
Стандартным электродным потенциалом металла называют его электродный потенциал, возникающий при погружении металла в раствор собственного иона с концентрацией (или активностью), равной 1 моль/л, измеренный по сравнению со стандартным водородным электродом, потенциал которого при 25°С условно принимается равным нулю (Е°=0;∆G0= 0).
Располагая металлы в ряд по мере возрастания их стандартных электродных потенциалов (Е0), получаем ряд стандартных электродных потенциалов (ряд напряжений).
Положение того или иного металла в ряду стандартных электродных потенциалов (ряд напряжений) характеризует его восстановительную способность, а также окислительные свойства его ионов в водных растворах при стандартных условиях. Чем меньше значение Е°, тем большими восстановительными способностями обладает данный металл в виде простого вещества и тем меньшие окислительные способности проявляют его ионы, и наоборот. Электродные потенциалы измеряют приборами, которые называют гальваническими элементами. Окислительно-восстановительная реакция, которая характеризует работу гальванического элемента, протекает в направлении, в котором ЭДС элемента имеет положительное значение. В этом случае ∆G0 < 0, так как ∆G 0= - nFE0.
Пример 1. Стандартный электродный потенциал никеля больше, чем кобальта (табл. 8). Изменится ли это соотношение, если измерить потенциал никеля в растворе его ионов с концентрацией 0,001 моль/л, а потенциалы кобальта — в растворе с концентрацией 0,1 моль/л.
Решение. Электродный потенциал металла (Е) концентрации его ионов в растворе. Эта зависимость уравнением Нернста: 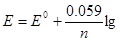 с,
с,
где Е° — стандартный электродный потенциал; и — число электронов, принимающих участие в процессе; с — концентрация (при точных вычислениях — активность) гидратированных ионов металла в растворе, моль/л; Е0 — для никеля и кобальта соответственно равны -0,25 и -0,277 В. Определим электродные потенциалы этих металлов при заданных концентрациях:
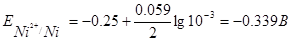

Таким образом, при изменившейся концентрации потенциал кобальта стал больше потенциала никеля.
Пример 2. Магниевую пластинку опустили в раствор его соли. При этом электродный потенциал магния оказался равен -2.41 В. Вычислите концентрацию ионов магния (в моль/л).
Решение. Подобные задачи также решаются на основании уравнения Нернста (см. пример 1): 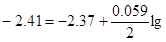 с ; -0,04=0,0295lg c?
с ; -0,04=0,0295lg c?
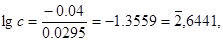
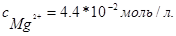
Таблица 8
Стандартные электронные потенциалы(∆Е0) некоторых металлов
| Электрод | Е0, В | Электрод | Е0, В |
| Li+/ Li | -3.045 | Cd2+/Cd | -0.403 |
| Rb+/ Rb | -2.925 | Co2+/Co | -0.277 |
| K+/K | -2.924 | Ni2+/Ni | -0.25 |
| Cs+/Cs | -2.923 | Sn2+/ Sn | -0.136 |
| Ba2+/Ba | -2.90 | Pb2+/Pb | -0.127 |
| Ca2+/Ca | -2.87 | Fe3+/Fe | -0.037 |
| |Na+/Na | -2.714 | 2H+/H2 | -0.000 |
| Mg2+/Mg | -2.37 | Sb3+/Sb | +0.20 |
| Al3+/Al | -1.70 | Bi3+/Вi | +0.215 |
| Ti2+/Ti | -1.603 | Cu2+/Сu | +0.34 |
| Zr4+/Zr | -1.58 | Cu+/Cu | +0.52 |
| Mn4+/Mn | -1.18 | Hg2+2/2Hg | +0.79 |
| V2+/V | -1.18 | Ag+/Ag | + 0.80 |
| Cr2+/Cr | -0.913 | Hg2+/Hg | +0.85 |
| Zn2+/Zn | -0.763 | Pt2+/Pt | +1.19 |
| Cr3+/Cr | -0.74 | Au3+/Au | +1.50 |
| Fe2+/Fe | -0.44 | Au+/Au | +1.70 |
Пример З.Составьте схему- гальванического элемента, в котором электродами являются магниевая и цинковая пластинки, опущенные в растворы их ионов с активной концентрацией 1 моль/л. Какой металл является анодом, какой катодом? Напишите уравнение окислительно-восстановительной реакции, протекающей в этом гальваническом элементе, и вычислите его ЭДС.
Решение. Схема данного гальванического элемента
(-) Mg | Mg2+ || Zn2+ | Zn (+)
Вертикальная линейка обозначает поверхность раздела между металлом и раствором, а две линейки — границу раздела двух жидких фаз — пористую перегородку (или соединительную трубку, заполненную раствором электролита). Магний имеет меньший потенциал (-2,37 В) и является анодом, на котором протекает окислительный процесс:
Mg°-2e- = Mg2+ (1)
Цинк, потенциал которого -0,763 В, — катод, т.е. электрод, на котором протекает восстановительный процесс:
Zn2+ + 2е~ = Zn° (2)
Уравнение окислительно-восстановительной реакции, характеризующее работу данного гальванического элемента, можно получить, сложив электронные уравнения анодного (1) и катодного (2) процессов:
Mg+ Zn2+ = Mg2+ + Zn
Для определения ЭДС гальванического элемента из потенциала катода следует вычесть потенциал анода. Так как концентрация ионов в растворе 1 моль/л, то ЭДС элемента равна разности стандартных потенциалов двух его электродов:

Электролиз
Пример 1.Какая масса меди выделится на катоде при электролизе раствора CuSO4 в течение 1 ч. При силе тока 4А? Решение. Согласно законам Фарадея
m = ЭIt/96500, (1)
где т — масса вещества, окисленного или восстановленного на электроде; Э — молярная масса эквивалента вещества; I — сила тока, A; t — продолжительность электролиза, с.
Молярная масса эквивалентов меди в CuSO4 равна 63,54 : 2 = =31,77 г/моль. Подставив в формулу (1) значения Э = 31,77, I = 4 А, t= 60 ∙ 60 = 3600 с, получим
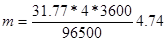
Пример 2.Вычислите молярную массу эквивалента металла, зная, что при электролизе раствора хлорида этого металла затрачено 3880 Кл электричества и на катоде выделяется 11,742 г металла.
Решение. Подставляя в формулу (1) числовые значения, получаем
Э = 11,742 ∙ 96500/3880 = 29,35 г/моль,
где m = 11,742 г; It = Q = 3880 Кл.
Пример 3.Чему равна сила тока при электролизе раствора в течение 1 ч 40 мин 25 с, если на катоде выделилось 1,4 л водорода (н.у.)?
Решение. Из формулы (1)
I = m 96500/Эt
Так как дан объем водорода, то отношение т/Э заменяем отношением VH; /VЭ(Н 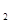 ), где VH
), где VH 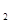 — объем водорода, л.; VЭ(Н
— объем водорода, л.; VЭ(Н 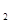 ) объем эквивалентной массы водорода, л. Тогда
) объем эквивалентной массы водорода, л. Тогда
I = VH 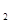 96500/ VЭ(Н
96500/ VЭ(Н 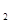 ).
).
Объем эквивалентной массы водорода при н.у. равен половине молярного объема 22,4/2 = 11,2 л. Подставив в приведенную формулу значения VН 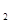 = 1,4 л, VЭ(Н
= 1,4 л, VЭ(Н 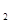 ) = 11,2 л, t = 6025 (1 ч 40 мин 25 с=6025с), находим
) = 11,2 л, t = 6025 (1 ч 40 мин 25 с=6025с), находим
I = 1,4∙96,500/(11.2*6025) = 2А
Пример 4.Какая масса гидроксида калия образовалась у катода при электролизе раствора K2SO4, если на аноде выделилось 11,2 л кислорода (н.у.)?
Решение. Объем эквивалентной массы кислорода (н.у.) 22,4/4 = = 5,6 л. Следовательно, 11,2 л содержат две молярные массы эквивалента кислорода. Столько же эквивалентных масс КОН образовалось у катода, или 56,11 ∙ 2 = 112,22 г (56,11 г/моль — молярная и эквивалентная масса КОН).
8.3Коррозия металлов
При решении задач этого раздела см. табл. 8.
Коррозия — это самопроизвольно протекающий процесс разрушения металлов в результате химического или электрохимического взаимодействия их с окружающей средой.
При электрохимической коррозии на поверхности металлаодновременно протекают два процесса: анодный — окисление металла
Ме°-пе=Меп+ и катодный — восстановление ионов водорода
2Н+ + 2е = Н2
или молекул кислорода, растворенного в воде,
О2 + 2Н2О + 4е- = 4ОН-
Ионы или молекулы, которые восстанавливаются на катоде, называют деполяризаторами. При атмосферной коррозии — коррозии во влажном воздухе при комнатной температуре — деполяризатором является кислород [1].
Пример 1.Как происходит коррозия цинка, находящегося в контакте с кадмием в нейтральном и кислом растворах. Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
Решение. Цинк имеет более отрицательный потенциал (-0,763 В), чем кадмий (-0,403 В), поэтому он является анодом, а кадмий катодом.
Анодный процесс:
Zn°-2e-=Zn2+ катодный процесс:
в кислой среде 2Н+ + 2е- = Н2
в нейтральной среде ½ О2 + Н2О + 2е- = 2ОН-
Так как ионы Zn2+ с гидроксильной группой образуют нерастворимый гидроксид, то продуктом коррозии будет Zn(OH)2.
Дата добавления: 2019-09-30; просмотров: 691;











