Меркаптаны (тиоспирты, тиолы)
Меркаптаны – органические производные сероводорода, содержащие углеводородный радикал, связанный с сульфгидрильной группой – SH.
Получение. Меркаптаны содержатся в небольших количествах в нефтях.
Основные методы синтеза меркаптанов:
1) пропускание смеси паров спирта и Н2S над катализатором ТhO2 :
R―OH 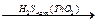 R―SH + H2O;
R―SH + H2O;
2) действие элементарной серы на металлорганические соединения с последующим гидролизом:
R―MgX 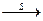 R―S―MgX
R―S―MgX 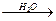 R―SH;
R―SH;
3) действие серы на ароматические углеводороды в присутствии солей алюминия
C6H6 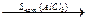 C6H5SH + HCl.
C6H5SH + HCl.
Физические свойства. Меркаптаны, особенно низшие члены гомологического ряда, обладают ярко выраженным специфическим запахом, благодаря чему могут быть обнаружены в воздухе в концентрации 2·10-9 мг/л. Алифатические меркаптаны R―SH c C1 – C4 – являются газами с температурами кипения от 6 0С до 98,2 0С. С увеличением количества углеродных атомов температуры кипения повышаются. Тиофенол С6Н5SH – бесцветная жидкость с неприятным запахом, tкип = 169 0С.
Химические свойства определяются наличием подвижного атома водорода, связанного с атомом серы, а также неподеленной пары электронов на атоме серы.
1. Являясь слабыми кислотами, меркаптаны легко растворяются в щелочах с образованием металлических производных – меркаптидов:
RSH + NaOH → RSNa + H2O.
2. С оксидами тяжелых металлов также образуются соответствующие меркаптиды:
2RSH + MeO → (RS)2Me + H2O.
3. Ацилирование меркаптанов в присутствии оснований приводит к образованию соответствующих S – ацильных производных:
O O
|| ||
RSH + CH3C―CI 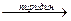 RSC―CH3 + HCl.
RSC―CH3 + HCl.
Тиофенол (фенилмеркаптан) является более сильной кислотой, чем фенол, легко образует устойчивые соли щелочных и тяжелых металлов. Остальные реакции аналогичны алифатическим меркаптанам.
Дата добавления: 2018-11-26; просмотров: 2226;











