Уровням и подуровням у элементов больших периодов
Формирование четвертого и последующих периодов сложнее, чем у элементов малых периодов.
В соответствии с первым правилом Клечковского четвертый период начинает заполняться электронами с 4s – AO у калия [Ar] 4s1 и [Ar] 4s2 – у кальция. В последующем в соответствии со вторым правилом Клечковского происходит заполнение 3d – подуровня, начиная с элемента скандия [Ar] 3d14s2 (табл. 3).
Таблица 3
Электронные конфигурации элементов
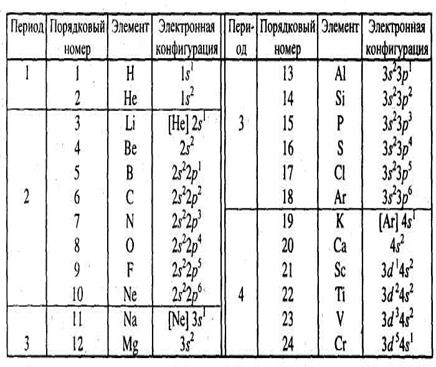
|
Продолжение табл. 3
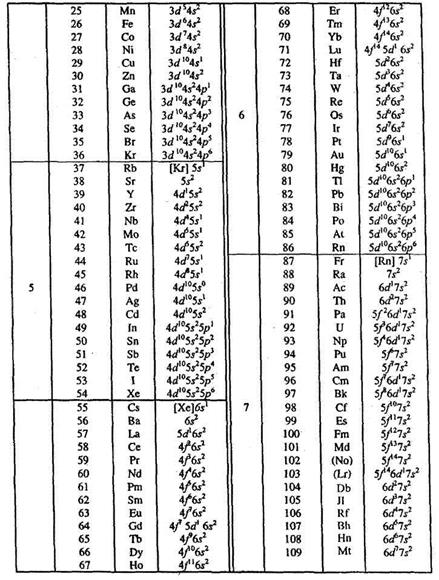
|
Из табл. 3 видно, что в некоторых элементах последовательность заполнения 3d – АО происходит перемещение электрона с более высокого уровня на еще незаполненный подуровень более низкого уровня (так называемый ''провал'' электрона). Так, например, в атоме хрома в место казалось бы, нормального размещения электронов по формуле [Ar] 3d44s2, фактически размещение электронов выражается конфигурацией [Ar] 3d54s1. Подобные отступления наблюдаются также и у атомов меди, ниобия и некоторых других элементов.
В пятом периоде, содержащем 18 элементов, как и в четвертом периоде, вначале заполняется 5s – AO, затем 4d – AO, а завершается период заполнением 5p – AO.
Шестой период содержит 32 элемента и начинается, как и предыдущие с s – элементов (цезий, барий). Затем в соответствии с правилом Клечковского происходит заполнение 4f – AO (n = 4, l = 3). Элементы с семью 4f – AO, заселяемыми электронами от лантана до иттербия, называют лантаноидами, что означает – подобные лантану. В седьмом периоде появляются 5 – элементы от актиния до жолиотия, известные под общим названием актиноиды – подобные актинию.
Седьмой период еще не завершен, он должен заканчиваться элементом с z = 118, экардоном.
Дата добавления: 2016-12-09; просмотров: 2220;











