Атомно-молекулярное учение
Понятие о материи и движении
Современная химия является одной из естественных наук, предметом изучения которых является материя и представляет собой систему отдельных химических дисциплин – неорганической, аналитической, физической, органической, коллоидной и др.
Весь окружающий нас многообразный мир, вся совокупность предметов и явлений объединяются общим понятием – материя, для которой известны две формы существования – вещество и поле.
Вещество представляет собой материальное образование состоящее из частиц, имеющих собственную массу или массу покоя. Современной науке известны различные типы материальных систем и соответствующие им структурные уровни материи. К ним относятся как элементарные частицы (электроны, протоны, нейтроны и т.д.), так и макроскопические тела различных размеров (геологические системы, планеты, звезды, звездные скопления, Галактика, системы галактик и др.) современные познания структуры материи простираются от 10-14 см до 1028 см (примерно 13 млрд. световых лет).
В отличие от вещества - поле – материальная среда, в которой осуществляется взаимодействие частиц. Например, в электронном поле происходит взаимодействие между заряженными частицами, а в ядерном - между протонами и нейтронами.
Всеобщими формами бытия материи являются пространство и время, которые не существуют вне материи, как не может быть и материальных объектов, которые не обладали бы пространственно – временными свойствами.
Коренным и неотъемлемым свойством материи является движение - способ её существования. Формы движения материи очень разнообразны, они взаимно связаны и могут переходить из одной в другую. Например, механическая форма движения материи может переходить в электрическую форму, электрическая - в тепловую и т.д. Мерой движения материи, количественной его характеристикой является энергия.
Определение химии
Различные формы движения материи изучаются различными науками – физикой, химией, биологией и др. Химия изучает химическую форму движения материи, под которой понимается качественное изменение веществ, превращение одних веществ в другие. При этом разрываются, вновь возникают или перераспределяются химические связи между атомами, входящими в состав вещества. В результате химических процессов возникают новые вещества с новыми физико-химическими свойствами.
Таким образом, химия это наука, изучающая процессы превращения веществ, сопровождающиеся изменением состава, структуры и свойств, а также взаимные переходы между этими процессами и другими формами движения материи.
Объектом изучения в химии являются химические элементы и их соединения. Изучая свойства веществ и их превращения химия раскрывает законы природы, познает материю и её движение. Изучение химии как одной из важнейших фундаментальных естественных наук необходимо для формирования научного мировоззрения.
Атомно-молекулярное учение
Атомно-молекулярное учение развил и впервые применил в химии великий русский ученый М.В. Ломоносов. Основные положения его учения изложены в работе "Элементы математической химии". Сущность учения М.В. Ломоносова сводится к следующему.
1. Все вещества состоят из "корпускул" (так М.В. Ломоносов назвал молекулы). 2. Молекулы состоят из элементов (атомов). 3. Частицы - молекулы и атомы находятся в непрерывном движении. 4. Молекулы простых веществ состоят из одинаковых атомов, молекулы сложных веществ - из различных атомов.
В дальнейшем это учение получило развитие в работах Д. Дальтона и Я. Берцелиуса. Окончательно атомно-молекулярное учение в химии утвердилось в середине ХIХ века. На Международном съезде химиков в г. Карлсруэ в 1860 г. были приняты определения понятий химического элемента, атома и молекулы.
Атом - наименьшая частица химического элемента, обладающая его химическими свойствами и неделимая при химических реакциях.
Молекула - наименьшая частица вещества, обладающая его химическими свойствами. Химические свойства молекулы определяются ее составом и химическим строением.
Все вещества делятся на простые и сложные.
Простое вещество – состоит из атомов одного и того же элемента.
Сложное вещество – состоит из атомов разных элементов. Так, например, оксид меди (II) образован атомами элементов меди и кислорода.
Всего 100 лет назад атом рассматривался как неделимый объект. Однако в соответствии с современными представлениями атом имеет сложную структуру и состоит из трех субатомных частиц: протонов, нейтронов и электронов. Протоны имеют положительный заряд; нейтроны не имеют заряда, а электроны имеют отрицательный заряд. Заряды на протоне и электроне одинаковы по величине. Протоны и нейтроны занимают вместе очень небольшой объем атома, называемый ядром. Большую часть остального объема атома составляет пространство, в котором движутся электроны. Поскольку атомы не имеют результирующего электрического заряда, в каждом атоме содержится равное число электронов и протонов. Заряд ядра определяется числом протонов.
Химический элемент - вид атомов, характеризующихся одинаковым зарядом ядра и, соответственно, характеризующихся определенной совокупностью свойств. Атомы одного и того же элемента, отличающиеся числом нейтронов, и, следовательно, массой, называются изотопами. Символ 126С или просто 12С означает атом углерода с шестью протонами и шестью нейтронами. Число протонов в ядре атома называется атомным номером. Верхний индекс (12) называется массовым числом и указывает суммарное число протонов и нейтронов в ядре атома.
Понятие "химический элемент" нельзя отождествлять с понятием "простое вещество". Простое вещество характеризуется определенной плотностью, растворимостью, температурами плавления и кипения и др. Эти свойства относятся к совокупности атомов и для разных простых веществ они различны.
Химический элемент характеризуется определенным зарядом ядра, изотопным составом и др. Свойства элемента относятся к его отдельным атомам.
Сложные вещества состоят не из простых веществ, а из элементов. Например, вода состоит не из простых веществ водорода и кислорода, а из элементов водорода и кислорода.
Многие химические элементы образуют несколько простых веществ, различных по строению и свойствам. Это явление называется аллотропией, а образовавшиеся вещества - аллотропными видоизменениями или модификациями. Так, элемент кислород образует две аллотропные модификации: кислород О2 и озон О3; элемент углерод - три: алмаз, графит и карбин.
Химическая форма движения материи исследуется и познается измерением физических свойств и физических величин, присущих каждому веществу. Физической величиной является, например, масса вещества, его плотность, температура плавления. В химии широко используются понятия относительной атомной и молекулярной массы вещества.
Относительная атомная масса.Массы атомов чрезвычайно малы. Так, масса атома водорода составляет 1,674×10-27 кг, кислорода - 2,667×10-26 кг. В химии традиционно применяют не абсолютные значения масс, а относительные. За единицу относительных масс принята атомная единица массы (сокращенно а.е.м.), представляющая собой 1/12 массы атома углерода - 12, т.е. изотопа углерода 6С - 1,66×10-27 кг. Поскольку большинство элементов имеют атомы с различной массой, поэтому относительная атомная масса химического элемента есть безразмерная величина, равная отношению средней массы атома естественного изотопического состава элемента к 1/12 массы атома углерода.
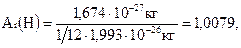 |
Относительную атомную массу элемента обозначают Аr. Например,
где 1,993·10-26 кг – масса атома углерода.
Относительная молекулярная масса.Относительные молекулярные массы, так же как и атомные, выражаются в атомных единицах массы. Относительная молекулярная масса вещества есть безразмерная величина, равная отношению средней массы молекулы естественного изотопического состава вещества к 1/12 массы атома углерода 126С.
Относительную молекулярную массу обозначают Мr. Она численно равна сумме относительных атомных масс всех атомов, входящих в состав молекулы вещества, и подсчитывается по формуле вещества. Например, Mr (H2О) будет слагаться из 2 Аr (Н)» 2; Аr (O)= 1 × 16 = 16; Mr (H2О) = 2 + 16 = 18.
Моль.В международной системе единиц (СИ) за единицу количества вещества принят моль. Моль - это количество вещества, содержащее столько структурных или формульных (ФЕ) единиц (молекул, атомов, ионов, электронов или других), сколько содержится атомов в 0,012 кг изотопа углерода 126C.
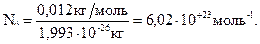 |
Зная массу одного атома углерода 12C (1,993×10-26 кг), вычисляют число атомов NA в 0,012 кг углерода.
Число частиц в 1 моль любого вещества одно и то же. Оно равно 6,02×1023 и называется постоянной Авогадро (обозначается NA, размерность 1/моль или моль-1). Очевидно, в 2 моль углерода будет содержаться 2 × 6,02×1023 атомов, в 3 моль - 3 × 6,02×1023 атомов.
Молярная масса.Обычно ее обозначают M. Молярная масса - величина, равная отношению массы вещества к количеству вещества. Она имеет размерность кг/моль или г/моль. Например, M = m/n или M = m/n , где m - масса в граммах; n (ню) или n - количество вещества в молях, M - молярная масса в г/моль - постоянная величина для каждого данного вещества. Так, если масса молекулы воды равна 2,99×10-26 кг, то молярная масса M (H2O) = 2,99×10-26 кг × 6,02×1023 моль-1 = 0,018 кг/моль или 18 г/моль. В общем случае молярная масса вещества, выраженная в г/моль, численно равна относительной атомной или относительной молекулярной массе этого вещества.
Например, относительные атомные и молекулярные массы C, O2, H2S соответственно равны 12, 32, 34, а их молярные массы составляют соответственно 12, 32, 34 г/моль.
Дата добавления: 2016-12-09; просмотров: 3750;











