Понятия о явлениях переноса. Средняя длина свободного пробега, эффективный диаметр молекул.
Молекулярно-кинетическая теория имеет дело с равновесными состояниями и обратимыми процессами, то есть процессами, при которых система проходит через последовательность равновесных состояний. Наука, изучающая процессы, возникающие при нарушениях равновесия, носит название физической кинетики. Нарушение равновесия сопровождается переносом массы (диффузия), импульса (внутреннее трение) или энергии (теплопроводность). Эти процессы называются явлениями переноса. Они возникают самопроизвольно вследствие теплового движения при отклонении вещества от равновесного состояния и являются необратимыми.
Явления переноса протекают медленно, свободному движению молекул препятствуют их взаимные столкновения. Молекулы газа, находясь в тепловом движении, непрерывно сталкиваются друг с другом. Под столкновением молекул подразумевается процесс взаимодействия между молекулами, в результате которого молекулы изменяют направление своего движения. Столкновения молекул представляют как раз тот механизм, который приводит систему в равновесное состояние. В идеальном газе эти столкновения происходят только между двумя молекулами, а одновременными столкновениями между тремя и большим числом молекул можно пренебречь.
Расстояние, которое проходит молекула между двумя последовательными столкновениями, называется длиной свободного пробега молекулы. Так как молекул в газе чрезвычайно много, то вводят понятие средней длины свободного пробега молекул. Средней длиной свободного пробега молекул `l называется среднее расстояние, которое молекула проходит без столкновений.
При столкновении молекулы сближаются до некоторого наименьшего расстояния, которое условно считается суммой радиусов взаимодействующих молекул. Столкновение между молекулами может произойти только в том случае, если их центры сблизятся на расстояние, меньшее и равное диаметру d, или столкновение произойдет только в том случае, если центр молекулы окажется внутри круга, имеющего площадь: s =p d2.
Величина s называется сечением рассеяния, или эффективным сечением, d - эффективный диаметр. Эффективный диаметр молекулы – минимальное расстояние, на которое сближаются центры двух молекул при столкновении.
Число столкновений, испытываемых молекулой в единицу времени, может быть различным. Поэтому следует говорить о среднем значении этой величины 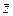
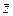 =
= 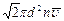 , (7.1.1.)
, (7.1.1.)
где n – концентрация молекул.
Средняя длина свободного пробега 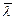 и среднее число столкновений в единицу времени
и среднее число столкновений в единицу времени 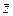 являются главными характеристиками процесса столкновений газовых молекул. Эти величины связаны между собой:
являются главными характеристиками процесса столкновений газовых молекул. Эти величины связаны между собой:
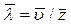 ,
,
где 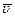 – средняя арифметическая скорость.
– средняя арифметическая скорость.
Используя формулу (7.1.1), вычислим среднюю длину свободного пробега
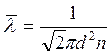 . (7.1.2)
. (7.1.2)
При нормальных условиях для молекул воздуха (азота) 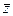 =9·109 с-1,
=9·109 с-1, 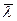 »10-7 м. Это очень малое расстояние, однако d <<
»10-7 м. Это очень малое расстояние, однако d << 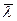 , и время пребывания молекул под взаимным воздействием в `l/ d, то есть в 1000 раз меньше времени их свободного движения. Следовательно, подавляющую часть времени молекулы движутся свободно. При постоянной температуре концентрация газа пропорциональна его давлению (р=nkT) и средняя длина свободного пробега молекул: `l =
, и время пребывания молекул под взаимным воздействием в `l/ d, то есть в 1000 раз меньше времени их свободного движения. Следовательно, подавляющую часть времени молекулы движутся свободно. При постоянной температуре концентрация газа пропорциональна его давлению (р=nkT) и средняя длина свободного пробега молекул: `l = 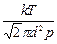 .
.
С уменьшением давления длина свободного пробега молекул возрастает в той же мере, в какой падает давление (`l ~ 1/р). При определенном значении давления она станет равной размерам сосуда.
Диффузия газов.
Диффузия есть процесс проникновения одного газа в объем, занятый другим газом, или же движение газа из области повышенной концентрации в область, где концентрация ниже (самодиффузия). Если газ предоставлен самому себе, то в результате диффузии происходит постепенное выравнивание концентраций. Если же неравновесное состояние поддерживается неизменным, то устанавливается стационарный (не зависящий от времени) процесс.
Пусть в большом сосуде с плоскими стенками поддерживается разность концентраций газа n1 и n2.
Разность числа прошедших молекул через площадку S, согласно представлениям молекулярно-кинетической теории, равна:
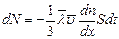 (7.2.1)
(7.2.1)
Задолго до появления молекулярно-кинетических представлений Фиком был эмпирически установлен закон диффузии:
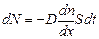 , (7.2.2)
, (7.2.2)
где D – коэффициент диффузии.
Из полученного с помощью кинетической теории соотношения (7.1.1) и закона Фика (7.2.2) коэффициент диффузии: 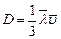 ([D]=м2/с).
([D]=м2/с).
Умножим обе части (7.2.2) на массу одной молекулы m0 и учтем, что r=n·m0 - плотность компонента переносимого газа, dm=n0dN - переносимая масса газа: 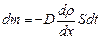 .
.
Отсюда сформулируем физический смысл коэффициента диффузии. Коэффициент диффузии – это масса, переносимая в единицу времени через единичную площадку в направлении нормали к этой площадке в сторону убывания плотности компонента при градиенте плотности, равном единице.
Коэффициент диффузии определяется из опыта по измеренной переносимой массе. Рассмотрим ее зависимость от внешних условий.
`l ~ 1/n ~ Т/р; 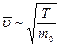 Þ D ~
Þ D ~ 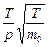 .
.
Коэффициент диффузии определяется давлением, температурой и родом газа.
Дата добавления: 2016-12-09; просмотров: 1954;











