Сущность процесса и область применения
Абсорбцией называется процесс поглощения газов или паров из газовых или парогазовых смесей жидкими поглотителями (абсорбентами). При физической абсорбции поглощаемый газ (абсорбтив) не взаимодействует химически с абсорбентом. Если же абсорбтив образует с абсорбентом химическое соединение, то процесс называется хемосорбцией.
Физическая абсорбция в большинстве случаев обратима. На этом свойстве абсорбционных процессов основано выделение поглощенного газа из раствора - десорбция. Сочетание абсорбции с десорбцией позволяет многократно использовать поглотитель и выделять поглощенный компонент в чистом виде.
В промышленности процессы абсорбции применяются главным образом для извлечения ценных компонентов из газовых смесей или для очистки этих смесей от вредных примесей. Для проведения процессов абсорбции применяют абсорбенты, обладающие избирательной, селективной способностью.
Абсорбционные процессы обычно сопровождаются тепловыми процессами. При этом в большинстве из них наблюдается выделение теплоты.
Физическая сущность процесса заключается в растворении газов в жидкости. Зависимость между растворимостью газа и парциальным давлением выражается законом Генри, в соответствии с которым растворимость газа при данной температуре прямо пропорциональна парциальному давлению газа над жидкостью:
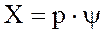 , (3-19)
, (3-19)
где X - количество растворенного газа, отнесенное к поглощающей жидкости, моль/м3; ψ- коэффициент пропорциональности, зависящий от свойств абсорбента и температуры; p - парциальное давление абсорбтива, Па.
В соответствии с законом Дальтона в газовой смеси парциальное давление какого-либо компонента можно выразить уравнением:
p=y pобщ (3-20)
где y- доля рассматриваемого компонента (абсорбтива) в газовой смеси; pобщ - общее давление газовой смеси, Па.
Из выражений (3-19) и (3-20) следует:
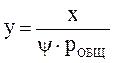 , (3-21)
, (3-21)
 Обозначив отношение
Обозначив отношение 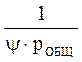 через H , получим уравнение фазового равновесия:
через H , получим уравнение фазового равновесия:
y=H x, (3-22)
где H - константа фазового равновесия.
Уравнение (3-22) показывает, что зависимость между концентрацией данного компонента в газовой смеси и в равновесной с ней жидкости выражается прямой линией, проходящей через начало координат и имеющей угол наклона, тангенс которого равен 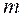 (рис.3.4). Численные значения
(рис.3.4). Численные значения 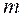 зависят от температуры и давления: уменьшаются с увеличением давления и снижением температуры.
зависят от температуры и давления: уменьшаются с увеличением давления и снижением температуры.
Таким образом, растворимость газа в жидкости увеличивается с повышением давления и снижением температуры.
Дата добавления: 2016-11-29; просмотров: 2229;











