Индекс экскреции и задержки
Одним из важнейших аспектов связи объекта и окружающей его среды является его потребление и выделение. Концепция иерархической организации, относительно индивидуальности объектов, придала особое значение изучению указанных процессов. Для каждого объекта его собственное окружение представлено вторичной частью объекта, находящегося непосредственно выше него. Ядерный сок, таким образом, представляет окружающую среду, из которой хромосомы берут материал для своего обмена веществ и где они освобождаются от веществ, в которых больше не нуждаются. Подобным же образом, цитоплазма представляет окружение ядра, интерстициальная жидкость - для клеток, лимфа - для тканей, кровь - для органов, а реальная окружающая среда - для организма. Указанная систематизация, основанная на организационной индивидуальности объектов, помогала планировать изучение связи между объектами и окружающей их средой при нормальных и ненормальных условиях. Именно в указанном аспекте мы исследовали экскреторную функцию почек, которые в соответствии с иерархической организацией, соответствует связи между организмом, в качестве объекта, и окружающей его средой.
Некоторые выделяемые вещества происходят из метаболизма объектов более низкого уровня. Что касается крови, они будут представлены часто вредными нежелательными веществами, если не вмешивается более высокий механизм крови. Хотя те из них, что касаются мочи, являются результатом связи между организмом, в качестве объекта, и его окружением, происхождение разных веществ, формирующих его, относящихся к разным иным уровням, еще требует уяснения. Если для определенных элементов указанное происхождение очевидно, для многих веществ сегодня возможны лишь предположения.
Когда предпринималась попытка провести систематический анализ этих составных частей, возникали другие препятствия. Хотя анализы мочи легко доступны, они имеют весьма относительное значение для многих указанных исследований. Данные, полученные при титровании и выражаемые в виде концентрации разных веществ, все зависят от количества воды, элиминированного в пробе. Поскольку указанный показатель весьма вариабелен, получается очень относительная информация. Анализ баланса, предусматривающий исследование всего потребления и выделения представляет столь значительные технические сложности, что делает его неприемлемым для рутинного использования у сотен индивидуумов, подвергающихся исследованию ежедневно. Мы постарались преодолеть указанное затруднение путем элиминации из рассматриваемых данных фактора экскреции воды. Исключить указанный фактор позволило то обстоятельство, что концентрация вещества и относительная плотность мочи, обе, прямо зависят от количества присутствующей воды. Соотношение между ними оказывается, таким образом, не зависящим от количества присутствующей воды. Это связывает количество вещества с таковым, выделяемым почками. Индекс экскреции, таким образом, получали путем деления концентрации вещества на относительную плотность мочи. Противоположная пропорция будет соответствовать индексу ретенции.
С физиологической точки зрения, указанные выше отношения не зависят от факторов, управляющих клубочковой фильтрацией, действующих одинаково на все присутствующие вещества. Они также мало подвержены влиянию обратного всасывания, при котором различия разных веществ уменьшены. Они также обнаруживают большие вариации, являющиеся результатом активной реабсорбции, происходящей в дистальных отделах выводящих канальцев. Именно это свойство обусловливает значение индексов экскреции и ретенции, и их мы можем вычислять. Многие годы мы использовали указанные показатели для хлоридов, натрия, калия, иона фосфора, сульфгидрила, кальция, для получения ценной информации, которую нельзя добыть из простого анализа отдельных проб мочи. Мы вернемся к указанным индексам при дальнейших исследованиях.
Глава 4, Заметка 16.Вода и обмен азота
Анализ разных проб мочи показал, что количество присутствующей в моче воды косвенно влияет на ее состав. Таким образом, можно представить, что при очень разведенной моче, соответствующей большому количеству выделенной мочи, она обычно имеет щелочную реакцию, а концентрированная моча, соответствующая малым количествам выделенной мочи, обычно кислая. Более того, можно наблюдать, что указанные изменения связаны с более глубокими метаболическими различиями. Если учитывать обмен азота, можно увидеть, что разведенная моча богата свободными аммониевыми радикалами, в то время как концентрированная - мочевой кислотой. Мы исследовали связь между указанными двумя факторами, количеством выделяемой мочи и формой, в которой элиминируется азот.
Сравнительная физиология показывает нам, что способ, каким азот выделяется, различен у разных животных и соответствует количеству воды, доступному в окружающей среде. У рыб, для которых ограничений по воде нет, азот выделяется в форме аммония. Высокая токсичность указанной формы выделения азота уравновешивается количеством воды, в которой экскрет разведен. Рыбы являются аммониоселиками. У сухопутных животных, у которых доступ к воде более ограничен, выделение азота осуществляется в форме мочевины, значительно менее токсичной, чем аммоний. Таким образом, снижается опасность отравления выделениями при питье воды. Млекопитающие являются уреоселическими животными. У птиц, для которых вода менее доступна, форма выделения азота представлена мочевой кислотой, которая вследствие своей слабой растворимости в воде имеет небольшие шансы загрязнить питьевую воду. Птицы являются уроселиками. Основываясь на этой связи между доступностью воды и типом выделяемого азота, мы искали подобную связь и у человека между количеством выделяемой мочи и типом азота, метаболизируемого при нормальных и ненормальных условиях. Немедленное подтверждение было получено при тех ненормальных условиях, когда количество выделяемой воды было ненормальным. Как мы уже показывали, у индивидуумов, имеющих высокий диурез, который, обычно будет соответствовать высокому количеству доступной для выделения из организма воды, моча обычно щелочная за счет аммония. И наоборот, в противоположной от нормы стороне находятся индивидуумы с очень небольшим количеством выделяемой мочи. У пациентов, выделяющих лишь 200-300 см3 мочи за сутки, количество мочевой кислоты в моче заметно увеличено. При отстаивании указанные пробы всегда обнаруживают красноватый осадок, формируемый главным образом, мочевой кислотой. Сравнительная физиология в указанных случаях состоит в следующем. В то время как нормальные индивидуумы выглядят уроселиками, страдающие полиурией могут считаться аммониоселиками, а олигурией - урикоселиками.
Мы попытались выяснить, не повлияет ли изменение количества воды, подлежащей экскреции, на форму выделяемого азота. Нормальным индивидуумам, чья моча тестировалась определенное количество времени на предмет содержания в ней аммония, мочевины и мочевой кислоты, давали пить от 1 до 2 литров воды. Высоко разведенная моча, которая в последующем выделялась, становилась щелочной. Общее количество аммония увеличилось, в то время как мочевина и мочевая кислота слегка уменьшились. Позже этим же индивидуумам прекратили давать пить в течение 12 часов и более. В большинстве указанных случаев относительная плотность мочи составила более 1.026, что свидетельствовало о нормальной концентрационной функции почек. Хотя содержание аммония в этих пробах мочи заметно уменьшилось, увеличение выделения мочевой кислоты было минимальным. Мы подвергли этих же индивидуумов диетическим ограничениям с минимумом потребления воды в течение 3-4 дней. При этих условиях выделение мочевой кислоты стало возрастать. Большое потребление воды, таким образом, трансформировало нормального уреоселического индивидуума в аммониоселического всего за несколько минут. Такой же переход в уреоселика возможен лишь на протяжении нескольких дней и даже тогда обнаруживались лишь минимальные изменения. Это может быть объяснено тем фактом, что если аммоний в моче появляется, главным образом, благодаря изменениям в самих почечных клетках, мочевая кислота является результатом более глубоких метаболических сдвигов, затрагивающих особенно азотистые основания, в частности пурины.
Глава 5, Заметка 1.рН струпа поверхности раны второго дня
Метаболические процессы, характеризующие патологические очаги, исследовались разными путями. Один из методов предназначался для изучения изменений кислотно-щелочного равновесия, происходящих в ненормальных очагах, полученных хирургическим путем, ран под воздействием разных химических, физических и биологических факторов. Указанное исследование выполнено в сотрудничестве с C. Huesca-Mejia. (212)
Использовались взрослые Carworth Farm женские и мужские особи крыс-альбиносов, весом от 150 до 200 г. Животные были разделены по половому признаку и получали стандартную диету Purina Chow и воду ad lib. Исследования проводились на группах из 20 животных, с двумя-четырьмя контрольными животными в каждой из групп.
Животные были разделены на группы по экспериментальным воздействиям на них, производимым на протяжении трех дней, после чего под эфирным наркозом широкая область спины каждого животного была подвергнута ручной депиляции. Затем в депилированной области им наносилась рана площадью 1 см2 глубиной до апоневроза спины. Рана поддерживалась обескровленной благодаря прижатию к ней сухого марлевого шарика вплоть до полного прекращения кровотечения и оставлялась открытой. Все раны наносились в промежутке времени между 8 и 10 часами утра.
Использовали стеклянный электрод, изготовленный согласно спецификациям Mclnnes и Dole (223). В соответствии с их методикой, применяли эталонный электрод, содержащий нормальный физиологический раствор. (224) Электроды поднимались на штативе в фиксированное положение. Использовали рН-метр модели H Beckman, чей сигнал усиливался путем 6H6 и 6SN7 подтяжек в виде первого усилителя. Записи осуществлялись на 200 микроамперметре, откалиброванном таким образом, чтобы представлять всю шкалу в виде одной единицы рН. При использовании указанного аппарата экспериментальная ошибка составила менее ± .01.
Замеры pH проводили путем осуществления контакта области раны с концами электродов. Животные удерживались осторожно, но крепко, в одной руке вплоть до их полного обездвиживания, в то время как устанавливался плотный контакт центра области раны и концом стеклянного электрода и между эталонным электродом и периферией раны. Записи производили со свежеобнаженного апоневроза в течение 10-15 минут после хирургической операции. Последующие записи делались каждые 24 часа с поверхности раны, омытой и затем увлажненной каплей 0.1% раствора хлорида натрия, непосредственно приготовленного до pH 5, как предложено Blank для замеров рН кожи. (225) Электроды были стандартизированы буферами с разными значениями рН до тестирования и в течение каждого периода тестирования.
Воздействие разных химических агентов на рН раны изучали путем ежедневного перорального замера рН в течение трех дней, предшествовавших операции, и с этого времени -вплоть до завершения серии замеров рН. Обычно, вещества назначались в соответствии с весом, в количествах, соответствующих лечебным дозам, принятым для человека, или в количествах, равных 10% дневной токсической дозы. Водорастворимые вещества назначались в питьевой воде. Жирорастворимые вещества назначались на кусках хлеба. В некоторых случаях вещества вводились непосредственно в желудок через катетер. В нескольких случаях вещества вводились путем подкожной инъекции.
У 164 контрольных животных pH поверхности раны колебался между 7.30 и 7.33, при замере через 10-15 минут по завершению хирургической операции. Уровень рН не менялся на протяжении, по меньшей мере, трех часов.
Через 24 часа после образования ран, pH влажной поверхности, покрывающей область раны, колебался между 7.72 и 7.76 у всех животных, которым препарат не вводили. (Рис. 234)
Ко времени 48 часов после нанесения раны рН струпа колебался, что представляло период наибольших вариаций. На 72-ой и 96-ой час все замеры находились в пределах 7.28 - 7.32. После пятого дня были обнаружены такие же значения, и далее замеры не проводились.
Между значениями разных дней у одного и того же животного устойчивой связи не обнаружено. Например, у некоторых животных с рН раны 7.30—самой низкой величиной—непосредственно после операции, через 24 часа pH достиг 7.76, наивысшего значения для нормального разброса данных. У самцов, показатели оказались слегка выше, чем у самок.

Рис. 234. Значения рН струпа раны второго дня оставались между 7.72 и 7.76 у нормальных крыс, что наблюдалось у животных-контролей, служивших для проведения множественных экспериментов.
У 410 из 860 животных, подвергшихся воздействию различных химикатов, значение pH ран определялось через несколько минут после операции и составило между 7.28 и 7.35. Только у 22 отмечено отклонение от контрольных границ от 7.30 до 7.33. Связи между минимальными изменениями у этих животных и типом назначенного лечения не выявлено.
В то время как значения pH, обнаруженные через несколько минут после индукции раны, были в границах контрольных значений, или очень немного отличались от них и не были связаны с использованными разнообразными экспериментальными условиями, то в срок 24 часа обнаруживали изменения, характеризовавшие определенную относительную значимость использованных агентов. Через 24 часа и позже между величинами контролей и группами, подвергшимися различным воздействиям, значимой связи установлено не было. Продолжая указанные исследования, оценку осуществляли сразу через несколько минут после нанесения экспериментальных ран, и затем опять 24 часами позже. В действительности, только величины 24-часовых исследований оказались значимыми, и будут обсуждаться. Мы выполнили 24-часовые исследования у всех 860 животных, подвергшихся действию разными агентами. Для большей достоверности мы будем ссылаться на значения рН земной коры через 24 часа после нанесения экспериментальной раны, как на pH второго дня.
При испытании активности каждого из агентов использовались от двух до двенадцати животных. Применяя одинаковые условия эксперимента в группах животных, тестированных в разное время, оказалось возможным определить, являются ли наблюдавшиеся изменения следствием влияния некоторых внешних факторов, таких как температура, влажность и прочие, или они действительно были вызваны особыми условиями эксперимента. Особый интерес вызвал рН раны второго дня, поскольку одинаковые изменения вызывались одними и теми же агентами при их использовании в разных группах животных, протестированных с разрывом в несколько недель или месяцев.
Учитывая всех животных, подвергшихся тестированию с разными агентами, была установлена возможность существования трех следующих вариантов: 1) Воздействия на рН раны второго дня, могло не быть, в этом случае все значения окажутся в контрольных пределах от 7.72 до 7.76, установленных для нетестированных животных; 2) рН раны второго дня может подниматься до значений между 7.77 и 7.85; или 3) рН раны второго дня pH может быть уменьшено до значений от 7.70 до 7.60.
Ниже мы приводим выводы из проведенных указанных исследований исключительно в связи с применявшимися изучаемыми агентами.
ХИМИЧЕСКИЕ ФАКТОРЫ
Катионы и анионы
Интересным казалось изучение влияния, оказываемого некоторыми катионами и анионами, сначала используя один и тот же анион с разными катионами и затем, используя разные анионы с одним и тем же катионом. Во всех экспериментах оказалось очевидным, что непосредственный показатель рН раны не отличается от такового у нелеченных животных, и что данные рН раны второго дня у них согласуются.
Мы изучили влияние, оказываемое анионами, сначала, исследуя эффекты назначения кислот. Даже при использовании сильных органических кислот в нормальных тканях изменений не обнаружено. Определенные и противоположные эффекты были получены с кислотами, соответствующими элементам седьмой серии и с таковыми шестой серии. Первая группа кислот, особенно HC1, вызвала явный окисляющий эффект, в то время как вторая вызывала ощелачивающий эффект. Фосфатные и азотистые ионы обнаруживали сильное закисление, ионы иодидов и бромидов оказались слабее ионы хлорида. Явно ощелачивался ион бикарбоната, также как и сульфата и селената. Ион тиосульфата имел явное ощелачивающее действие с повышением значения рН до 7.85. Среди органических кислот, лимонная кислота оказывает одно из самых сильных воздействий, сильнее даже чем у неорганических кислот. Силу лимонной кислоты обусловливает то, что она слабо метаболизируется. Ион глюконата вызывает слабое закисление. Ион карбоната, похоже, не вызывает изменений, хотя для проверки указанного факта использовали достаточно животных.
При изучении эффектов солей, выясняли роль и катиона и аниона. Удостовериться в действии катиона оказалось возможным, используя разные анионы по отношению к одному и тому же катиону.
Натрий и литий давали относительно слабое закисление. Калий закислял заметно, также как и аммоний, однако последний из них менее выражено. Заметный закисляющий эффект наблюдался у железа, ртути и висмута. Меньший эффект был получен со стороны молибдена и алюминия. С другой стороны, заметное ощелачивание было обнаружено для двухвалентного кальция, стронция, меди, бария и кобальта. Катионы магния и серебра, кажется, влияют на рН раны второго дня лишь слегка ощелачивающе. Похоже, у разных элементов наблюдается синергичный эффект, закисляющий или ощелачивающий. Указанное обстоятельство позволило нам удостовериться в эффектах разных ионов. Калий вызывает большее закисление, чем натрий, и, в то же время, большее закисление, чем аммоний. Хлорид калия, в котором указанные два иона обладают синергичным эффектом, является, таким образом, более явно закисляющим. Указанное также справедливо для кислого фосфата. Ощелачивающая тенденция иона сульфата противоположна окисляющему эффекту калия и объясняет легкое окисляющее действие сульфата калия. Учитывая относительно сильную ощелачивающую тенденцию иона карбоната, искали анион, способный противостоять закисляющему эффекту калия. Действие карбоната калия на рН раны второго дня находится в пределах нормы. Полученные в указанном исследовании данные побудили провести изучение вмешательства этих элементов в биологии, что является предметом Главы 5. В этой главе обсуждается информация, касающаяся влияния этих элементов на рН раны второго дня, также как и связи между указанным эффектом и структурой элементов.
Иону кальция свойственен ощелачивающий эффект, достаточно сильный чтобы противостоять закисляющим тенденциям таких анионов, как хлорид и фосфат. Более слабые закисляющие анионы, такие как лактат и глюконат, являются недостаточно сильными, чтобы противостоять ощелачивающей тенденции кальция, и соли кальция указанных кислот обладают сильным ощелачивающим действием.
Анализ показывает, что действие соли на местный показатель рН измененных тканей может быть удостоверен, учитывая синергичное действие, оказываемое анионом и катионом, причем эффект усиливается, если оба обладают однонаправленной тенденцией, и уменьшается при наличии противоположных тенденций. Мы не будем оценивать здесь прочие антагонистичные биологические эффекты катионов и анионов при их переходе от закисляющего (лимонная кислота и калий) к ощелачивающему (кальций и тиосульфат). Мы обсудим указанные эффекты в связи с фармакологическим исследованием указанных агентов. А сейчас мы лишь оценим указанный метод исследования.
Кислотные липоиды
Следующим шагом в применении рН раны второго дня было изучение эффектов особой группы кислот, которые нас заинтересовали, жирных кислот. Анализ полученных результатов ясно показывает важность неполярной группы. Карбоксил, в случае связывания с длинной цепью, как в жирных кислотах, сам по себе не способен вызывать изменения рН в поверхностной пленке раны второго дня, указанный показатель остается в пределах нормы. Вещество становится неактивным, когда неполярная группа не обладает собственным энергетическим центром или образованием. Насыщенные жирные кислоты, содержащие 10-16 атомов углерода, не влияют на рН раны второго дня. Присутствие двойных связей в неполярной группе изменяет оказываемое влияние. Все изученные ненасыщенные жирные кислоты обнаруживают ощелачивающее действие с относительно слабыми отличиями для более высоких ненасыщенных членов, таких как линоленовая или арахидоновая жирные кислоты, или смесь, полученная из жира печени трески. Тем не менее. изучение конъюгированных жирных кислот, таких как элеостеариновая или смесь кислот, начиная от жира печени трески, продемонстрировало в этой группе наивысшие величины, даже для такого малого количества, как 5 мг на животное в день. Эти данные указывают на роль энергетических образований в неполярных группах жирных кислот.
Мы отмечаем отличие между водорастворимыми органическими кислотами и группой жирных кислот, упомянутой выше. У предидущих, действие, вероятно, обусловлено участием карбоксила, что может объяснить высокую сильной активность трикарбоксиловой лимонной кислоты. В связи с важностью неполярной группы указанный карбоксил кажется не способным удерживать молекулу и, поэтому, не может действовать. Вмешательство двойной связи может осуществляться двумя путями: 1) путем связывания молекулы, таким образом увеличивая ее подвижность, что также уменьшает точку плавления; 2) в качестве энергетического центра, где происходят реакции. Тот факт, что десятиуглеродная тауровая кислота является неактивной, указывает на слабое влияние, которое можно ожидать от связывания одной молекулы, как в олеиновой кислоте. Влияние, оказываемое метаболическими изменениями, при которых жирные кислоты вмешиваются, благодаря энергетическим центрам в неполярной группе, объясняет тот факт, что они обладают местным ощелачивающим эффектом, вместо закисляющего эффекта многих других органических кислот. (Рис. 235)
Спирты
Роль связи между полярными и неполярными группами выглядит очень наглядно в исследовании ряда алифатических спиртов.
Группу агентов, широко используемых в нашем исследовании, мы рассматривали отдельно. Существуют органические вещества, имеющие радикал с двухвалентной серой в качестве полярной группы. Выше мы отмечали, что неорганическое вещество с таким же составом, тиосульфат натрия, оказывает сильный ощелачивающий эффект на pH второго дня. Подобный эффект на рН второго дня был получен со всеми препаратами, содержащими полярную тиоловую группу при пероральном или парентеральном назначении. Мы должны отметить необычную одинаковость результатов, редко встречающуюся в других биологических экспериментах. Оказывается, что ощелачивающее действие указанных препаратов является достаточным, чтобы преодолеть индивидуальные различия субъектов, получающих их. Такой же ощелачивающий эффект наблюдался и для тиосульфата натрия и, вероятно, является общим свойством для веществ, имеющих в своей полярной группе двухвалентную серу.
Указанные спирты не оказывают влияния на pH нормальных тканей, что показывают измерения, проведенные непосредственно после выполнения разреза кожи. Первые члены ряда, от метилового до пропилового спирта, не влияют на рН в поверхностной пленке раны второго дня.
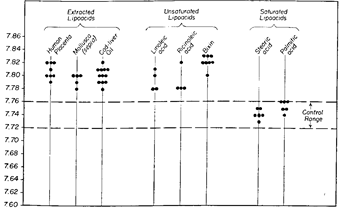
Рис. 235. Назначение разных жирных кислот и рН в поверхностной пленке раны второго дня. Продемонстрировано, что в то время как насыщенные жирные кислоты не оказывают на него влияния, ненасыщенные жирные кислоты и препараты жирных кислот, полученные из разных источников, вызывают подъем местного pH.
От бутилового до нонилового спирта, члены ряда обнаруживают устойчивое окисляющее влияние. Тем не менее, интересным оказалось наблюдение над четырьмя изомерами бутилового спирта. Три демонстрировали окисляющее действие, в то время как один, третичный изомер, как и более низкие спирты, не влиял на рН в поверхностной пленке раны второго дня. Указанный феномен мог быть связан с особыми свойствами этих веществ, их особой растворимостью в воде и нейтральных растворителях. Также как и низшие спирты, третичный бутиловый спирт смешивается с водой и нейтральными растворителями, в то время как другие три бутиловых спирта, как высшие члены ряда, являются более растворимыми в нейтральных растворителях, чем в воде. (Рис. 236) Указанная характеристика, применявшаяся с целью систематизации полярно-неполярных веществ, оказывается, определяет активность алифатических спиртов по отношению к рН раны второго дня. Мы вновь должны указать на прямой характер указанной активности, однако, она влияет на определенные метаболические процессы, поскольку при прямом эффекте активный спирт вызывает скорее местное окисление, чем ощелачивание.
Другим фактором, вероятно влияющим на активность указанного ряда спиртов, является длина углеродной цепи. В то время как гептанол вызывает характерное окисляющее действие, октиловый спирт оказывает его лишь у некоторых животных. Нониловый и дециловый спирты оказались неактивными.
Вероятность существования биологической соревновательности между указанными агентами и жирными кислотами обусловила необходимость проведения исследования других спиртов, способных комбинироваться с жирными кислотами, особенно in vivo. Мы изучили глицерин, глицерофосфорный ион и стерины, которые часто обнаруживаются связанными с жирными кислотами. Мы добавили к этой группе глюкозу из-за ее метаболической связи с производными глицерина, хотя это, очевидно, не связано с жирными кислотами.
Интересно отметить, что глицерин оказывал лишь минимальное влияние на непосредственное значение pH. Самые высокие значения были все еще в пределах нормы. Окисляющий эффект глицерина на рН раны второго дня, вероятно, был обусловлен индивидуальными вариациями, но также при значениях величины, близких к нижней границе нормы, например при 7.72. Глюкоза обнаруживала слабый окисляющее действие, в то время как холестерин обнаруживал определенную окисляющую активность на рН раны второго дня, так же как и препараты неомыляемой фракции разных органов или тканей. Ацидификация, производимая препаратами неомыляемой фракции, более интенсивна, чем одного холестерина, что указывает на другие составляющие части этих препаратов, также имеющие окисляющее влияние.

Рис. 236. Величины рН в поверхностной пленке раны второго дня для разных спиртов обнаруживают связь между активностью и липоидическим свойством. Все спирты ниже бутанола и третичного бутанола, не являющиеся липоидами, неактивны. Указанное выше, также справедливо для спиртов с цепями, содержащими более восьми атомов углерода.
Другие агенты
Мы исследовали некоторые гормоны, часто применяемые клинически, и обнаружили, что биологический антагонизм между половыми гормонами мужчины и женщины также заметен по их влиянию на pH второго дня, причем мужской гормон обладает ощелачивающим эффектом, а женский - окисляющим. Здесь мы должны отметить, что окисляющий эффект также очевиден для прогестерона.
Указанный эффект противоположен таковому мужского гормона и идентичен в этом плане стильбэстролу, что выглядит неожиданно. Здесь отмечается такой же антагонизм между дезоксикортикостеролом и супраренином, поскольку первый является окисляющим, а последний - слегка ощелачивающим средством. Антианемический экстракт печени также обладает ощелачивающим действием.
Исследовались также некоторые витамины. Мы установили, что, в то время как витамины B1, В2, Е и К обладают окисляющим действием, то витамины A, D и B6 - ощелачивающим. Аскорбиновая кислота, вероятно, не влияет на рН струпа раны второго дня.
Был изучен ряд алкалоидов и гликозидов, имеющих важную фармакодинамическую активность. Два опиумных алкалоида и идентичное синтетическое средство обладают умеренно окисляющим действием. Атропин, кофеин и хинин обладают слабым ощелачивающим эффектом. Разные эффекты дигиталина и сапонина были неожиданны; оба обнаружили слабое, но противоположное по направленности, действие, первый – закисляющее, а второй - ощелачивающее.
Были изучены наркотики и гипнотические средства, из-за их воздействия на центральную нервную систему. В то время как эфир и хлороформ являются слегка ощелачивающими, два протестированных барбитурата обнаружили окисляющий эффект. Интересно, что опиумные алкалоиды и демерол тоже индуцируют закисление, хотя и в меньшей степени, чем барбитураты.
Были также изучены разные иные агенты. Среди пиретогеников и антипиретиков существует очевидный антагонизм в отношении влияния на рН струпа раны второго дня. В то время как пиретогеник метиленовый синий индуцирует явное закисление, три исследованных антипиретика дают ощелачивание. Однако ацетилсалициловая кислота не следует приведеному правилу—ей свойственен закисляющий эффект.
Среди противомикробных агентов одинаковое, в изучаемом аспекте, действие очевидно для трех антибиотиков грибковой природы и двух сульфаниламидов. Все они, как антипиретики, оказывают ощелачивающее действие. Закисляющий эффект бензедрина не согласуется с таковым у веществ, обладающих гипнотической и успокаивающей активностью. Подобное несоответствие в фармакологической активности и воздействии на рН струпа раны второго дня свидетельствует о том, что на второй из показателей во многих случаях оказывается вторичное влияние со стороны интерстициального уровня.
Антагонистическая биологическая активность отмечена у антианемического печеночного экстракта и препарата железа. Действие первого, благотворно влияющего при гиперхромной анемии, а второго - на гипохромные формы, проявляется в их противоположном воздействии на pH струпа раны второго дня. Антианемический экстракт печени индуцирует ощелачивание, в то время как железо вызывает закисление. Tакой же антагонизм наблюдается у двух агентов, которым свойственно противоположное воздействие на свертывание крови. В то время как витамин К вызывает закисление, дикумарол является ощелачивающим средством. Хотя рутин влияет на другие факторы, когда оказывает действие при кровотечении, он влияет на pH струпа раны второго дня идентично витамину К.
Аминофиллин вызывает закисление, в противоположность кофеину, дающему слабое ощелачивание. С другой стороны, закисление вызывают как прокаин, так и алкалоиды опия и барбитураты.
Это может быть связано с влиянием высших спиртов, обладающих также наркотической активностью. Они, как уже сообщалось выше, вызывают закисление.
таблица XXVII демонстрирует эффекты в отношении pH струпа раны второго дня всех исследованных веществ.
таблица XXVII ВЛИЯНИЕ РАЗНЫХ ВЕЩЕСТВ НА pH струпа раны второго дня.
| Поднимают | Уменьшают | Не оказывают эффекта | |
| Витамины | A, D, B6 | B1, В2, К, Е | С |
| Гормоны | Тестостерон, адреналин | Стильбэстрол, прогестерон, дезоксикортикостерон | |
| Алкалоиды | Атропин, хинин | Кодеин, морфин | |
| Антибиотики | Пенициллин, стрептомицин, ауреомицин | ||
| Сульфониламиды | Сульфатиозол, сульфомеразин | ||
| Антипиретики и аналгетики | Ацетофенетидин, аминопирин, антипирин | Ацетил – салициловая кислота | |
| Наркотики | Хлороформ | Фенобарбитал, пентобарбитал | |
| Антианемические средства | Экстракт печени | Железо (уменьшено) | |
| Ксантины | Кафеин | Аминофиллин | |
| Разные | Дикумерол, бензен, толуол, сапонин, птерилглютаминовая кислота тероптерин | Прокаин, бенадрил, корамин, глюкоза, глицерин, глюконат натрия, рутин, метиленовый синий, меркугидрин, бензедрин, демерол |
Основываясь на полученных результатах, касающихся разных групп агентов, метод определения pH струпа раны второго дня оказался интересным средством изучения фармакологической активности. Следует отметить, что ни одно из упомянутых веществ, по крайней мере, в этих дозах, не оказало
никакого влияния на рН неизмененных тканей, судя по замерам рН, полученным непосредственно после нанесения ран. Поскольку наше исследование касается только неизмененных тканей, следовало бы измерить pH струпа раны второго дня. Тем не менее, интегрируя полученные значения pH в общую картину этих дисбалансов, не следует забывать, что они представляют изменения в интерстициальных жидкостях, которые соответствуют вторичной части тканевого уровня.

Рис. 238. Воздействие растущей пересаженной опухоли Уолкера на рН струпа раны второго дня в хирургических ранах, нанесенных серийно в день пересадки и каждые три дня затем. У животных отмечено заметное уменьшение рН струпа раны второго дня.
ФИЗИЧЕСКИЕ АГЕНТЫ
Животные, содержавшиеся в инкубаторе при температуре 38° С, демонстрировали определенную тенденцию в направлении снижения pH струпа раны второго дня. Воздействие холода на животных, содержавшихся в рефрижераторе на протяжении 48 часов перед операцией, было менее явным.
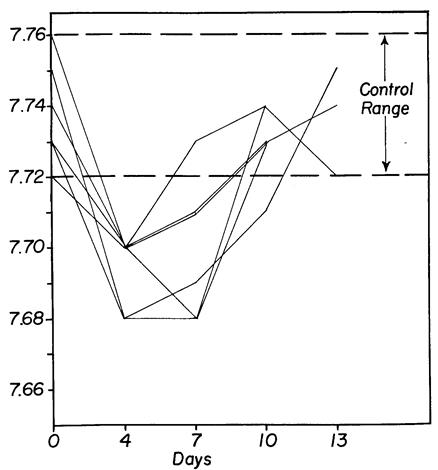
Рис. 239. Последовательные изменения рН струпа раны второго дня у животных с пересаженными опухолями, которые быстро поддались регрессу, или не смогли вырасти. Легкое падение значений наблюдалось на четвертый и седьмой день после операции трансплантации с возвращением к контрольным значениям у всех животных к десятому дню.
БИОЛОГИЧЕСКИЕ ФАКТОРЫ
Пересаженные опухоли. Было проведено предварительное исследование воздействия пересаженной опухоли Walker на pH струпа раны второго дня экспериментальной раны. Перед выполнением трансплантации был проведен контроль pH струпа раны второго дня для каждого животного. Затем опухоли были пересажены подкожно на левый фланк троакарным методом. После проведения пересадки опухоли животным, наносились операционные раны с интервалами в три дня. Ряд замеров величины pH струпа раны второго дня получали на четвертый, седьмой, десятый и тринадцатый дни после трансплантации. Величины pH, определявшиеся всякий раз после нанесения раны, не отличались от величин, обнаруженных у нелеченых животных контрольной группы. Как и у всех других животных, только pH струпа раны второго дня обнаруживал значительные изменения.

Рис. 240. Изменения pH струпа раны второго дня у двух крыс с растущими опухолями Walker (——), из которых опухоль была извлечена на седьмой день после трансплантации. Вслед за удалением опухолей pH струпа раны второго дня начал возвращаться к норме. Идентично большой разрез выполняли и двум животным без опухолей. У них не установлено никакого влияния на pH струпа раны второго дня (....).
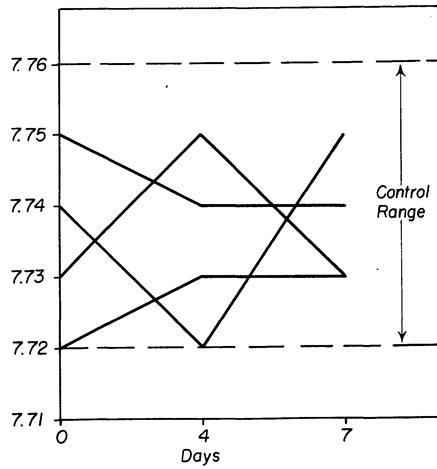
Рис. 241. Последовательный ряд замеров pH струпа раны второго дня у крыс без пересаженных опухолей. Ряд малых хирургических вмешательств не смещали величины pH струпа раны второго дня в сторону от контрольных значений.
РИС. 238 графически иллюстрирует изменения pH струпа раны второго дня в группе из 12 животных с успешной пересадкой опухолей. У каждого животного наблюдалось устойчивое снижение pH струпа раны второго дня <
Дата добавления: 2021-02-19; просмотров: 492;











