Зависимость массовой скорости горения от тепло-и массопереноса (уравнение Зельдовича)
В процессе горения зарядов конденсированных ВС следует различать три основных процесса:
- зажигание от источника воспламенения с торца заряда;
- послойное горение;
- воспламенение заряда с боковой поверхности (при отсутствии бронировки боковой поверхности).
Теоретически описать такой сложный гетерогенный процесс, как горение, весьма трудно. Но если сделать ряд допущений:
- реакция целиком протекает при максимальной температуре горения,
- вещество сначала полностью испаряется, а затем идут реакции в парах и т.д., то процесс поддается описанию.
Согласно теории нормального горения скорость распространения зоны химической реакции обуславливается совокупностью двух процессов:
● переносом тепла из зоны химической реакции в зону прогрева за счет теплопроводности и
● массопереносом вещества из зоны прогрева в зону химической реакции за счет диффузии.
При совместном решении уравнений теплопроводности и диффузии получили выражение массовой скорости горения:
Um = 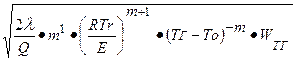
λ – коэффициент теплопроводности;
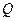 – тепловой эффект реакции окисления (с единицы массы газа);
– тепловой эффект реакции окисления (с единицы массы газа);
m – порядок реакции;
Tr – температура горения;
Е – энергия активации;
Т0 – начальная температура;
WTГ – скорость реакции при Т горения.
WTГ=ρо·z·exp(-E/RTг).
 |
Важнейшей характеристикой порохов и ракетных топлив является закон горения – зависимость скорости горения от давления. Эту зависимость можно представить в виде эмпирического уравнения:
U = a + в × рν
где а, в и ν – эмпирические коэффициенты.ν
Закон горения определяют экспериментальным путем для определенного диапазона давлений. При других давлениях он может изменяться. Для порохов и ТРТ важнейшим параметром является показатель степени ν. При устойчивом горении 0≤ν≤1. Если ν›1, то горение происходит с ускорением и может перейти в детонацию. Коэффициент «а» в значительной мере зависит от процессов, протекающих в конденсированной фазе, коэффициент «в» – в газовой.
Для большинства летучих ВВ (нитроглицерин, ТЭН) процессы идущие в концентрированной фазе не играют существенной роли, и закон горения имеет вид:
U=в × рν
Это объясняется тем, что теплота испарения летучих ВВ значительно уступает энергии активации процесса. Но при высоких давлениях, процесс превращения может перейти в конденсированную фазу.
Для нелетучих ВМ (бездымные пороха) в конденсированной фазе происходит разложение веществ до промежуточных газообразных продуктов (газификация) которые потом воспламеняются.
Пороха и ТРТ по своей химической природе представляют собой смесевые взрывчатые системы, которые горят более устойчиво при повышенных давлениях и температурах, чем их компоненты в отдельности. БВВ имеют малые коэффициенты ускорения процесса горения и с этой точки зрения переход горения в детонацию у них затруднен. Однако они имеют пористую структуру или находятся в жидком состоянии, что способствует возникновению дополнительного ускорения массовой скорости горения за счет увеличения его эффективной поверхности горения. Из-за этого горение может стать неустойчивым и перейти в детонацию. Однако не всякое непористое твердое БВВ может использоваться как порох.
Кристаллические БВВ, отличающиеся малой механической прочностью, при разрушении кристаллов также приведут к резкому увеличению поверхности горения и переходу горения в детонацию. Поэтому пороха должны изготовляться из механически прочных, аморфных, часто высокополимерных БВВ, которые сохраняют форму и поверхность горения при воздействии высоких давлений и перепадов температур.
Дата добавления: 2016-11-04; просмотров: 2438;











