XV. ПЕРЕГОНКА ЖИДКОСТЕЙ
1. Общие сведения
2. Простая перегонка
3. Ректификация
Схемы ректификационных установок для разделения бинарных смесей
Устройство ректификационных аппаратов
4. Специальные виды перегонки
4.1. Экстрактивная ректификация
4.2. Азеотропная ректификация
Молекулярная дистилляция
Низкотемпературная ректификация
.
Общие сведения
Одним из наиболее распространенных методов разделения жидких однородных смесей, состоящих из двух или большего числа летучих компонентов, является перегонка (дистилляция и ректификация).
В широком смысле перегонка представляет собой процесс, включающий частичное испарение разделяемой смеси и последующую конденсацию образующихся паров, осуществляемые однократно или многократно. В результате конденсации получают жидкость, состав которой отличается от состава исходной смеси.
Если бы исходная смесь состояла из летучего или нелетучего компонентов, то ее можно было бы разделить на компоненты путем выпаривания. Посредством же перегонки разделяют смеси, все компоненты которых летучи, т.е. обладают определенным, хотя и разным давлением пара. Разделение перегонкой основано на различной летучести компонентов смеси при одной и той же температуре. Поэтому при перегонке все компоненты смеси переходят в парообразное состояние в количествах, пропорциональных их фугитивности (летучести).
В простейшем случае исходная смесь является бинарной, т.е. состоит только из двух компонентов. Получаемый при ее перегонке пар содержит относительно большее количество легколетучего, или низкокипящего, компонента (НК), чем исходная смесь. Следовательно, в процессе перегонки жидкая фаза обедняется, а паровая фаза обогащается НК. Неиспарившаяся жидкость, естественно, имеет состав, более богатый труднолетучим, или высококипящим компонентом (ВК).
Эта жидкость называется остатком, а жидкость, полученная в результате конденсации паров,— дистиллятом, или ректификатом.
Степень обогащения паровой фазы НК при прочих равных условиях зависит от вида перегонки. Существуют два принципиально отличных вида перегонки: 1) простая перегонка (дистилляция) и 2) ректификация.
Простая перегонка представляет собой процесс однократного частичного испарения жидкой смеси и конденсации образующихся паров. Простая перегонка применима только для разделения смесей, летучести компонентов которой существенно различны, т.е. отношение летучестей (относительная летучесть) компонентов значительна. Обычно ее используют лишь для предварительного грубого разделения жидких смесей, а также для очистки сложных смесей от нежелательных примесей, смол и т.п. Известны несколько разновидностей простой перегонки, которые будут рассмотрены ниже.
Значительно более полное разделение жидких смесей на компоненты достигается путем ректификации.
Ректификация — процесс разделения гомогенных смесей летучих жидкостей путем двустороннего массо- и теплообмена между неравновесными жидкой и паровой фазами, имеющими различную температуру и движущимися относительно друг друга. Разделение осуществляется обычно в колонных аппаратах при многократном или непрерывном контакте фаз. При каждом контакте из жидкости испаряется преимущественно НК, которым обогащаются пары, а из паровой фазы конденсируется преимущественно ВК, переходящий в жидкость. Обмен компонентами между фазами позволяет получить, в конечном счете, пары, представляющие собой почти чистый НК. Эти пары, выходящие из верхней части колонны, после их конденсации в отдельном аппарате дают дистиллят, или ректификат (верхний продукт) и флегму — жидкость, возвращаемую для орошения колонны и взаимодействия с поднимающимися по колонне парами. Снизу колонны удаляется жидкость, представляющая собой почти чистый ВК, — остаток (нижний продукт). Часть остатка испаряют в нижней части колонны для получения восходящего потока пара.
Ректификация известна с начала XIX века как один из важнейших технологических процессов главным образом спиртовой и нефтяной промышленности. В настоящее время ректификацию все шире применяют в самых различных областях химической технологии, где выделение компонентов в чистом виде имеет весьма важное значение (в производствах органического синтеза, изотопов, полимеров, полупроводников и различных других веществ высокой чистоты).
Процессы перегонки осуществляются периодически или непрерывно. Ниже рассмотрены характеристики двухфазных систем жидкость—пар, необходимые для анализа и расчета процессов перегонки.
Простая перегонка
 Фракционная перегонка. Перегонку проводят путем постепенного испарения жидкости, находящейся в перегонном кубе. Образующиеся пары отводятся и конденсируются. Процесс осуществляют периодическим или непрерывным способом.
Фракционная перегонка. Перегонку проводят путем постепенного испарения жидкости, находящейся в перегонном кубе. Образующиеся пары отводятся и конденсируются. Процесс осуществляют периодическим или непрерывным способом.
Если простая перегонка проводится периодически, то в ходе отгонки НК содержание его в кубовой жидкости уменьшается. Вместе с тем, изменяется во времени и состав дистиллята, который обедняется НК по мере протекания процесса. В связи с этим отбирают несколько фракций дистиллята, имеющих различный состав. Простая перегонка, проводимая с получением конечного продукта разного состава, называется фракционной, или дробной, перегонкой.
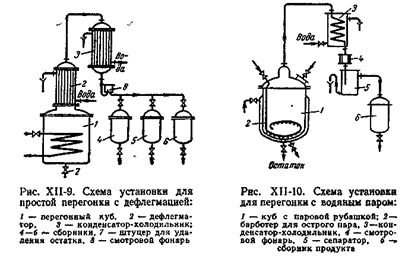
В периодически действующей установке для фракционной перегонки (рис. XV-1) исходную смесь загружают в перегонный куб 1, снабженный змеевиком для обогрева, и доводят до кипения. Пары отводят в конденсатор-холодильник 2. Фракции дистиллята поступают через смотровой фонарь 3 в отдельные сборники 4-6. По окончании операции остаток сливают из куба, после чего в него вновь загружают разделяемую смесь.
Для составления материального баланса простой перегонки примем, что в кубе в некоторый момент времени t содержится L кг перегоняемой смеси, имеющей текущую концентрацию х (по низкокипящему компоненту). Масса НК в жидкости в этот момент равна Lх.
Пусть за бесконечно малый промежуток времени dt испарится dL кг смеси и концентрация жидкости в кубе уменьшится на величину dx. При этом образуются dL кг пара, равновесного с жидкостью и имеющего концентрацию у*; количество НК в паре будет равно dLy*. Соответственно остаток жидкости в кубе составит (L-dL), кг, а ее концентрация будет (х-dx). Тогда материальный баланс по НК выразится уравнением
Lx = (L – dL)(x – dx) + dLy*
Раскрывая скобки и пренебрегая произведением dLdx, как бесконечно малой величиной второго порядка, после разделения переменных получим
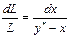
Это дифференциальное уравнение должно быть проинтегрировано в пределах изменения массы жидкости в кубе от начальной L = F до конечной L = W (где F — масса исходной смеси, или литания, и W — масса остатка) и соответствующего падения ее концентрации от хр до xW за всю операцию перегонки:
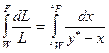
В результате интегрирования получим
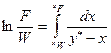 (XV,1)
(XV,1)
Вид функции у* = f(х) определяется формой кривой равновесия и не может быть установлен аналитически для каждого конкретного случая перегонки. Поэтому интегрирование правой части уравнения (ХII,1) проводят графически — путем построения зависимости 1/(у*—х) от х.
Для ряда значений х в пределах от xF до xw находят из диаграммы у—х равновесные им значения у* и по размеру площади под кривой, ограниченной абсциссами xF и xw, определяют (с учетом масштабов диаграммы) значение искомого интеграла.
По уравнению (XV,1), зная массы F загруженной в куб смеси и ее состав xF, а также заданный состав остатка xW, находят массу остатка W. Масса перегнанной жидкости составляет F—W.
Средний состав (хр)ср, получаемого дистиллята рассчитывают из уравнения материального баланса по низкокипящему компоненту:
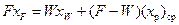
откуда
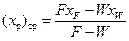 (XV,2)
(XV,2)
Расчет простой перегонки обычно имеет целью определить массу жидкости, которую необходимо перегнать, для того чтобы получить в кубе остаток заданного состава и дистиллят требуемого среднего состава.
Простую перегонку проводят при атмосферном давлении или под вакуумом, присоединяя сборники дистиллята к источнику вакуума. Применение вакуума дает возможность разделять термически малостойкие смеси и, вследствие испарения температуры кипения раствора, использовать для обогрева куба пар более низких параметров.
Простая перегонка с дефлегмацией. Для повышения степени разделения смеси перегонку осуществляют, дополнительно обогащая дистиллят путем дефлегмации. Пары из перегонного куба 1 (рис. ХV-2) поступают в дефлегматор 2, где они частично конденсируются. Из пара конденсируется преимущественно ВК и получаемая жидкость (флегма) сливается в куб. Пары, обогащенные НК, направляются в конденсатор-холодильник 3, где полностью конденсируются. Дистиллят собирается в сборниках 4—6. Окончание операции контролируют по температуре кипения жидкости в кубе, которая должна соответствовать заданному составу остатка. Последний удаляется из куба через штуцер 7.
Перегонка в токе носителя. Понижение температуры кипения разделяемой смеси может быть достигнуто не только при перегонке под вакуумом, но также путем введения, в эту смесь дополнительного компонент-носителя (водяного пара или инертного газа).
Перегонка с водяным паром. Если компоненты исходной смеси нерастворимы в воде, то ее используют в качестве дополнительного компонента, который вводят в куб обычно в виде острого пара.
При перегонке высококипящих веществ, нерастворимых в воде, с водяным паром температура кипения смеси должна быть ниже температуры кипения воды при данном давлении. Таким образом, при давлении, равном 1 атм, температура перегонки будет ниже 100 оС.
Этим способом обычно разделяют (или очищают от примесей) смеси веществ, кипящих при температурах, превышающих 100 °С, что и обусловливает необходимость подачи воды в куб в виде острого перегретого пара (рис. ХV-3).
Исходная смесь загружается в куб 1, обогреваемый глухим паром через рубашку. Внутрь куба через барботер 2 подается острый пар. Пары, образующиеся при испарении смеси, направляются в конденсатор-холодильник 3. Образующийся здесь конденсат через смотровой фонарь 4 поступает на разделение в сепаратор 5. Снизу сепаратора через гидравлический затвор удаляется, например вода, а сверху — отогнанный, не растворимый в воде более легкий компонент, который сливается в сборник 6.
Практически перегонка с водяным паром протекает в неравновесных условиях. В данном процессе острый пар играет двоякую роль — теплоносителя – агента, снижающего температуру кипения. Поэтому пар надо вводить в количестве, большем его теоретического расхода на процесс собственно отгонки выделенного вещества.
|
|
Процесс можно рассматривать как перегонку в токе носителя — водяного пара, которая может проводиться периодически (как показано на рис. XV-3) или непрерывно. Общий расход тепла при перегонке с водяным паром больше, чем при простой перегонке на количество тепла, удаляющееся с носителем (водяным паром).
Перегонка с инертным газом. При перегонке смесей вместо водяного пара иногда используют инертные газы, например азот, двуокись углерода и др. Перегонка в токе неконденсирующегося инертного газа позволяет более значительно снизить температуру испарения разделяемой смеси, чем при перегонке в токе водяного пара, где это снижение ограничено температурой его конденсации. Вместе с тем, присутствие инертного газа в парах, поднимающихся из куба, приводит к резкому уменьшению коэффициента теплоотдачи в конденсаторе-холодильнике и соответственно — к значительному возрастанию поверхности теплообмена. Кроме того, конденсация парогазовых смесей часто сопровождается туманообразованием. Это весьма затрудняет разделение смесей и вызывает заметный унос конечного продукта с инертным газом.
Теоретический расход водяного пара или инертного газа может быть найден из соотношения (XV,3). Обычно пар полностью не насыщается извлекаемым компонентом. Поэтому, учитывая степень насыщения пара (газа), которая определяется коэффициентом насыщения j = 0.5-0.9, расход носителя рассчитывают по уравнению
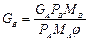 (XV,3)
(XV,3)
где все обозначения величин те же, что и в уравнении (XV,2).
Уравнением (XV, 3) не учитывается расход носителя, который требуется для нагревания смеси до температуры перегонки, испарения смеси и компенсации потерь тепла в окружающую среду. Чтобы избежать чрезмерно большого расхода носителя и разбавления им паров, тепло для указанных выше целей подводят в куб с помощью глухого пара или другого теплоносителя.
|
|
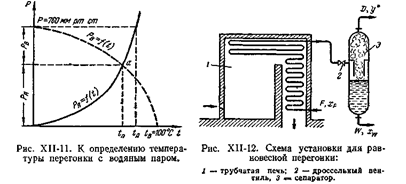
Температуру перегонки с инертным газом или водяным паром можно определить, пользуясь графиком зависимости давления паров чистых компонентов от температуры (рис ХV-4). Нанося на график кривую давления паров РB = f (t) носителя (например, водяного пара) «обращение», т.е. не от нуля, а от давления, равного атмосферному, вниз, и находят точку а пересечения кривых давлений насыщенных паров носителя и соответствующей жидкости. Абсцисса точки пересечения указывает искомую температуру перегонки tn.
Равновесная перегонка. Этот вид перегонки применяется, например в нефтеперерабатывающей и нефтехимической промышленности в основном для предварительного (перед ректификацией) разделения сложных смесей, содержащих летучие компоненты.
Исходная смесь нагревается и однократно испаряется в трубчатой печи 1, показанной на рис. XV-5 (D — количество пара) (остальные обозначения — прежние). До конца процесса пары длительно соприкасаются с неиспарившейся жидкостью и приходят в равновесие с ней. После достижения конечной температуры смесь пара и жидкости через дроссельный вентиль 2 направляется в сепаратор 3, где образовавшиеся пары отделяются от неиспарившейся жидкости. В таком процессе не достигается четкого разделения смеси. Поэтому получаемые продукты обычно подвергаются последующей ректификации.
Молекулярная перегонка. Для извлечения дорогостоящих компонентов из смесей, где они содержатся в небольших количествах, или для тщательной очистки термически нестойких смесей от примесей используют молекулярную перегонку, проводимую в условиях глубокого вакуума. Этот процесс отличается специфическими особенностями, требует применения специальной аппаратуры.
Ректификация
 Принцип ректификации. Как отмечалось, достаточно высокая степень разделения однородных жидких смесей на компоненты может быть достигнута путем ректификации. Сущность процессов, из которых складывается ректификация, и получаемые при этом результаты можно проследить с помощью t—х—y-диаграммы (рис. ХV-6).
Принцип ректификации. Как отмечалось, достаточно высокая степень разделения однородных жидких смесей на компоненты может быть достигнута путем ректификации. Сущность процессов, из которых складывается ректификация, и получаемые при этом результаты можно проследить с помощью t—х—y-диаграммы (рис. ХV-6).
Нагрев исходную смесь состава х1 до температуры кипения, получим находящийся в равновесии с жидкостью пар (точка b). Отбор и конденсация этого пара дают жидкость состава x2, обогащенную НК (х2 >х1). Нагрев эту жидкость до температуры кипени t2, получим пар (точка d), конденсация которого дает жидкость с еще большим содержанием НК, имеющую состав х3, и т.д. Проводя таким образом последовательно ряд процессов испарения жидкости и конденсации паров, можно получить в итоге жидкость (дистиллят), представляющую собой практически чистый НК.
Аналогично, исходя из паровой фазы, соответствующей составу жидкости x4, путем проведения ряда последовательных процессов конденсации и испарения можно получить жидкость (остаток), состоящую почти целиком из ВК.
В простейшем виде процесс многократного испарения можно осуществить в многоступенчатой установке, в первой ступени которой испаряется исходная смесь. На вторую ступень поступает на испарение жидкость, оставшаяся после отделения паров в первой ступени, в третьей ступени испаряется жидкость, поступившая из второй ступени (после отбора из последней паров), и т.д. Аналогично может быть организован процесс многократной конденсации, при котором на каждую следующую ступень поступают для конденсации пары, оставшиеся после отделения от них жидкости (конденсата) в предыдущей ступени.
При достаточно большом числе ступеней таким путем можно получить жидкую или паровую фазу с достаточно высокой концентрацией компонента, которым она обогащается. Однако выход этой фазы будет мал по отношению к ее количеству в исходной смеси. Кроме того, описанные установки отличаются громоздкостью и большими потерями тепла в окружающую среду.
Значительно более экономичное, полное и четкое разделение смесей на компоненты достигается в процессах ректификации, проводимых обычно в более компактных аппаратах — ректификационных колоннах.
Процессы ректификации осуществляются периодически или непрерывно при различных давлениях: при атмосферном давлении, под вакуумом (для разделения смесей высококипящих веществ), а также под давлением больше атмосферного (для разделения смесей, являющихся газообразными при нормальных температурах).
Дата добавления: 2016-10-18; просмотров: 12077;











