Заряд белковой молекулы
Появление заряда на молекулах белков связано с их амфотерными свойствами (наличием кислотных и основных свойств). Группы, способные приобретать заряды, называются ионогенными. К ним относятся СООН - группы глютамата, аспартата, СООН - группы С-концевых аминокислот, NH2 - группы лизина, аргинина, α- NH2. - группы N-концевых аминокислот, азот имидазольного кольца гистидина. В очень незначительной степени ионизируются –SH группы цистеина и –OH группы тирозина. Ионизация различных функциональных групп белка групп определяется величиной рН среды.
Ионизация кислотных групп (СООН - группы – доноры Н+).
При рН = 2-4 половина карбоксильных групп в белках находится в ионизированном состоянии (–СОО-), половина – в неионизированном виде(–СООН). При физиологических значениях рН в интервале 7,35 – 7,45 (более щелочная среда) карбоксильные группы полностью ионизированы и определяют отрицательный заряд белковой молекулы.

Ионизация щелочных групп (NH2 -группы - акцепторы Н+)
При рН около 10 половина аминогрупп белков ионизирована, а половина не ионизирована. При физиологических величинах рН =7.4 (более кислая среда) преобладает ионизированная форма аминогрупп (NH3+), придающая белковым молекулам положительный заряд.

Кислотно-основные свойства белков и аминокислот изучают методом потенциометрического титрования. Изменение ионизации белка при разных значениях рН имеет вид графика, приведенного ниже.
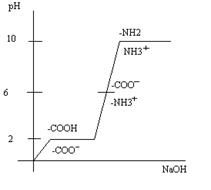
Из всех аминокислот только гистидин обладает буферными свойствами при рН = 6-7. Входя в состав белка гемоглобина, гистидин определяет его буферные свойства, необходимые для связывания кислорода.
Изменениями величины рН среды белок можно перевести в особое изоэлектрическое (электронейстральное) состояние, в котором сумма положительных зарядов равна сумме отрицательных зарядов, а молекула в целом электронейтральна
(+Н3N - белок - СОО-). Значение рН, при котором молекула белка электронейтральна, называется изоэлектрической точкой (ИЭТ). Для большинства белков изоэлектрическая точка находится в кислой среде (рН = 5-5,5). В то же время для гистонов ИЭТ находится в щелочной среде (рН= 9-11). В изоэлектрическом состоянии белки менее устойчивы, чем при наличии зарядов, поскольку одинаковый по знаку заряд белковой молекулы является фактором электростатического отталкивания белковых молекул, определяет ионные связи в белках и формирует наиболее стабильную конформацию белковой молекулы.
Дата добавления: 2016-09-26; просмотров: 3356;











