Понятие о процессах плавления и кристаллизации. Условие кристаллизации. Термические кривые.
Кристаллизацией называют переход металла из жидкого состояния в твердое (кристаллическое). Известно, что все вещества могут находиться в твердом, жидком, газообразном состояниях. При определенных температурах происходит изменение агрегатного состояния чистых металлов. При нагреве выше температуры плавления (Тпл). Твердое состояние сменяется жидким, а при нагреве выше температуры кипения (Тк) жидкое состояние сменяется газообразным.
Главным признаком твердого состояния является кристаллическое строение. Жидкий расплав характеризуется хаотическим тепловым движением атомов и молекул металла.
Процесс плавления металла заключается в разрушении кристаллического строения при достижении Тпл.
Затрачиваемая на разрушение кристаллических решеток энергия является для каждого металла величиной постоянной и характеризуется теплотой плавления.
Тпл для различных металлов находится в пределах от –38,9 (Hg) до +3410 °С (W).
Кристаллизация протекает в условиях, когда система переходит к термодинамически более устойчивому состоянию с меньшей свободной энергией Z, т.е. когда Zкр < Zж.
Свободная энергия определяется Z=U-TS, где
U – полная внутренняя энергия системы
T – абсолютная температура
S – энтропия
Свободной энергией (термодинамическим потенциалом) называют ту составляющую полной энергии вещества, которая обратимо изменяет свою величину с изменением температуры. С повышением температуры Z уменьшается.
Изменение свободной энергии Z жидкого и твердого состояния в зависимости от температуры показано на рисунке:
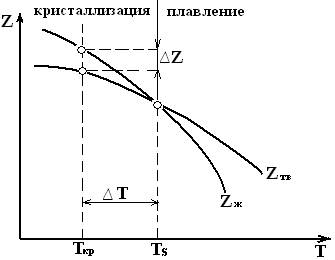
Выше Ts более устойчив жидкий металл, имеющий меньший запас свободной энергии, ниже Ts – устойчив твердый металл. При Ts Zж=Zтв. При этой температуре жидкая и твердая фазы могут существовать бесконечно долго. Отклонение в ту или иную сторону является термодинамическим стимулом для плавления или кристаллизации.
Процесс кристаллизации развивается, когда созданы условия для возникновения разности свободных энергий, образующейся вследствие меньшей свободной энергии твердого металла по сравнению и жидким.
Таким образом, процесс кристаллизации может протекать только при переохлаждении металла ниже равновесной температуры Ts
Разность между Ts и Ткр, ∆ Т=Ts – Ткр называется степенью переохлаждения.
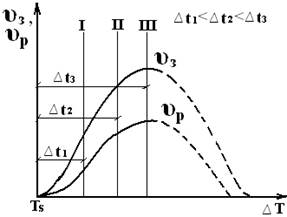
Изобразим термические кривые, характеризующие процесс кристаллизации металла при разных скоростях охлаждения:
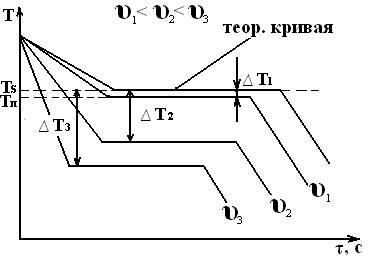
При очень медленном охлаждении ∆Т невелика и кристаллизация протекает при температуре, близкой к равновесной. С увеличением υохл ∆Т возрастает. Для полного переохлаждения металла в жидком состоянии требуются большие скорости охлаждения (миллионы и даже миллиарды °/с). Охлаждение жидкого металла до комнатной температуры следует проводить так, чтобы получить переохлажденный жидкий металл (т.е. не имеющий кристаллического строения) за ничтожную долю секунд. Такой металл называется аморфным или металлическим стеклом. Начинает применяться на практике. Степень переохлаждения зависит от природы и чистоты металла. Чем чище металл, тем более склонен он к переохлаждению, например, при затвердевании Sn была достигнута ∆Т=1180С, но скачок указывает на то, что в результате переохлаждения образуется большое число центров кристаллизации, рост кристаллов происходит так бурно, что температура скачкообразно повышается, чаще степень переохлаждения не более 10-30оС.
Скачок на кривой охлаждения указывает на то, что в результате большего переохлаждения образуется большее число центров кристаллизации, рост кристаллов происходит так бурно, что температура скачкообразно повышается почти до температуры плавления. Это характерно для Sb, температура переохлаждения 631 – 590 = 41 °С.
На перевод жидкого металла в газообразное состояние также затрачивается энергия, характеризующаяся температурой кипения (Ткип).
2. Процесс зарождения и роста кристаллов.
Итак, кристаллизация – это процесс образования кристаллов. Различают первичную и вторичную кристаллизацию. Первичная – образование кристаллов из жидкости в процессе затвердевания металла, вторичная – изменение кристаллического строения в твердом состоянии.
Кристаллизация, как впервые установил Д. К. Чернов, происходит не мгновенно по всему объему, а развивается постепенно. Она объединяет 2 элементарных процесса: возникновение центров кристаллизации (зародышей) и рост кристаллов из центров кристаллизации.
Центрами кристаллизации являются либо затвердевшие мельчайшие частицы металла, либо посторонние твердые примеси, находящиеся в жидком металле. По мере протекания процесса кристаллизации происходит как зарождение новых центров кристаллизации, так и рост кристаллов.
Пока образовавшиеся кристаллы растут свободно и окружены жидкостью, они имеют правильную форму. Однако при столкновении и сростании кристаллов их форма нарушается.
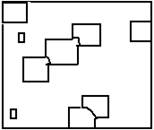
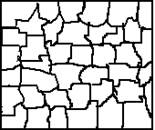
После затвердевания металла получаются кристаллы неправильной формы, границы которых чаще всего принимают округлые очертания. Такие кристаллы называют зернами или кристаллитами. Внутри каждого зерна наблюдается определенная ориентация кристаллической решетки, отличная от ориентации соседних зерен.
3. Строение слитков.
В зависимости от условий роста, главным образом от скорости направления отвода теплоты, температуры жидкого металла, форма зерен может быть самой разнообразной.
При кристаллизации металлов и их сплавов рост зерен осуществляется по дендритной (древовидной) схеме. Рост дендрита происходит путем образования осей 1 порядка (стволов), перпендикулярно к которыым вырастают ветвиП порядка, перпендикулярно к ним ветви 3-го порядка и т.д. Большая скорость роста кристаллов наблюдается по таким плоскостям и направлениям решетки, которые имеют наибольшую плотность упаковки атомов, в результате чего и вырастают оси 1 порядка. Одновремено с ростом ветвей П и т.д.порядков идет кристаллизация между осями дендритов.
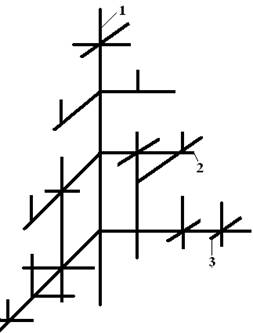

После соприкосновения дендритов и окончательного заполнения межосного пространства, дендриты превращаются в полновесные кристаллиты.
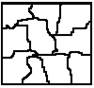
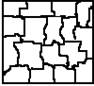
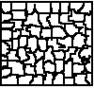
Кристаллизация слитка идет в три стадии. Схема:
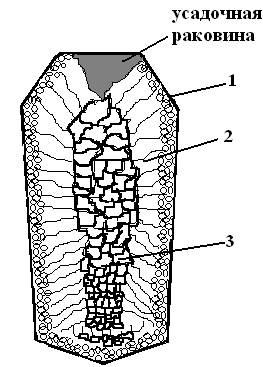
Как видно, условия отвода тепла при кристаллизации значительно влияют на форму зерен. Сначала на поверхности слитка образуется зона 1 – мелкозернистая корка, состоящая из разнообразно ориентированных мелких дендритов. При первом соприкосновении со стенками изложницы в тонком прилегающем слое жидкого металла возникает резкий градиент температуры и явление переохлаждения, ведущее к образованию большого количества центров кристаллизации.
2-я зона – зона столбчатых кристаллов. С образованием корки условия теплоотвода меняются, градиент температуры резко уменьшается и, следовательно, уменьшается степень переохлаждения металла. В результате из небольшого числа центров кристаллизации начинают расти нормально ориентирванные к поверхности корки (т.е. в направлении отвода тепла) столбчатые кристаллы.
3-я внутренняя зона состоит из крупных, различно ориентированных дендритов. В центре слитка уже нет определенной направленности отдачи тепла. Температура застывающего металла успевает почти совершенно уравниваться в различных точках. В результате образуется равноосная структура. Зародышами кристалла здесь являются обычно различные мельчайшие включения в жидкой стали, например, тугоплавкие составляющие.
В случае сильного перегрева и резкого охлаждения зона столбчатых кристаллов заполняет весь слиток. Структура такого слитка называется транскристаллической, она менее прочна.
Свойства металла зависят от относительного распределения зон столбчатых и равноосных кристаллов. В зоне столбчатых кристаллов металл более плотный, он содержит меньше раковин и газовых пузырей. Однако места стыка столбчатых кристаллов обладают малой пластичностью. Ввиду скопления большого количества неметаллических включений и при последующей горячей обработке (ковка, штамповка) в этих местах могут получаться трещины. Поэтому для малопластичных металлов (в том числе и для стали) нежелательно развитие транскристаллизации. Для пластичных сплавов и металлов (Cu, Al и др.) развитие транскристаллизации желательно.
Жидкий металл имеет больший объем, чем закристаллизовавшийся. Залитый в форму металл в процессе кристаллизации сокращается в объеме, поэтому образуются пустоты, называемые усадочными раковинами. Раковины могут быть либо сконцентрированы в одном месте, либо рассеяны по всему объему слитка.
В хорошо раскисленной [раскисление – процесс удаления из сваренной стали О2, которая присутствует в виде FeO] отлитой в изложницу стали, усадочная раковина образуется в верхней части слитка и в объеме всего слитка содержится малое количество газовых пузырей и раковин. Сталь, недостаточно раскисленная, так называемая кипящая, содержит раковины и пузыри во всем объеме.
Спокойная сталь, т.е. раскисленная Mn, Si, Al с концентрированной усадочной раковиной, лучше стали кипящей, раскисленной только Mn. Однако и кипящие стали имеют применение, т.к. они дешевые и их производство дает меньше отходов.
В спокойном металле в отходы идет верхняя и нижняя части слитка, а раковины и пустоты, равномерно распределенные по объему слитка кипящего металла, при прокатке завариваются.
4. Скорость процесса кристаллизации.
При прочих равных условиях, скорость процесса кристаллизации и строение металла после затвердевания зависят от числа центров кристаллизации, возникающих в единице времени, в единице объема, т.е. от скорости образования зародышей [1/см3∙с] υз и скорости роста зародышей, или скорости увеличения минимальных размеров растущего кристалла в единице времени υр [мм/с].
Чем больше скорость υз и υр, тем быстрее протекает процесс кристаллизации. При равновесной температуре кристаллизации Тs (пл-кр) число центров и скорость роста равны нулю и поэтому кристаллизация не происходит.
. 
При увеличении степени переохлаждения до определенной величины ∆ Т=Тs-Ткр υз и υр возрастают, достигая максимума, после чего снижаются. Обычно скорость образования зародышей растет более резко, поэтому с увеличением степени переохлаждения получают все более мелкие кристаллы
Характер кривых объясняется тем, что для образования зародышей необходимо не только увеличение разности свободных энергий жидких и твердых металлов ∆Z, но и диффузионное перемещение атомов в жидком металле. Очень низкие температуры снижают подвижность атомов настолько, что большой выигрыш ∆ Z оказался недостаточным для образования зародышей и их роста (υз = 0 и υр = 0). В результате затвердевания в таком случае должно быть достигнуто аморфное состояние.
Металлы обычно кристаллизуются раньше, чем достигается степень переохлаждения, вызывающая снижение υз и υр, т.е. реализуются только восходящие ветви скорости образования зародышей и скорости роста.
5. Величина зерна.
Величина зерна находится в следующей зависимости от числа зародышей и скорости их роста:
Чем больше скорость образования зародышей и меньше скорость их роста, тем меньше размер кристалла. При небольшой степени переохлаждения число зародышей мало и зерно крупное, с увеличением ∆ Т скорость образования зародышей возрастает, и размер зерна в затвердевшем металле уменьшается.
Величина зерна сильно влияет на механические свойства сплава, в частности, вязкость и пластичность выше, если металл мелкозернист. Величина зерна зависит от температуры нагрева и разливки жидкого металла, его химического состава и присутствия примесей.
В настоящее время в производстве черных и цветных металлов широко практикуется процесс искусственного регулирования размеров и формы зерен путем введения в расплавленный металл нерастворимых веществ. Этот процесс называется модифицированием, а примеси, воздействующие на структуру – модификаторами. Благодаря равномерному распределению искусственных примесей по всему объему жидкого металла, зерна получаются мелкими и несколько иной формы. Такое изменение структуры металла улучшает его механические и технологические свойства.
6. Методы исследования кристаллического строения металла.
Внутреннее строение металлов и сплавов изучается с помощью рентгеноструктурного и металлографического анализов.
Строение кристаллических решеток, ориентацию кристаллических плоскостей, внутренние напряжения в решетках изучают рентгеноструктурным методом.
Внутреннее строение, определяемое рентгеноструктурным анализом, называется атомнокристаллической структурой.
Металлографический анализ делится на макро- и микроанализ и позволяет определить размеры, форму и расположение кристаллов.
Макроанализ заключается в исследовании строения металлов и сплавов невооруженным глазом или при небольших увеличениях (до 30 раз).
Строение, определенное термической обработкой, называется макроструктурой. Исследования проводят на макрошлифах или изломах. Макроанализ позволяет установить:
1.Строение металла (зернистое, дендритное); наличие зон кристаллизации, трещин, пузырей и т.д..
2. Химическую неоднородность (ликвацию), получаемую при кристаллизации. S, F, C имеют склонность к неравномерному распределению по сечению слитка, что сильно сказывается на свойствах. Это явление не устраняется последующей обработкой.
3. Строение после горячей обработки (волокна).
4. Определить характер разрушения металла (вязкость, хрупкость).
Микроанализом называют исследование внутреннего строения металла с помощью оптического микроскопа при увеличении от 30-50 до 1500-1800 раз и электронного при увеличении от 15000 до 60000 раз. Внутреннее строение, изучаемое с помощью микроскопа, называется микроструктурой или структурой. Впервые применил Павел Петрович Аносов (1831 г.). Микроструктурный анализ проводят с целью определения микроструктуры и фазового состава сталей и сплавов, оценки количества, размеров, формы и распределения различных фаз. Этот анализ позволяет установить связь химического состава, условий производства и обработки сплава с его микроструктурой и свойствами.
7. Диффузия.
Многие процессы, протекающие в металлах и сплавах, в том числе кристаллизация, носят диффузионный характер.
В кристаллическом теле под диффузией понимают перемещение атомов на расстояния, превышающие средние межатомные расстояния данного вещества. Если процесс перемещения атомов не связан с изменением концентрации в отдельных объемах, то процесс называется самодиффузией.
Самодиффузия – это перемещение атомов основного металла в своей собственной кристаллической решетке.
Диффузия, сопровождающаяся изменением концентрации, происходит в сплавах с повышенным содержанием примесей и называется гетеродиффузией.
Каждый атом совершает случайные блуждания, т.е. ряд скачков между различными равновесными положениями в решетке. Любая атомная теория должна начинаться с рассмотрения механизма, объясняющего, каким образом данный атом перемещается в решетке.
Для описания процесса диффузии в твердом теле предложено несколько возможных механизмов: циклический, обменный, вакансионный, межузельный.
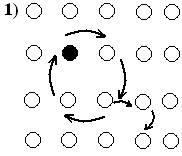 По циклическому механизму диффузии перескок представляет собой совместное перемещение группы атомов (вращение). Такое вращение не требует большой энергии, но маловероятно.
По циклическому механизму диффузии перескок представляет собой совместное перемещение группы атомов (вращение). Такое вращение не требует большой энергии, но маловероятно.
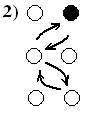 Обменный механизм является частным случаем циклического (гр. из 2-х атомов) и заключается в обмене соседних атомов.
Обменный механизм является частным случаем циклического (гр. из 2-х атомов) и заключается в обмене соседних атомов.
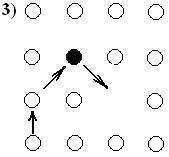 При вакансионном механизме диффузии атомы обмениваются местами с вакансией.
При вакансионном механизме диффузии атомы обмениваются местами с вакансией.
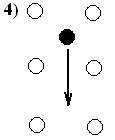 При межузельном механизме атом переходит в состояние равновесия в ближайшее междоузлие.
При межузельном механизме атом переходит в состояние равновесия в ближайшее междоузлие.
В металлах диффузия преимущественно осуществляется по вакансионному механизму. При диффузии в металле элементов с малым атомным радиусом (С, N2, H2) механизм межузельный.
Скорость диффузии определяется количеством вещества m, диффундирующего через единицу площади поверхности раздела в единицу времени. m зависит от градиента концентрации элемента dc/dx в направлении, перпендикулярном к поверхности раздела и пропорционально коэффициенту Д: dx
m= - Д dc - закон Фика.
Знак « - » указывает, что диффузия протекает в направлении от объемов с большей концентрацией к объемам с меньшей концентрацией.
Коэффициент Д [см2/с] – количество вещества, диффузирующего через единицу площади 1 см2 в единицу времени (1 с.) при перепаде концентраций равном 1. Коэффициент зависит от природы сплава, размеров зерна и от температуры.
“Д” в твердых сплавах крайне чувствителен к дефектам кристаллической решетки, возникающим при нагреве, напряжениях, деформациях и других воздействиях. Увеличение числа дефектов (главным образом вакансий) облегчает перемещение атомов и приводит к росту “Д”.
Дата добавления: 2019-05-21; просмотров: 1019;











