Денатурация белка. Термодинамическая характеристика денатурации. Этапы денатурации белка. Механизмы денатурации. Способы денатурации. Ренатурация.
Денатурация – потеря белком своей активности, нативности, рабочей структуры.
В термодинамическом плане денатурация сопровождается увеличением энтропии и уменьшением свободной энергии белка. Существует два механизма денатурации для малых и крупных белковых молекул.
1. 
2. 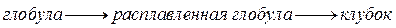
В первом случае процесс денатурации представляет собой ФП 1 рода, что обеспечивается наличием большого числа слабых связей с глобуле.
Во втором случае на первом этапе плавления глобулы происходит нарушение упорядоченности боковых групп, но сохраняется общая пространственная структура. Этот переход происходит как ФП 1 рода. Дальнейшие этапы денатурации зависят от доменной и вторичной структуры и могут происходить как ФП любого рода.
Расплавленная глобула является устойчивым интермедиатом разворачивания белка и характеризуется минимумом свободной энергии.
Самые распространенные способы денатурации: температурная, химическая, лучевая (механизмы – это то, что лежит в основе каждого способа денатурации).
Температурная – 2 типа:
1.Тепловая – при увеличении температуры. В основе лежит увеличение скорости молекулярных движений, приводящих к разрыву связей (ковалентных, дисульфидных, координационных, реже пептидных).
2.Холодовая – при понижении температуры. Причина денатурации – снижении гидрофобности.
Химическая– оттягивается часть водородных связей при погружении в раствор, следовательно белок становится менее стабилен (т.к. вода тоже является конкурентной).
Лучевая – обусловлена поглощением атомами белка энергии, следствие – разрыв связей.
Установлено, что денатурация (Д.) малых белков представляет собой S-образную кривую. 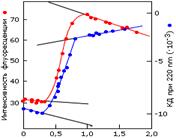
Характеристики молекулы меняются от тех, что характерны для нативного белка до тех, что характерны для белка денатурированного.
Узость этих S-образных кривых свидетельствует о кооперативности перехода (о том, что он охватывает много аминокислотных остатков).
Переход «все или ничего»:
Калориметрическое исследование тепловой денатурации лизоцима при разных рН. Положение пика удельной теплоемкости (Ср) определяет температуру T0, его ширина — ширину перехода дельта T, площадь под пиком — поглощенное при плавлении тепло дельта Н в расчете на грамм белка. ( Т.е. Энтальпия и температура денатурации белка зависят от рН среды, следовательно, существенна роль электростатических эффектов).
Например, миоглобин
при рН 12,2 - Т плавл. =50°С и ΔН =300 кДж/моль;
при рН 10,7 - Т плавл. = 78°С и ΔН=710 кДж/моль.
Сочетание факторов существенно влияет на механизм денатурации.
Денатурация кислотой или щелочью определяется:
1.Свободная энергия полиэлектролита обратно пропорциональна квадрату суммы заряда поверхности. Стабильность глобулы уменьшается в обе сторон от изоэлектрической точки (ИЭТ – это когда число разноименных зарядов в молекуле одинаково, суммарный заряд = 0).
2.Изменение pH может приводить к ионизации групп, погребенных в неполярном ядре глобулы (гидрофобном ядре). Эти группы притягивают гидратные оболочки, а следовательно происходит сдвиг равновесия к расплавленной форме.
Увеличенная теплоемкость денатурированного белка – следствие увеличения поверхности контакта его гидрофобных боковых групп с водой при частичном или полном разворачивании белка.
Принцип «все или ничего» - микроскопический аналог ФП 1-ого рода (ФП 1-ого рода в чистом виде наблюдается в маленьком белке или отдельных доменах крупного белка). Денатурация крупного белка – есть сумма денатурации доменов.
Как плавится белок: целиком или по частям?
Калориметрическая теплота – это кол-во тепла, поглощаемо одной молекулой белка в процессе плавления.
Эффективная теплота перехода – это кол-во тепла, поглощенного одной независимой «единицей плавления».
Если эффективная теплота перехода МЕНЬШЕ калориметрической теплоты перехода, значит единица плавления МЕНЬШЕ, чем сама молекула белка. Такая молекула плавится по частям.
Если эффективная теплота перехода БОЛЬШЕ калориметрической теплоты перехода, единица плавления БОЛЬШЕ этой молекулы. Плавится агрегат молекул.
Если эти 2 теплоты перехода равны, значит молекула плавится как единое целое, единица плавления = этой молекуле. (критерий Вант-Гоффа – для перехода «все или ничего»).
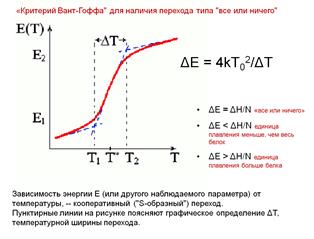
Детьта Т определяется шириной зоны резкого изменения любого экспериментального параметра, определяющего вероятность расплавленного состояния.
• ΔE = ΔH/N «все или ничего», где ΔH – кол-во тепла, поглощаемое всеми имеющимися молекулами, N – кол-во всех молекул белка, ΔH/N – калориметрическая теплота.
• ΔE <ΔH/N единица плавления меньше, чем весь белок
• ΔE > ΔH/N единица плавления больше белка (сразу несколько молекул плавится).
В процессах денатурации и ренатурации белка разные стадии представляют собой фазовые переходы разного рода. Для малых белков процесс можно считать одностадийным. Этот процесс происходит как ФП 1 рода.
Для крупных белков этот процесс многостадийный, и разные его стадии происходят как ФП разного рода. 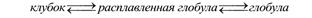
Денатурация может быть:
Обратимой, если возможно восстановление свойственной белку структуры. Такой денатурации подвергаются, например, рецепторные белки мембраны.
Необратимой, если восстановление пространственной конфигурации белка невозможно. Обычно это происходит при разрыве большого количества связей, например, при варке яиц.
Если белок подвергся обратимой денатурации, то при восстановлении нормальных условий среды он способен полностью восстановить свою структуру и, соответственно, свои свойства и функции. Процесс восстановления структуры белка после денатурации называется ренатурацией.
Дата добавления: 2020-11-18; просмотров: 853;











