Продукция цветной металлургии
· слитки цветных металлов;
· лигатуры (сплавы цветных металлов с легирующими компонентами);
· слитки чистых и особо чистых металлов, для электронной и радиотехнической промышленности.
Исходные материалы для производства металлов и сплавов
Для производства металла используют руду, флюсы, топливо и огнеупорные материалы.
Промышленной рудой является горная порода, из которой при данном уровне развития техники целесообразно извлекать металл или его соединения (железа, если его в руде содержится 30 – 60 %; меди, если ее содержание в руде составляет 3 – 5 %, молибдена – 0,005 – 0,02%). Сама руда состоит из минералов и пустой породы.
Минерал – это сам металл или его соединения.
Пустая порода – различные примеси.
Сами руды бывают богатыми и бедными. Бедные руды подвергают обогащению, после чего из них получают концентрат. Использование концентрата улучшает технико-экономический показатель металлургических печей.
Флюсы – материалы, загружаемые в плавильные печи для образования легкоплавких соединений с пустой породой руды или концентрата. Такое соединение называют шлаком, то есть
Флюс -> печь с высокой температурой обработки -> шлак.
Шлак имеет меньшую плотность по сравнению с основным металлом, он всплывает в процессе плавки и защищает металл от печных газов и воздуха.
Шлак бывает двух видов: кислый и основной.
В кислом шлаке преобладают такие элементы как кремний, кислород, оксид фосфора.
В основном шлаке – оксид кальция, оксид магния, оксид железа и др.
Топливо используется для доменного процесса (кокс, природный газ, мазут, колошниковый газ).
Огнеупорные материалы используют для изготовления внутренней облицовки слоя печи и ковшей для расплавленного металла.
Физико-химическая сущность процесса получения стали
Стальной лом (скраб) и передельный чугун – основные материалы для получения стали. Эти перечисленные материалы называются шихтой.
Сущностью любого металлургического процесса является переделка чугуна в сталь и снижение содержания углерода и примесей путем их избирательного окисления и перевода в шлак или в газы в процессе плавки.
Состав передельного чугуна низкоуглеродистой стали
Таблица 1
| Компоненты | Содержание компонента в % | |
| Передельный чугун | Низкоуглеродистая сталь | |
| Углерод | 4 – 4,4 | 0,14 – 0,22 |
| Кремний | 0,76 – 1,26 | 0,12 – 0,3 |
| Марганец | до 1,75 | 0,4 – 0,65 |
| Фосфор | 0,15 – 0,3 | 0,05 |
| Сера | 0,03 – 0,07 | 0,0055 |
Примеси отличаются по своим физико-химическим свойствам, следовательно для удаления каждой из них в плавильном агрегате создают определенные условия, используя основные законы физической химии.
1 закон. В соответствии с законом “Действующих масс” скорость химических реакций пропорциональна концентрации реагирующих веществ. Так как в чугуне содержится наибольшее количество железа (Fe), то оно окисляется в первую очередь, при взаимодействии с кислородом (О2).
Fe + ½ O2 = FeO + 264 кДж(выделение тепла – экзотермическая реакция) (1)
Одновременно с железом будут окисляться Si, P, Mn и другие примеси. Образующийся FeO при повышении температуры растворяется в Fe и отдаёт свой кислород более активным примесям в чугуне, окисляя их.
2FeO + SiO = SiO2 + 2Fe + 330.5 кДж (2)
5FeO + 2P = P2O5 + 5Fe + 226кДж (3)
FeO + Mn = MnO + Fe + 123кДж (4)
FeO + C = CO + Fe – 154 кДж (поглощение тепла – эндотермическая реакция) (5)
Чем больше содержания FeO в жидком металле, тем активнее будут окисляться примеси, следовательно для ускорения окисления примесей в расплав добавляют железную руду или окалины.
2 закон. Скорость окисления примеси зависит не только от концентрации, но и от температуры, и подчиняется закону Ле Шателье – химические реакции выделяющие теплоту интенсивно протекают при низких температурах, а реакции с поглощением тепла протекают активно при более высоких температурах.
3 закон. После расплшавления шихты образуются две несмешивающиеся жидкости (среды) – это жидкий шлак и металл, которые разделены. В соответствии с законом распределения Нернста “Если какое-либо вещество растворяется в двух соприкасающихся но не смешивающихся жидкостях, то распределение вещества между ними происходит до установления определенного соотношения при данной температуре (характеризуется константой распределения)”.
Следовательно, большинство компонентов и их соединения будут распределяться между шлаком и металлом. Нерастворимые соединения в зависимости от плотности будут либо в шлаке, либо в металле.
Изменяя состав шлака можно менять соотношение между количеством примесей в металле и шлаке так, что нежелательные примеси будут удаляться из металла в шлак. Удаляя шлак с поверхности металла и наводя новый при подаче флюса требуемого состава, можно удалять вредные примеси такие как фосфор (P), сера (S). Следовательно регулирование состава шлака с помощью флюсов является одним из путей управления металлургическим процессом.
Весь процесс плавки происходит в три этапа:
1 этап. Расплавление шихты и нагрев ванны жидкого металла. Так как на этом этапе температура невелика, то интенсивно происходит окисление железа с образованием оксида и окислов примесей (по реакциям 2 и 4 указанных выше). Выделяющийся фосфорный ангидрид P2O5 (реакция 3) образует с оксидом железа FeO нестойкое соединение (FeO)3P2O5. Так как у CaO сильнее основные свойства, чем у FeO, то он связывает фосфорный ангидрид, переводя его в шлак.
2[P] + 5(FeO) + 4(CaO) = (4CaOP2O5) + 5[Fe], (6)
здесь [] – в металле;
() – в шлаке.
Для удаления фосфора из металла необходимо достаточное содержание FeO , для этого в период плавки добавляют железную окалину или руду, наводя железистый шлак.
По мере удаления фосфора из металла его содержание в шлаке увеличивается, следовательно согласно закону распределения удаление фосфора из металла будет замедляться. Для ускорения процесса удаления фосфора старый шлак сливают и наводят новый со свежими добавками CaO.
2 этап. “Кипение” ванны жидкого металла. Процесс начинается по мере прогрева при более высокой температуре, чем на первом этапе. При повышенной температуре в соответствии с принципом Ле Шателье начинает более интенсивно протекать реакция окисления углерода (реакция 5) так как в металле содержится углерода С2 больше чем всех других примесей, то в соответствии с законом действующих масс для его окисления в металл вводят значительное количество руды, окалины или вдувают кислород (протекает реакция 1). При этотм образующийся оксид железа реагирует (согласно реакции 5) с С2, а пузырьки углекислого газа СО2 выделяются из жидкого металла, вызывая его “кипение”. При “кипении” уменьшается содержание углерода до требуемого количества, выравнивается температура по объему ванны, частично удаляются неметаллические включения, прилипающие к всплывающим пузырькам углекислого газа. Всё это способствует качеству металла, следовательно, процесс “кипения” металла является основным в плавке сталей. В этот же период создаются условия для удаления серы из металла, которая находится в нем в виде сульфида, а также в шлаке ((FeS) и [FeS] ). Чем выше температура, тем дольше количество FeS растворяется в шлаке, происходит процесс перехода серы из металла в шлак, при этом сульфид железа растворяется в шлаке, взаимодействуя с СаО.
(FeS) + (CaO) = (CaS) + [FeO] (7)
Как видно из реакции (7) , чем больше (СаО) и меньше (FeS), тем полнее удаляется сера в шлак.
Вывод:
при плавке в основных печах можно снизить содержание угленрода и серы в стали, при этом выплавлять металл из шихты любого химического состава;
в печах с кислой футеровкой нет условий для уменьшения количества фосфора и серы в стали, так как нельзя использовать основной шлак с повышенным содержанием СаО из-за разрушения футеровки печи, следовательно, в “кислых” печах выплавляют метел с низким содержанием серы и фосфора.
3 этап. Раскисление стали. Это процесс восстановления оксида железа в жидком металле.
(FeS) + (CaO) = [FeO] +CaS (8)
При плавке высокое содержание кислорода необходимо для окисления примесей, но в готовой стали – это очень вредная примесь, сильно снижающая механические свойства металла при высокой температуре. Сталь раскисляют двумя способами: осаждающим и диффузионным.
Осаждающее раскисление – введение в жидкую сталь растворимых раскислителей (FeMn, FeSi, Al), которые в данных условиях обладают большим родством к кислороду, чем железо. Происходит восстановление железа и образуются оксид магния, оксид кремния и алюминия, имеющие малую плотность и удаляющиеся в шлак. При нарушении режима раскисления некоторые примеси могут остаться в металле, что снизит его механические свойства.
Диффузионное раскисление – раскисление шлака. Мелко размельченный раскислитель загружают на поверхность шлака, который восстанавливает оксид железа, уменьшая его содержание в шлаке. Согласно закону распределения растворенный оксид железа в стали, начинает переходить в шлак. При этом способе все образующиеся оксиды остаются в шлаке, а восстановленное железо переходит в сталь, что уменьшает содержание в ней неметаллических включений и повышает качество. При плавке в кислой печи процесс протекает при кислом шлаке (55-58% SiO2), что создает благоприятные условия для полного раскисления стали. Кремнеземные сильные свойства связывающие оксид железа с оксидом кремния при долгой выдержке под кислым шлаком приводят к резкому уменьшению процентного содержания оксида железа в стали.
По степени раскисления различают следующие виды сталей: спокойные, кипящие, полуспокойные. Спокойные стали – при полном раскислении в печи и ковше, кипящие стали – здесь раскисление в печи происходит не полностью, её раскисление продолжается в изложнице, при затвердевании слитка.
FeO + C = Fe +CO (9)
CО способствует удалению водорода и азота в виде пузырьков, вызывая “кипение”. “Кипящая” сталь почти не содержит неметаллических включений (продуктов раскисления). Такая сталь обладает высокой пластичностью.
Разливка высококачественной стали.
Выплавленную сталь разливают в изложницы, где происходит ее кристаллизация, то есть образуется слиток. Слиток по своему кристаллическому строению не однороден. Обычно слиток спокойной стали имеет следующие зоны:
1. поверхностный слой мелких кристаллов;
2. зона столбчатых кристаллов;
3. внутренняя зона крупных различно ориентированных кристаллов;
4. конус осаждения из более мелких неориентированных кристаллов;
5. мост плотного металла верхней части слитка из хорошо сформировавшихся неориентированных кристаллов;
6. усадочная раковина.
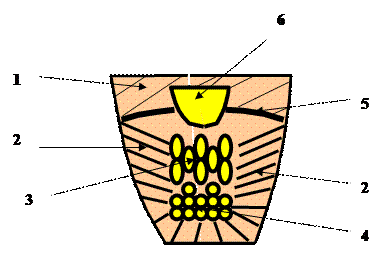
В слитке могут появляться продольные и поперечные трещины. Все пустоты, включая усадочную раковину – это следствие неравномерности теплообмена в изложнице во время кристаллизации.
Для устранения дефекта необходимо:
1. чтобы футеровка изложницы была без дефектов;
2. поверхность изложницы должна быть достаточно чистой;
3. изложница должна быть хорошо теплоизолирована.
При кристаллизации слитка создаются не равные условия теплообмена в верхней и нижней части слитка, т.к. через верхнюю поверхность (свободную) металла осуществляется несоизмеримо меньший отвод тепла, чем стенками и дном изложницы. То сокращение объёма слитка сопровождается нижним уровням жидкого металла и образуется в итоге усадочная раковина, глубоко распространяющаяся в тело слитка. Усадочная раковина выводится с помощью прибыльной надставки – это сужающаяся часть в верхней части изложницы.

Чтобы сохранить металл в прибыльной части слитка, в течение всего времени затвердевания, применяют специальные способы обогрева прибыли сверху. Это делается с помощью люнкеритных смесей, которые содержат 20% Al, 10%FeSiO2, 20% древесного угля, 20% кокса + шамотный порошок и боксит. Или используются экзотермические смеси, которые засыпаются в прибыльную часть надставки на поверхность металла.
Использование смесей уменьшает скорость снижения температуры металла в прибыльной части слитка (в 4 раза по сравнению с открытым зеркалом металла). Жидкую сталь разливают в изложницы на установках непрерывной разливки. Сама разливка металла в изложницы осуществляется двумя способами: разливка осуществляется сверху или производится сифоном.
При разливке сверху, металл поступает в изложницу (2) непосредственно из сталеразливочного ковша (1) или через промежуточное устройство в виде воронки (3). При сифонной разливке жидкая сталь из ковша попадает в центровую (2), затем по сифонной проводке (3) поступает в изложницу (4) через поддонник (количество изложниц 2 - 6).

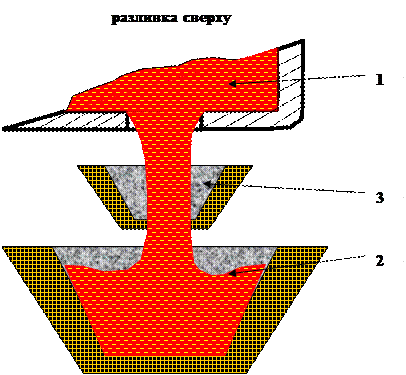
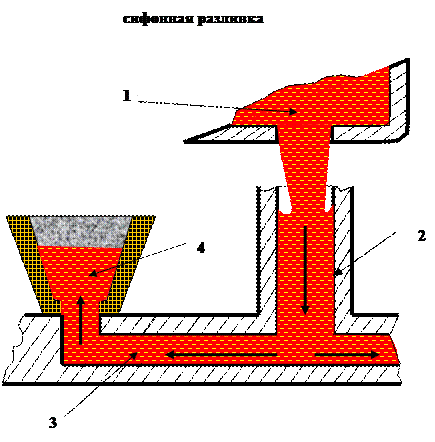
Разливка сверху часто встречается в цехах с большой производительностью при выплавке больших слитков. Разливка сифоном даёт возможность разлить единовременно сталь на несколько малых слитков, удобно наблюдать за поверхностью поднимающегося металла, а также улучшается поверхность металла в слитках. К недостаткам можно отнести увеличение расхода огнеупора, трудозатраты по зачистке сифонов.
ВНЕПЕЧНОЕ РАФИНИРОВАНИЕ СТАЛИ (ВРС)
Особенности внепечного рафинирования:
При увеличение удельной мощности дуговых печей и мощности трансформатора. Нерациональное проведения процессов рафинирования (очистка от примесей) в сталеплавильных печах, особенно с восстановительным периодом. Рафинирование стали в крупных сталеплавильных печах в следствие малой удельной поверхности ванны, низкой скорости процесса взаимодействия металла и шлака, а также сложности смены шлака весьма затруднительно, при этом очень низкое использование мощности. Все это приводит к снижению производительности, а также к увеличению расходов раскислителей и легирующих элементов. Сказывается на качестве стали, приводит к снижению. Все эти показатели значительно повышаются при внепечном рафинирование стали.
При внепечном рафинирование, используется вакуум, кислород, инертный газ, синтетический шлак и др.
Достоинства внепечного рафинирования:
- Увеличение скорости взаимодействия металла со шлаком, из-за увеличения контактной поверхности в результате перемешивания.
2. Повышение интенсивной массы переноса, из-за увеличения градиента концентрации с уменьшением объема.
3. 3.Улучшение термодинамических условий удаления примесей, из-за изменения состава газовой атмосферы или создания вакуума.
4. Глубокое обезуглероживание стали.
5. Глубокое рафинирование стали от серы, в результате добавки синтетического шлака.
6. Возможность глубокой очистки от водорода.
Внепечное рафинирование осуществляется различными методами и их использование превращает сталеплавильную дуговую печь в агрегат для расплавления жидкостей и получения полупродукта.
Основные способы:
Дата добавления: 2016-07-27; просмотров: 3129;











