Інгібітори для розчинів
Механізм дії інгібіторів в рідких середовищах в більшості випадків полягає в гальмуванні катодних і анодних процесів електрохімічної корозії, утворенні захисних і пасивуючих плівок. У зв'язку з цим інгібітори можна класифікувати на анодні і катодні.
Анодні інгібітори
Дія анодних інгібіторів заснована на пасивації анодних ділянок кородіруючої поверхні металу. Тому їх нерідко називають пасиваторами.
Найчастіше всього як пасиватори використовують неорганічні окислювачі: хромати, нітрит, молібдати, вольфрамати. Легко відновлюючись на катодних поверхнях, вони поводяться як деполяризатори, викликаючи появу на анодних ділянках щільності струму, перевищуючих величини, необхідні для їх пасивації. При цьому стаціонарний потенціал облагороджується на десятих вольта, а швидкість анодного переходу в розчин іонів кородіруючого металу різко знижується.
До анодних сповільнювачів корозії відносять також деякі з'єднання з лужними властивостями: фосфати, поліфосфати, силікати, борати, бензоат натрію і ін. Їх інгібіруюча дія виявляється тільки за наявності розчиненого кисню, який і виконує роль пасиватора. Не будучи окислювачами, ці речовини лише сприяють адсорбції кисню на поверхні металу. Крім того, вони гальмують анодний процес розчинення через утворення захисних плівок, що є важко розчинні продукти взаємодії інгібітору з іонами перехідного в розчин металу. Так, наприклад, фосфати, адсорбуючись на поверхні стали, утворюють з іонами заліза екрануючі плівки, що складаються із суміші - Fе2O3 і FePO4∙2H2O .
Анодні інгібітори корозії відносяться до категорії небезпечних, тому що за певних умов вони із сповільнювачів корозії перетворюються на її стимулятори. Це найчастіше відбувається, коли корозійний процес протікає з катодним контролем, і по тим чи іншим причин не забезпечується пасивація анодних ділянок. У даному випадку сильні окислювачі, що є хорошими деполяризаторами, легко відновлюються на катодних ділянках і збільшують швидкість корозії. Для того, щоб цього не відбулося, щільність корозійного струму повинна бути вище тієї, при якій досягається повна пасивація анодних ділянок. Тому концентрація інгібітору (пасиватору) не повинна бути нижче визначеною величини, інакше пасивація може не наступити чи буде неповною.
Неповна пасивація також дуже небезпечна, тому що приводить до скорочення анодної поверхні, збільшення швидкості і глибини руйнування металу на локалізованих ділянках, тобто появі точеної корозії.
Мінімальна концентрація CrO22-, NO2-, MO42-, використовуючи як інгібітори корозії стали, приблизно рівна 10-4–10-3 моль/л. При підвищенні температури середовища чи наявності в ній активаторів, наприклад хлор - іонів, необхідне збільшення концентрації інгібітору.
Анодні сповільнювачі неокислювального типу (фосфати, силікати і ін.), додані в незначній кількості, також викликають більш глибоку місцеву корозію через сильне збільшення співвідношення катодної площі до анодної.
Таким чином, для забезпечення ефективного захисту необхідно підтримувати концентрацію анодного інгібітору вище за граничне значення у всіх ділянках виробу, що захищається (наприклад, у нарізних сполученнях, щілинах і інших важкодоступних місцях).
Анодні інгібітори дуже чутливі і до рН середовища.
Застосування анодних інгібіторів різноманітне. Хромати і біхромати використовують для захисту сталевих конструкцій в оборотних охолоджуючих водах двигунів внутрішнього згорання, ректифікаторів, резервуарів, напірних баків, баштових холодильників і т.д. У нейтральних середовищах за відсутності іонів Сl - достатня концентрація К2СrO4 0,04 — 0,1%. При змісті хлоридів від 100 до 1000 міліграм/л вона повинна бути збільшена до 1—2%. Хромати застосовують також для захисту від корозії алюмінію, магнію і їх сплавів в нейтральних і лужних середовищах.
Нітрит успішно використовують як інгібітори в антифризах, тому що на противагу хроматам вони слабо реагують із спиртами і етиленгліколем. Нітрит менш придатний для охолоджуючих вод, оскільки поступово розкладаються бактеріями. Дія нітриту, що інгібірує, обмежується рН середовища не менше 6.
Фосфати і поліфосфати знаходять застосування як сповільнювачі корозії стали у воді і холодильних розсолів. Більший ефект досягається при спільному використанні фосфатів і хроматів.
Катодні інгібітори
Катодні інгібітори зменшують швидкість корозії внаслідок зниження ефективності катодного процесу чи скорочення площі катодів.
Зниження ефективності катодного процесу може бути досягнуте:
а) при корозії з кисневою деполяризацією — зменшенням змісту
кисню в рідкому корозійному середовищі;
б) при корозії з водневою деполяризацією — підвищенням
перенапруження реакції виділення водню.
Зменшення змісту розчиненого в корозійному середовищі кисню гальмує реакцію його відновлення, а отже, і швидкість корозії.
Перенапруга водню може бути підвищене при введенні в корозійне середовище солей деяких важких металів — AsCl3, Bi2(SO4)3. Катіони цих металів контактно відновлюються на катодних ділянках, утрудняють реакцію виділення водню і тим самим — процес корозії, якщо він відбувається по механізму водневої деполяризації.
Скорочення площі катодів досягається додаванням інгібіторів, які на катодних ділянках в умовах місцевого підлуженя середовища утворюють нерозчинні продукти, ізолюючі частину поверхні катодів від розчину. Такою речовиною є, наприклад, бікарбонат кальцію, який в підлуженому середовищі виділяється у вигляді важко розчинного осаду карбонату кальцію. Цим пояснюється менша корозія сталі в жорсткій воді в порівнянні із зм'якшеною.
Катодні інгібітори по захисній дії менш ефективні, ніж анодні. Проте вони зовсім безпечні, оскільки не викликають посилення корозії при їх недостатньому змісті.
Інгібітори травлення
Анодними і катодними сповільнювачами корозії в нейтральних та лужних середовищах, є переважно неорганічні речовини. Ці інгібітори не роблять захисної дії в сильно кислих розчинах, де процес корозії протікає з водневою деполяризацією.
Сповільнювачами корозії в кислих середовищах звичайно є органічні речовини, у молекулах яких містяться полярні або деякі специфічні групи, наприклад аміни, альдегіди, тіомочевіна, меркаптани, феноли, деякі гетероциклічні з'єднання, солі ароматичних карбоксильних кислот і ін. Передбачається, що механізм дії цих сповільнювачів носить адсорбційний характер. Адсорбуючись на катодних і анодних ділянках, вони утрудняють розряд іонів водню і реакцію іонізації металу. Тому при додаванні інгібітору в кислоту стаціонарний потенціал може майже не змінюватися, хоча швидкість корозії значно зменшується .
Захисний ефект органічних інгібіторів корозії в значній мірі залежить від їх природи, концентрації, температури, виду аніона кислоти, концентрації водневих іонів.
Органічні інгібітори знаходять достатньо широке застосування при травленні сталі в кислотах для видалення окалини і іржі. При додаванні цих інгібіторів у травильні розчини оксиди розчиняються без скільки-небудь помітного руйнування металу, що дозволяє уникнути перетравлювання, зменшує витрату кислоти.
Інша важлива перевага використання інгібіторів при кислотному травленні - зменшення водневої крихкості оброблюваного металу. У процесі травлення частина водню, що виділяється, дифундує в глиб металу і викликає появу водневої крихкості. Адсорбція інгібіторів підвищує перенапругу реакції виділення водню, зменшує кількість проникаючого в метал водню і тим самим знижує його крихкість.
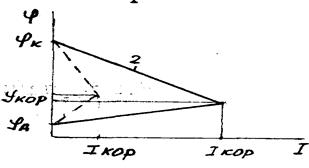
Рисунок 1 - Поляризаційна діаграма корозії заліза при травленні в
кислоті з інгібітором (I) і без нього (2)
2. Інгібітори атмосферної корозії
Атмосферна корозія — це електрохімічний процес, що протікає в тонкій плівці вологи, що утворюється на поверхні металу. Як правило, це корозія з кисневою деполяризацією. Тому до числа інгібіторів атмосферної корозії можна віднести майже всі пасиватори, використовувані як анодні сповільнювачі в нейтральних і лужних розчинах.
Інгібітори атмосферної корозії підрозділяють на нелетучі (контактні) і летучі (парофазні).
Нелеткі інгібітори наносять на поверхню металу чи пакувального матеріалу (папери, плівки для обгортання виробів). Дія їх обмежена місцем зіткнення з поверхнею металу. Прикладом нелетучого інгібітору служить нітрит натрію NaNO2. Після обробки сталевих деталей у водних розчинах NaNO2 і сушіння на поверхні металу утворюється пасивна плівка, що володіє високими захисними властивостями, а також тонкий шар сухого NaNO2, що безупинно відновлює пасивну плівку у випадку її механічного пошкодження.
Контактне інгибірування нітритом натрію застосовують для міжопераційного захисту сталевих виробів, у цехових умовах і при зберіганні готової продукції на складі. В останньому випадку вироби після пасивації в гарячому 25-30%-ном розчині NaNO2 загортають у пакувальний папір, змочений 10-15%-ним розчином NaNO2, а потім у сухий парафінований папір.
Більше значення мають летучі інгібітори. Вони здатні захищати метал, знаходячись у газовій чи паровій фазі. Ці інгібітори володіють високою пружністю пари, швидко заповнюють навколишню повітряну атмосферу і, адсорбуючись на металі, захищають його від атмосферної корозії. Летучі інгібітори характеризуються анодним, і катодним механізмом дії. Крім того, вони сприяють створенню гідрофобності поверхні металу, що захищається.
Деякі летучі інгібітори нетоксичні і не мають запаху. Тому їх можна застосовувати навіть у виробничих приміщеннях. Летючість інгібітору атмосферної корозії багато в чому визначає тривалість його захисної дії.
При повному випаровуванні інгібітору, нанесеного на обгортковий папір, його захисна дія припиняється. До летучих інгібіторів відносять нітрит заміщених амінів, складні ефіри карбонових кислот, карбонати заміщених амінів. Особливо ефективні нітрит і карбонат діциклогексиламіна, бензоат моноетаноламіна.
Тривалість захисної дії летучих інгібіторів також залежить від герметичності зовнішньої упаковки. При належній концентрації інгібітору і повної ізоляції від зовнішнього середовища (целофаном, фольгою) деталі з чорних металів можуть не піддаватися корозії в течії 10 років і більш.
3.Антикорозійні змащення
Захист металевих виробів від атмосферної корозії здійснюють також за допомогою антикорозійних змащень: нафтових олій, сала, воску, вазеліну. Широко використовують інгибірованні змащення, тобто змащення, що містять інгібітори корозії. При їх введенні значно підвищуються захисні властивості змащень.
Нафтові олія і змащення відносно дешеві. Їх легко наносити, видаляти, відновлювати. Застосування змащень не вимагає такої ретельної підготовки поверхні, яка необхідна при захисті металевими і лакофарбовими покриттями.
Нафтові змащення, як правило, не взаємодіють з металом, що захищається, не утворюють агресивних по відношенню до металу продуктів, достатньо стабільні при зберіганні і застосуванні.
Розрізняють щільні (консистентні) і рідкі мастила.
Щільні змащення — це мінеральні олії, що згущують до мазеподібних консистенцій додаванням мила, стеаринової, олеїнової і інших кислот, продуктів переробки нафти (петролатуму, парафіну, церезину). Шар щільного змащення, нанесений на металеву поверхню, перешкоджає проникненню води і кисню повітря до металу і тим самим утрудняє протікання корозійних процесів. Консистентні змащення наносять тільки на суху поверхню. Якщо на металі залишається волога, хоча б у вигляді мікрокрапельок, то він буде інтенсивно кородувати під шаром змащення. Консистентні інгібіруючі змащення застосовують в основному для консервації зовнішніх поверхонь машин, верстатів, механізмів.
Рідкі мастила — це мінеральні олії з розчинними в них інгібіторами корозії. У порівнянні з консистентними змащеннями їх легше наносити і знімати. Процес консервації рідкими мастилами піддається повній механізації і автоматизації. Витрата рідких мастил у декілька разів менше, ніж щільних.
Поряд з оліями як захисні змащення широко використовують віск. Його наносять прямо на метал чи пакувальний матеріал (папір).
Оліям і жирам віддають перевагу у випадках, коли експлуатація виробів переривається на короткий період або при необхідності зберігання напівфабрикатів. Олія більш легка наноситься на виріб і віддаляється з нього. Інгібіруючі олії в порівнянні з воском володіють гіршими захисними властивостями.
Плівка олії навіть значної товщини пропускає водяні пари в кількостях, достатніх для протікання корозійного процесу. Крім того, в олії міститься більше кисню, ніж у воді.
Недоліки захисних змащень: відсутність гарного товарного виду, трудомісткість процесу розконсервування.
4. Неіржавіючі стали
Матеріали, об'єднані терміном "неіржавіючі сталі", містить у собі сплави, основними складовими яких є залізо і не менше 10% С, як і в нізьколегірованих сталях існує різниця між сталями з малим, середнім і високим змістом вуглецю. Останні за своєю природою ближче до легованих чавунів. Їх застосовують головним чином там, де потрібна стійкість до окислення при високих температурах та опіру стиранню. Для підвищення стійкості до кислот до складу сталей почали вносити добавки молібдену - 2-3% і мідь, останніми роками титана і ніобію. Наявність цих добавок повисіла корозійну стійкість і розширила сфери застосування виробів з цих неіржавіючих сталей.
Стійкість неіржавіючих сталей зв'язана майже винятково з тим, що в найрізноманітніших зовнішніх умовах вони знаходяться в стані пасивності. Робоча гіпотеза прийнята багатьма спеціалістами, полягає у тому, що пасивна плівка є по суті оксидом. Загальний вид анодної поляризаційної кривої для неіржавіючих сталей у кислих розчинах показано на рис. (крива АВСДЕ). Якщо катодна крива цієї системи PQ перетинає анодну в єдиній крапці Р між В і З, то сталь знаходиться в пасивному стані і плівка, що утворилася, відновлюватиметься навіть після ушкоджень. У такий спосіб цей випадок взаємного розташування анодної і катодної кривих представляє умови, у яких сталь можна надійно використовувати. Якщо ж катодна крива РIQI перетинає анодну ще і на ділянці ДЕ, то пасивний стан нестійкий, і будь - яке ушкодження приводить до швидкого розчинення металу.
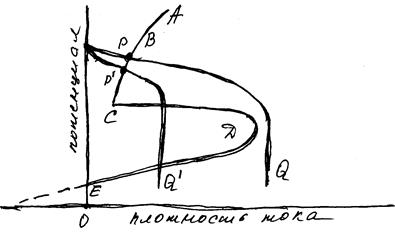
Кислоти, що встановлюють суміші кислот чи мають тенденцію зміщати катодні криві в область більш низьких потенціалів, тим самим сприяють корозії. Окисні розчини зміщують катодні криві до більш високих потенціалів і сприяють пасивності, якщо тільки катодні криві перетинають анодну криву на ділянці АВ. Це область перепасивації де плівка стає нестійкою через окислення.
ПИТАННЯ
1.Визначення і величина захисної дії інгібіторів.
2.Характеристики і умови застосування анодних інгібіторів.
3.Характеристики і умови застосування катодних інгібіторів.
4.Поняття про інгібітори травлення їх область застосування.
5.Характеристики і умови застосування інгібіторів атмосферної
корозії.
6.Склад і характеристики неіржавіючих сталей.
ЛІТЕРАТУРА
1. Л.И. Андропов. Коррозия и защита металлов. М. 1981 г., 270 с.
2. Е.С. Иванов Ингибиторы коррозии в кислых средах. М.
Металлургия, 1986 г 175 с.
ЛЕКЦІЯ №8
ЕКОЛОГІЧНО ЧИСТІ І РЕСУРСНОЗБЕРЕЖУЮЧІ ТЕХНОЛОГІЇ АНТИКОРОЗІЙНИХ ПОКРИТТІВ
Нанесення гальванічних покриттів ізносо -, корозійно ,-, ерозійно - і жаростійких антифрикційних, під паяння, декоративних виконується на гальванічних виробах використовується практично всіх промислових галузях народного господарства України.
Слідством гальванічного виробництва є шкідливі умови праці, забруднення навколишнього середовища викидами шкідливих відходів в повітряний і. водний басейни, а також велика кількість високотоксичних відходів (шлаків), які необхідно зберігати в спеціальних сховищах.
Об'єми покриттів, що наносяться щорічно в Україні 80-100 млн. м2. Ухвалення Законів про охорону навколишнього середовища передбачає штрафні санкції до шкідливих виробництв, у тому числі і гальванічного виробництва, і вимагає створення альтернативних екологічно чистих; ресурсо- і енергозберігаючих технологій і устаткувань.
Цим вимогам повністю відповідають засновані на є методах вакуумно-плазмові технології і їх устаткування для нанесення покриттів, а також ультразвукові (УЗ) технології і устаткування для очищення і знежирення поверхні виробів перед нанесенням покриттів. Практично всі працюючі і новостворювані в Україні підприємства, що вимагають в технологічному процесі виробництва виробів і матеріалів нанесення різноманітних покритті, потребують нового устаткування і технологічних процесів, що не створюють небезпеку навколишньому середовищу і працюючому персоналу.
У основу використовуваної технології встановлений модифікований метод конденсації речовини на поверхні промислового ним бомбардуванням (КІБ), що дозволяє одержувати, покриття різного призначення з хорошою адгезією до основи, зокрема на вироби складної конфігурації (труби, отвори, щілини, різьблення і ін.)
Замість хімічного або електрохімічного методів очищення виробів використовується УЗ-технологія, що дає можливість ефективно знежирювати і очищати поверхні виробів будь-якої конфігурації
Суть технології полягає в модифікації технології конденсування іонічним бомбардуванням КIБ за рахунок застосування ряду нових технологічних прийомів, включаючи використовування високочастотного поля. Вперше в світовій практиці вакуумно - плазмових установок здійснюється варіант без закріплення виробів, що покриваються. Розроблена i створена серія установок "АНГА" з продуктивністю не меншою, ніж у існуючого устаткування гальванічного виробництва. Перша з цієї серії «АНГА-01» для нанесення покриттів насипом на вироби в поперечнику від 1 до 30 мм була освоєна Сумським ВО "Електрон". Спроектовані установки «АНГА-02», призначені для нанесення покриттів на вироби розмірами до 850x350 мм, а також на рулонні матеріали; «АНГА-03» - для нанесення покриттів на довгомірні трубчасті і профільні вироби і «АНГА-04» - для нанесення покриттів на вироби особливо невеликого розміру насипом. Спроектовані УЗ-лінії різних габаритів, функціональних можливостей і потужностей, з напівавтоматичним (типу каруселі) і повністю автоматичним (конвеєр) управлінням. Економічне призначення використовуваних технологій полягає в:
- зниженні енергоспоживання, в порівнянні з гальванічним виробництвом, в 3-5 разів;
- підвищенні продуктивності в 2-3 рази;
- зменшенні витрат дефіцитного матеріалу для покриттів, і металоємності устаткування - в 5 разів. Соціальне і екологічне значення нових технологій полягає в:
- усуненні забруднення навколишнього середовища на робочих ділянках, де наносяться покриття на вироби промисловості, і повній безвідходній технології виробництва;
- підвищенні безпеки умов праці обслуговуючого персоналу.
- рулонна харчова жерсть для виготовлення консервних кришок, консервних банок і корпусів металевих термосів;
- лопатки і диски газових, парових, енергетичних і авіаційних турбін, компресорів; робочі колеса насосів; елементи клапанів, регуляторів і ін. енергетичне устаткування;
- деталі і вузли автомобільних і тракторних двигунів {поршні, кільця, вкладиші, клапани і ін.);
- галантерейна і меблева фурнітура (оправи окулярів ї затемнені стекла, корпуси авторучок, корпуси і браслети годинника, біжутерія і ін.);
- фарфоровий і скляний посуд, ювелірні вироби;
- метизи, ріжучий інструмент;
- накладні декоративні елементи автомобілів, аудіо- і відеоапаратури і іншої побутової техніки.
Матеріалом покриттів можуть служити: метали, сполуки і сплави металів, діелектрики. На відміну від гальваніки, покриття можуть наноситься не тільки на метали, але і на пластмаси, фарфор, скло, мармур, напівкоштовне каміння, папір, шкіру і ін. Покриття можуть бути одношаровими і багатошаровими, багатокомпонентними і композиційними. Створені УЗ- технології підготовки поверхні виробів і екологічно чисті енерго- і ресурсозбережуючі вакуумно-плазмові технології нанесення покриттів і устаткування.
ЛЕКЦІЯ № 9
ГРУНТОВА КОРОЗІЯ
Для оцінки природних ґрунтів велике значення має зв’язаність, під якою розуміють взаємний зв'язок окремих частинок ґрунту. Зв’язаність ґрунту зростає у міру зменшення розміру окремих частинок. З природних ґрунтів найбільшою корозійною активністю володіють глинисті, солончакові, пилуваті i торф’янисті.
Не зважаючи, що штучні i насипні ґрунти зустрічаються дуже рідко, саме вони повинні розглядатися як особливо небезпечні з погляду корозії.
Склад і концентрація речовин, розчинених в ґрунті, визначають властивості ґрунтового електроліту. Значною мірою ступінь корозійної активності ґрунту визначається величиною рН, від якої залежить стійкість плівок, що виникають на поверхні металу.
Одним з показників корозійної активності ґрунту по відношенню до сталi є концентрація іонів Сl- i SO42-. Сумарний вміст їх в ґрунті більше 0,1%, як правило, указує на його підвищену корозійну активність, при цьому вміст іона Сl- більш безумовно характеризує корозійну активність ґрунту, ніж зміст SO42-. Це пояснюється тим, що при великому вмісті хлоридів важко змінюється процес утворення плівок. Для свинцевих оболонок кабелів небезпечна присутність в ґрунті органічних і азотних речовин, а для алюмінієвих конструкцій - розчинних хлористих солей.
Небезпека корозії залежить від насичення ґрунту водою Обчислення вологи (%) виробляється шляхом віднесення маси води в ґрунті, рівний втраті маси зразка в результаті його висушування, до маси мокрого ґрунту.
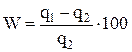
де q1 - маса ґрунту, узятого для визначення вологи, кг;
q2 - маса абсолютно сухого ґрунту, кг.
Вважається, що найсильніша корозія підземних споруд відбувається в ґрунті, що має волога 30%. Це обумовлено швидшою дифузією кисню в ґрунтах, не насичених водою , тобто в рихлих і пористих, тоді як при вологи > 30% кисень швидко розчиняється і швидкість дифузії його сповільнюється.
Процес корозії в ґрунті розвивається швидко при проникненні повітря в грунт, оскільки кисень повітря сприяє мiкробiологiчним процесам. Розміри частинок ґрунту впливають на його повiтропроникнiстъ. Пiщанi ґрунти унаслідок високої повiтропроникностi володіють звичайно окислювальними властивостями, а глинисті - відновними. В результаті нерівномірного проникнення повітря до підземної споруди по його довжині виникають гальванiчнi пари. Катодними ділянками цих пар, як правило, будуть добре aepуємі ділянки, а анодними - мало aepуємі.
Мiкроорганiзми змінюють хімічний склад середовища, що оточує підземну споруду, і активізують електрохімічні реакції, прискорюючи розвиток корозії. У ґрунтових умовах спостерігається корозія аероба, викликана дiяльнiстю бактерій аеробів, що живуть i розмножуються за відсутності вільного кисню за рахунок енергії розщеплювання різних хімічних сполук.
На швидкість корозії підземних споруд робить вплив температура ґрунту. В результаті добового i річного нагріву i охолоджування ґрунту виникає відмінність в температурі окремих частин підземної споруди, це веде до деякої рiзницi потенцiалiв між його суміжними ділянками і до протікання між ними корозійного струму.
Питомий опір ґрунту обумовлюється вмістом в ньому вологи i coлей. Крім того, воно залежить від величини i складу частинок ґрунту. Певну роль питомий опір ґрунту виконує у разі виникнення макрокорозiйних пар. Проте, повна характеристика корозійного процесу не завжди може бути дана на основі аналізу питомого опору ґрунту. Так, корозія сталевих або свинцевих конструкцій в піщаних ґрунтах, що володіють високим питомим опором, повинна бути малою, а в солончакових ґрунтах (низького питомого опору) - великою, Проте свинець в солончакових ґрунтах унаслідок утворення на його поверхні досить стійкої плівки з солей корозує слабкіше, ніж в піщаних.
Таким чином, інтенсивність корозії підземних споруд залежить від всіх розглянутих вище чинників, які можуть виявлятися. як окремо, так і в сукупності.
Лабораторна робота
При визначенні питомого опору ґрунту користуються симетричною чотириелектродною установкою (рис. 1), розміщеною в одну лінію, яка для проектованої споруди повинна співпадати з віссю траси, а для укладеного в землю - проходити паралельно останньому на відстані 2-4 м.
В якості установки можуть бути використані: вимірник заземлення МС-08, польовий потенціометр ЕП-ПМЕ, вимірник питомого опору IKC-1, ІKC-50.
У разі вимірювання питомого опору ґрунту приладом МС-08 відстані між електродами приймаються однаковими i рівними.
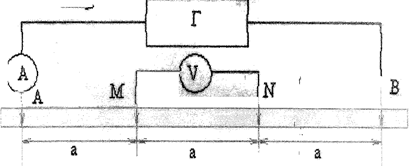
Рисунок 1 – Четырехэлектродная симметричная установка
А, В - токовые электроды;
М, N - потенциальные электроды;
Г - источник тока.
Удельное сопротивление грунта (Ом м) определяется по формуле:
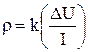
где 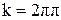 ;
;
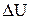 - разность потенциалов, измеренная между приемными
- разность потенциалов, измеренная между приемными
электродами МN, в;
І - величина тока, протекающего через цепь питающих электродов АВ,
Разнос электродов АВ должен отвечать условию 2h 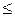 АВ
АВ 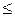 4h
4h
где h – глубина прокладки подземного сооружения
Наприклад величина, корозiйнiй активності ґрунтів по відношенню до сталевих підземних споруд залежно від питомого електричного опору буде:
Питомий опір, Ом м
більше 100 - низька
від 20 до 100 - середня
від 10 до 20 - підвищена
від 5 до 10 - висока
до 5 - дуже висока.
Метод визначення вмісту хлоріонів полягає в титруванні хлор - іонів розчином азотнокислого срібла у присутності хромату калія. Перша крапля надмірного нітрату срібла утворює осад хромату срібла , що офарблює розчин в червоно-бурий колір
NaCI + АgNО3 = AgCl 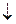 + NаNО3
+ NаNО3
К2С2О4 + АgNО3 = Ag2CrО4 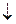 +2 КNО3
+2 КNО3
Вміст хлор - iонiв обчислюють по формулі:
у ґрунті: 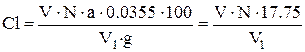 , %
, %
у воді: 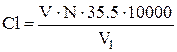 , мiлiграм/л
, мiлiграм/л
де V - об'єм азотнокислого срібла для титрування проби, мл
N - нормальність розчину азотнокислого срібла;
V1 - об’їм витяжки для титрування, мл
g - навішування ґрунту узяте для приготування водної витяжки, г
а - об’їм (загальний ) витяжки, мл
0,03555 - мiлiграм еквівалент хлориона, 35,5 – еквівалент
ЛІТЕРАТУРА
1. Защита подземных металлических сооружений от коррозии. М.:
Стройиздат, 1990, 303с.
2. Защита от коррозии, старения, биоповреждений машин,
оборудования и сооружений. Справочник под ред.
А.А.Герасименко. – М. Металлургия, 1987. т.1, 128с.
ЛЕКЦІЯ №10
ОСОБЛИВОСТІ ВЗАЄМОДІЇ ЗАЛІЗОБЕТОННИХ КОНСТРУКЦІЙ ІЗ СЕРЕДОВИЩЕМ
Залізобетон — комплексний матеріал, в конструкціях з який сталева арматура сприймає звичайно розтягують напруги, а бетон - стискаючі. У традиційних конструкціях бетон виконує роль захисту арматури від корозії і високих температур при можливій пожежі.
Таким чином, в залізобетонній конструкції з навколишнім середовищем безпосередньо стикається бетон. Очевидно, що в агресивних умовах конструкція може бути довговічною, якщо бетон є досить стійкими довгостроково зберігає здатність захищати арматуру.
Відомо, що тонкий наліт іржі, часто наявний на арматурі при бетонуванні, неможливо знайти, якщо і розкрити її, видаливши захисний шар бетону через декілька днів після нормального чи твердіння пропарювання виробу. Іржа зникає, розчиняється в бетоні і звичайно не з'являється знов, незважаючи на те, що бетон, будучи капілярно-пористим гідрофільним тілом, містить вологу і пропускає кисень - речовину, необхідні для електрохімічної корозії стали.
Поява і розвиток корозії арматури через більш менш тривалий час після виготовлення залізобетонної конструкції свідчить про втрату бетоном захисної здатності під впливом навколишнього середовища, "зовнішніх" факторів. Такими факторами можуть бути фізичні, хімічні і фізико-хімічні процеси.
До числа фізичних відносяться такі зовнішні дії, як механічні відколи бетону, ерозійний знос, періодичне нагрівання і охолоджування, заморожування і відтавання, що приводить до руйнування бетону в захисному шарі і оголенню арматури, яка потім корродирує при безпосередньому зіткненні із середовищем.
Хімічні і фізико-хімічні впливи середовища на конструкцію проявляються подвійно: або вони безпосередньо руйнують бетон захисного шару з подальшими оголенням і корозією арматури, або, не руйнуючи бетон безпосередньо, настільки змінюють його рідку фазу, що корозія арматури починається усередині бетону. При цьому її корозія часто йде значно швидше, ніж кородує відкриття сталева конструкція в тих же умовах дії середовища. Це пояснюється тим, що при періодичному зволоженні в захисному шарі бетону і під ним на поверхні арматури плівки вологи, необхідні для електрохімічної корозії стали, зберігаються довше, ніж на поверхні сталевої конструкції.
Продукти корозії, що утворюються, займають в 2-2,5 разу більший обсяг, ніж шар прокородованого металу, і тому тиснуть на навколишній бетон. У бетоні розвиваються розтягуючи напруги, що перевищують його міцність, в результаті утворюються тріщину в захисному шарі, орієнтовані уздовж кородирующих стрижнів. Утворення таких тріщин полегшує доступ агресивних агентів до арматури і прискорює, як правило, її корозію. Надалі, якщо не прийняти міри, розвиток корозії арматури приведе до відколювання захисного шару, при цьому порушиться зчеплення її з бетоном і різко впаде несуча здатність конструкції. Для елементів, що згинаються, втрата несучої здатності від порушення зчеплення арматури з бетоном, складає 30-35%.
Лужне середовище бетону, парова волога якого насичена гідратом окислу кальцію при рН=12-13, сприяє утворенню і збереженню плівок, що пасивують, на сталі, яка при цьому знаходиться в стані підвищеної корозійної стійкості.
При зменшенні рН бетону по тій або іншої причині до 11,8 і нижче пасивність сталі стає меншої, а потім взагалі порушується, оскільки умови вже не сприяють збереженню плівок, що пасивують.
Однією з двох основних причин порушення пасивного стану сталі в бетоні є його нейтралізація кислими газами, зокрема карбонізує. Суть її полягає в поглинанні бетоном з повітря вуглекислого, газу, який, з'єднуючись з гідратом окислу кальцію:
CO2 + Ca(OH)2 ® CaCO3 + H2O,
утворює вуглекислий кальцій. Насичений розчин СаСО3 має рН = 9; зниження рН порової рідини порушує умови стійкості існування гидратірованних мінералів цементного каменя.
Міцність бетону при цьому звичайно не втрачається, хоча при окремих видах цементу відмічене її зниження, але бетон позбавляється здатності пасивувати сталь яка переходить в активний стан і починає корродировати, оскільки капілярно - пориста структура бетону містить воду і пропускає кисень.
Оскільки на Землі практично немає повітря, що не містить вуглекислого газу. (нормальний вміст СО2 в атмосфері 0,03-0,04% карбонізує схильні практично всі наземні конструкції і частково підземні).
Іншою поширеною причиною корозії арматури в бетоні є хлориди. Їх відносять до речовин-активаторів сталі. При деякій невеликій концентрації вони здатні зруйнувати плівки, що пасивують, на поверхні сталі в лужному середовищу бетону. Ця дія пов'язана з підвищеною здібністю хлорид-іонів до адсорбції, внаслідок чого вони витісняють адсорбований кисень, відбувається пробій шару, що пасивує, і починається виразкова корозія сталі.
Для щільних цементних бетонів відсутність первинної дії, що пасивує, як показують дослідження, пов'язана звичайно з наявністю в рідкій фазі іонів-депассиваторів, таких як хлорид-іони, що потрапляють в бетонну суміш у вигляді добавок, у складі заповнювачів цементу з водою. Тому будівельні норми різних країн в тому або іншому ступені обмежують вміст хлоридів в перерахованих складових частинах бетонної суміші, особливо для конструкцій в напружуваній арматурою.
Тому разом з відомими обмеженнями при використовуванні попередньо-напружених конструкцій і підвищеними вимогами до захисного шару велике значення мають розробка і освоєння випуску високоміцних арматурних сталей, зокрема термічно зміцнених, підвищеної стійкості проти корозійного растріскуваня. Наприклад, застосування для виготовлення арматури нержавіючих високолегованих сталей типа X18H10.
Істотне підвищення корозійної стійкості сталевої арматури може бути досягнуте за допомогою металевих захисних покриттів. Найбільш перевіреними і придатними для арматури в багатьох видах бетону і конструкцій є цинкові покриття. Вони застосовуються наприклад, для захисту тканих і зварних сіток, якими армують тонкостінні, армоцементні конструкції, високоміцних арматурних канатів (стрижнів), що натягаються на бетон циліндрових елементів збірних силосних (сінажних) веж.
Найбільш надійним способом захисту залізобетонної, конструкції від дії кислих газів є пониження ступеня агресивності середовища, що досягається зменшенням їх концентрації вогкості атмосфери.
Ступінь агресивної дії газових середовищ на залізобетонні1 конструкції визначається видом, концентрацією, вогкістю і температурою газів. Агресивність газів оцінюється в СНіП II - 28 - 73.
При звичній концентрації вуглекислого газу 600 мг/м (група газів А) і відносної вологості Б більше 75% середовище є слабоагресивним по віднесенні до залізобетонних конструкцій. У цих умовах після карбонізації захисного шару бетону можлива корозія арматури. При періодичному зволоженні бетону конденсатом або атмосферними опадами процес карбонізує сповільнюється, проте корозія арматури в бетоні, що карбонізує, розвиватиметься інтенсивніше. При відносній вологості повітря менше 75% бетон карбонізує швидше, проте сталева арматура в бетоні, що карбонізує, при такій вогкості кородує дуже повільно, а при вологості менше 60% процес корозії практично цілком припиняється. У зв'язку з цим середовища, що містять вуглекислий газ нормальної і підвищеної концентрації при вологості до 60%, є неагресивними.
Якщо в повітрі одночасно мають два і більш агресивних гази, то оцінка виробляється по найбільш агресивному.
Хлор концентрації 1,5 мг/м3 і хлористий водень концентрації 7,5 мг/м3 - відносяться до групи газів В. При вологості до 60% вони роблять слабкий агресивний вплив на залізобетонні конструкції. При вологості більше 75% в суміжних приміщеннях, де відсутнє, виділення тепла з технологічного устаткування і маються мокрі процеси, агресивність середовища при тій же концентрації газів підвищується сильно.
Дата добавления: 2016-07-27; просмотров: 2088;











