СРЕДСТВА СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ, ТЕРАПИИ И ДИАГНОСТИКИ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ 2 глава
Поступивший в лабораторию неконсервированный материал можно хранить при 4 ºС 1...2сут; консервированный в 50%-м растворе глицерина (кусочки органов) — несколько недель; для длительного хранения материал замораживают при —15...—20 °С.
Кровь для серологических исследований у крупного рогатого скота, овец, лошадей берут из яремной вены в стерильные бактериологические пробирки в количестве 10... 15 мл, у свиней — из хвостовой, передней краниальной вен или глазного синуса, у птиц — из подкрыльцовой вен, у кроликов — из краевой ушной вены. Пробирки с кровью необходимо выдержать до формирования сгустка в тепле (1,5...2 ч), затем для отделения от стенок пробирки обвести сгусток стеклянной чистой палочкой или спицей. Для отстаивания сыворотки пробирки с кровью помещают в холодильник при 4...6 °С на 18...20 ч. После ретракции сгустка сыворотку крови переливают в серологические пробирки с резиновыми пробками. При необходимости сыворотку крови консервируют, добавляя в пробирку несколько крупинок борной кислоты, тиомерсал (конечное разведение 1:10 000), или замораживают.
Принципиальная схема микробиологического исследования. Диагностика инфекционных болезней включает в себя комплекс исследований: эпизоотологические, клинические, патологоанатомические, микробиологические. При важности каждого из них и ценности именно комплексного подхода микробиологическое исследование особенно важно, поскольку с его помощью либо непосредственно обнаруживают этиологический (причинный) агент болезни, либо косвенными специфическими иммунологическими методами доказывают его присутствие.
Микробиологическое исследование в принципе состоит из следующих этапов.
1. Обнаружение возбудителя непосредственно в исследуемом
материале без изоляции в виде чистой культуры на питательных
средах. На этом этапе применяют разные методы.
Неиммунологические методы включают в себя: а) выявление возбудителя путем микроскопического исследования окрашенных (по Граму и т. д.) мазков-отпечатков из органов и тканей; б) обнаружение при помощи генетических методов (генные зонды, ПЦР) нуклеиновых кислот возбудителя.
Иммунологические методы заключаются в выявлении антигенов возбудителя с помощью различных серологических реакций (РП, РДП, МФА, ИФА, РИГА и т.д.).
2. Обнаружение возбудителя (его токсинов) в биопробе (заражают исследуемым материалом чувствительных лабораторных животных).
3. Выделение культуры возбудителя из исследуемого материала путем посева на питательные среды.
4. Идентификация выделенной культуры микроорганизмов по совокупности морфологических, тинкториальных, культуральных, ферментативных и патогенных свойств. При этом широко используют серологические (РА, РП, РДП, ИФА и т.д.), а в случае необходимости генетические методы идентификации изолированных микроорганизмов.
5. Серологическая (ретроспективная) диагностика заключается в том, что при помощи различных серологических реакций (РА, РСК, ИФА и т. д.) в сыворотке крови исследуемых животных обнаруживают специфические следы пребывания возбудителя — антитела. Серолбгические реакции наиболее широко применяют при диагностике хронически протекающих бактериозов.
6. Аллергическое исследование в отличие от перечисленных выше методов проводят непосредственно на животных в хозяйстве. При помощи диагностических аллергенов у животных выявляют состояние гиперчувствительности замедленного типа. Аллергическую пробу в основном применяют для иммунологической диагностики хронических бактериозов.
Изложенная схема отражает возможные, но не обязательные направления микробиологических исследований. При каждой конкретной инфекции схему исследования определяют особенности биологии возбудителя и инфекционного процесса.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
1. Освоить методику взятия материала из трупа животного (кролик, морская свинка).
2. Приготовить консервирующие смеси различного типа (глицерин, физиологический раствор, лед и поваренная соль) и провести консервирование материалов различного типа.
3. Освоить технику взятия крови у кролика и получения сыворотки крови.
Контрольные вопросы
1.Какой материал берут прижизненно и какой посмертно у животных для микробиологического исследования?
2.Какие методы консервирования материала применяют для микробиологического исследования?
3.Какова схема микробиологического исследования?
Раздел III
ЧАСТНАЯ МИКРОБИОЛОГИЯ
Тема 22
ЛАБОРАТОРНАЯ ДИАГНОСТИКА СТАФИЛОКОККОЗОВ И СТРЕПТОКОККОЗОВ. БИОПРЕПАРАТЫ
Цель занятия. Ознакомить студентов с этапами лабораторной диагностики, основными свойствами возбудителей стафилоккозов, стрептококкозов и биопрепаратами.
Оборудование и материалы. Культуры S. aureus и S. saprophytics на МПА, кровяном МПА, в МПБ, результаты тестов по определению патогенных свойств стафилококков: ферментация манни-та, плазмокоагулазная, гемолитическая, лецитиназная, ДНК-азная, желатиназная активность, культуры S. pneumoniae, S. agalactiae (или S. pyogenes) на глюкозо-сывороточном МПА, МПБ, на средах Гисса с углеводами, пипетки Пастера; стерильные МПБ и кровяной МПА, красители для окраски по Граму и на капсулы, биопрепараты.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Стафилококкозы. Бактериальные инфекции, вызываемые патогенными стафилококками, характеризующиеся преимущественно гноеродными процессами различной локализации. Проявляются в виде абсцессов, флегмон, маститов, метритов, пневмоний, сепсиса. Токсигенные штаммы стафилококков могут вызывать пищевые отравления у людей.
Возбудитель стафилококкозов: в основном штаммы S. aureus, реже S. epidermidis и некоторые другие виды рода Staphylococcus, семейства Micrococcaceae.
Лабораторная диагностика стафилококкозов основана на результатах бактериологического исследования.
Бактериологическое исследование включает в себя обнаружение возбудителя в исходном материале методом световой микроскопии, выделение чистой культуры посевом на питательные среды и идентификацию возбудителя по культурально-морфологическим, ферментативным, серологическим, а также токсигенным признакам (методом биопробы).
Материал для исследования. Для прижизненной диагностики берут раневой экссудат стерильными ватными тампонами, содержимое абсцессов отбирают стерильным шприцем, при маститах материалом служит секрет вымени.
Микроскопия препаратов из исходного материала. Мазки окрашивают по Граму и на капсулу, микроскопируют. Клетки стафилококков грамположительные, сферической формы, диаметром 0,5... 1 мкм, располагаются в виде скоплений неправильной формы, а также единично, парами и цепочками из трех-четырех клеток (рис. 72), спор нет, вирулентные штаммы могут образовывать капсулу.
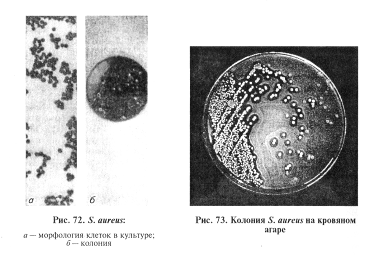
Выделение и идентификация культуры возбудителя. Стафилококки — факультативные анаэробы, температурный оптимум 30...37 ºС, рН 7,2...7,4, к питательным средам неприхотливы, могут расти при повышенном содержании хлорида натрия. Исследуемый материал высевают на МПА, в МПБ, посевы культивируют в условиях обычной атмосферы. При загрязнении материала посторонней микрофлорой используют питательные среды с селективными свойствами: солевые МПА, МПБ (8...10% хлорида натрия), желточно-солевой агар (ЖСА), 3,5%-й МПА с добавлением 3 мл 0,1%-го раствора кристаллвиолета (на этой среде патогенные стафилококки образуют колонии фиолетового или оранжевого цвета). Широко используют посев исходного материала на кровяной МПА.
На плотных средах через 18...24ч инкубирования вырастают колонии правильной круглой формы, выпуклые, с гладкой поверхностью, ровными краями, диаметром 2...7мм, непрозрачные. Цвет колоний зависит от типа вырабатываемого пигмента. S. aureus синтезирует золотистый и белый пигмент. На кровяном МПА вирулентные штаммы обычно растут, формируя широкую зону бета-гемолиза (рис. 73). На ЖСА вокруг колоний стафилококков, обладающих лецитиназной активностью, образуются зоны помутнения с перламутровым оттенком. В МПБ рост стафилококков сопровождается интенсивным помутнением среды и образованием значительного осадка.
Из культур, выросших на питательных средах, готовят мазки, окрашивают по Граму и микроскопируют. При обнаружении бактерий с типичными для стафилококков культурально-морф-логическими признаками приступают к изучению свойств, прямо или косвенно свидетельствующих о патогенности выделенного стафилококка.
Патогенные стафилококки в отличие от непатогенных образуют капсулу (S. aureus), выделяет гемолизин, фибринолизин (стафилокиназу), гиалуронидазу, плазмокоагулазу, желатиназу, ДНК-азу, лецитиназу, ферментируют маннит. Методы выявления этих факторов патогенности изложены в теме 13. Важнейшим из перечисленных факторов считают плазмокоагулазу: у 90...95 % плазмокоагулирующих стафилококков выражена способность продуцировать энтеротоксин.
Протеин А также рассматривают как фактор патогенности стафилококков. Этот белок, находясь в составе клеточной стенки, связывает Fc-фрагменты IgG, что способствует снижению эффективности фагоцитоза. Для выявления протеина А смешивают суспензию эритроцитов, сенсибилизированных IgG, и клетки исследуемой культуры стафилококка. При наличии белка А стафилококки соединяются с иммуноглобулинами и вызывают агглютинацию эритроцитов.
Биопроба. Заражают лабораторных животных для подтверждения токсигенных свойств выделенного стафилококка.
Летальный токсин выявляют внутривенным введением кролику фильтрата бульонной культуры 0,75 мл на 1 кг массы.
Некротоксин обнаруживают внутрикожной пробой. Готовят суспензию суточной культуры в физиологическом растворе с концентрацией клеток 4,2 • 109/мл и 1 *109/мл. Каждое разведение культуры по 0,1 мл вводят внутрикожно кролику, предварительно удалив шерстный покров на месте инъекции. Результаты учитывают ежедневно на протяжении 4...5сут. В положительных случаях развивается некроз кожи.
Энтеротоксин продуцируют токсигенные штаммы. Пробу на энтеротоксин ставят при отравлениях. Культуру стафилококка выращивают на специальной питательной среде (пептон, хлорид кальция, хлорид магния, дигидрофосфат калия, 0,8 % агар-агара, рН 7,2), в атмосфере, содержащей 20 % оксида углерода (IV), в течение трех суток. Затем культуру стерилизуют фильтрованием, 10...15 мл фильтрата смешивают с равным объемом молока и скармливают 4...8-недельным котятам. При наличии энтеротоксина через 1..2ч у животных возникают симптомы гастроэнтерита и рвота.
Стрептококкозы. Инфекционные болезни, вызываемые бактериями рода Streptococcus, к которому относят 29 видов. Наибольшее значение в патологии сельскохозяйственных животных имеют следующие виды: S. pneumoniae — возбудитель стрептококковой (диплококковой) септицемии молодняка сельскохозяйственных животных; S. equi, включающий в себя три подвида: S. equi subsp. equi — возбудитель мыта лошадей; S. equi subsp. equisimillis и S. equi subsp. zooepidemicus, который вызывает септические инфекции у других видов животных; S. agalactiae и S. dysagalactiae — этиологические агенты маститов крупного рогатого скота; S. pyogenes — возбудитель ряда заболеваний, преимущественно человека. Многие стрептококки, патогенные для животных, пока идентифицированы на уровне серологической группы и не получили видовых наименований.
Лабораторная диагностика стрептококкозов основана на результатах бактериологического исследования.
Бактериологическое исследование включает в себя обнаружение возбудителя в исходном материале методом световой микроскопии, выделение чистой культуры посевом на питательные среды или методом биопробы, идентификацию возбудителя по культурально-морфологическим, ферментативным, серологическим и патогенным признакам (методом биопробы).
Материал для исследования. При подозрении на мыт прижизненно берут носовые истечения, содержимое абсцессов лимфатических узлов (путем пункции), для посмертной диагностики — кровь из сердца, части печени, селезенки, легких. При стрептококковых маститах исследуют молоко, при подозрении на септические стрептококкозы (диплококковая инфекция и др.) — кровь из сердца, селезенку, печень, костный мозг, носовые истечения.
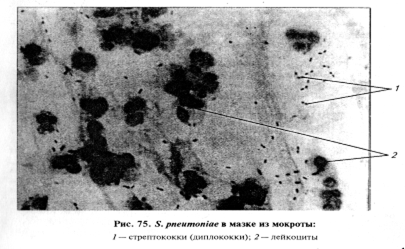
Микроскопия препаратов из исходного материала. Мазки окрашивают по Граму и на капсулу, микроскопируют. Все стрептококки представляют собой сферические или овальные грамполо-жительные клетки диаметром 0,5...1,25 мкм, без спор и жгутиков, с тенденцией к образованию цепочек различной длины (рис. 74, 75). Морфология стрептококков некоторых видов в препаратах из патологического материала несколько отличается. У S. pneumoniae клетки обычно парные, окруженные капсулой, концевые части клеток слегка удлинены, поэтому данный стрептококк ранее называли ланцетовидным диплококком. Клетки S. pneumoniae также могут располагаться единично и короткими цепочками. S. equi в мазках из гноя обнаруживают в виде длинных цепочек, причем клетки в цепочке как бы сплющены в горизонтальной плоскости, образуют капсулу; в мазках из культуры клетки S. equi чаще располагаются короткими цепочками, единично, парами. S. agalactiae и S. pyogenes в препаратах из материала чаще
обнаруживают в виде цепочек.

Выделение и идентификация культуры возбудителя. Стрептококки — факультативные анаэробы, температурный оптимум 37 °С (диапазон 25... 45 °С). На общепринятых питательных средах растут плохо, обычно используют обогащенные среды: МПБ с 1 % глюкозы и 10 % инактивированной сыворотки крови лошади, МПА с 1 % глюкозы и 5 % крови барана или кролика. Для выделения культуры возбудителя исследуемый материал высевают на указанные питательные среды и культивируют 18...24 ч.
 На глюкозо-кровяном МПА все виды патогенных стрептококков образуют мелкие колонии, чаще с зоной гемолиза. У S. pneumoniae колонии круглые, полупрозрачные, плоские, с приподнятым центром и краями, с зоной гемолиза типа «альфа»; в МПБ растет с равномерным помутнением среды. S. equi формирует мелкие, росинчатые, слизистые, правильной круглой формы колонии с узкой зоной бета-гемолиза, позднее они становятся серо-белыми, непрозрачными; в МПБ растет с помутнением среды, образованием пушистых хлопьев, через 3...5 сут культивирования бульон просветляется, на дне пробирки образуется осадок. У S. agalactiae (S. dysagalactiae) мелкие, сероватые, просвечивающие колонии с бета- или двойной зоной альфа-гемолиза, при росте в МПБ среда остается прозрачной, формирующиеся крупинки оседают на дно пробирки. S. pyogenes на кровяном МПА образует мелкие, прозрачные, правильной круглой формы колонии с зоной бета-гемолиза, в бульоне растет с просветлением среды и выпадением зернистого осадка.
На глюкозо-кровяном МПА все виды патогенных стрептококков образуют мелкие колонии, чаще с зоной гемолиза. У S. pneumoniae колонии круглые, полупрозрачные, плоские, с приподнятым центром и краями, с зоной гемолиза типа «альфа»; в МПБ растет с равномерным помутнением среды. S. equi формирует мелкие, росинчатые, слизистые, правильной круглой формы колонии с узкой зоной бета-гемолиза, позднее они становятся серо-белыми, непрозрачными; в МПБ растет с помутнением среды, образованием пушистых хлопьев, через 3...5 сут культивирования бульон просветляется, на дне пробирки образуется осадок. У S. agalactiae (S. dysagalactiae) мелкие, сероватые, просвечивающие колонии с бета- или двойной зоной альфа-гемолиза, при росте в МПБ среда остается прозрачной, формирующиеся крупинки оседают на дно пробирки. S. pyogenes на кровяном МПА образует мелкие, прозрачные, правильной круглой формы колонии с зоной бета-гемолиза, в бульоне растет с просветлением среды и выпадением зернистого осадка.
На следующем этапе из выделенных культур готовят мазки, окрашивают по Граму, микроскопируют. При обнаружении типичных по морфологии и тинкториальным свойствам клеток бактерий переходят к следующему этапу.
Чтобы исключить стафилококковую, энтерококковую (род Enterococcus) инфекции, чистую культуру исследуют в нескольких пробах. Ставят тест на каталазу — стафилококки образуют ката-лазу, стрептококки нет. С целью дифференциации пиогенных гемолитических стрептококков от энтерококков культуры высевают в МПБ, содержащий 40 % желчи крупного рогатого скота, МПБ с 6,5 % хлорида натрия. Энтерококки в отличие от гноеродных стрептококков растут на этих средах. Также проверяют чувствительность клеток культуры к желчи: в пробирку с МПБ, содержащим 10 % желчи крупного рогатого скота, вносят 0,5 мл исследуемой суточной бульонной культуры и выдерживают при 37 °С 1 ч. При лизисе содержимое пробирки просветляется, энтерококки не лизируются.
Параллельно изучают ферментативные свойства стрептококков (табл. 18).


Серогрупповую принадлежность выделенного микроба определяют в реакции преципитации. В РП используют стрептококковые групповые преципитирующие сыворотки. Исследуемую культуру выращивают в МПБ в течение 18...20 ч, затем 7...9 мл культуры центрифугируют, надосадочную жидкость удаляют, к осадку добавляют 0,3...0,4 мл 0,2 н. раствора соляной кислоты, осадок суспендируют, взвесь прогревают в кипящей водяной бане 10 мин, охлаждают, добавляют каплю 0,04%-го спиртового раствора фенолфталеина и нейтрализуют 0,2 н. раствором гидро-ксида натрия. Жидкость приобретает бледно-розовый цвет. Затем смесь вновь центрифугируют и надосадочную жидкость, содержащую термостабильный полисахаридный антиген С, используют как антиген для постановки реакции кольцепреципитции. По классификации Ленсфильд стрептококки на основании антигенных свойств полисахарида С можно отнести к той или иной серологической группе: А, В, С, D и т.д. S.pneumoniae не содержит серогрупповой полисахарид, но является антигенно-гетерогенным видом, который дифференцируют на типы в РА.
Биопроба. У выделенных культур стрептококков определяют патогенные свойства в биопробе на белых мышах. Для заражения используют только свежевыделенные штаммы в виде 18...20-часовых бульонных культур, которые по 0,5 мл вводят внутрибрюшинно трем мышам. Культуру признают патогенной при гибели не менее двух мышей.
В случае инфекции, вызываемой S. pneumoniae, практикуют выделение возбудителя из исследуемого материала методом биопробы. С этой целью тканевую суспензию, разведенную стерильным физиологическим раствором в соотношении 1:2, вводят внутрибрюшинно белым мышам по 0,5 мл. В положительных случаях мыши погибают через 1...2 сут.
Биопрепараты. Вакцину против диплококковой септицемии телят, ягнят и поросят готовят из штаммов S. pneumoniae, выделенных от указанных видов животных. Культуры выращивают на полужидком агаре, инактивируют 0,4%-м раствором формалина, проверяют на стерильность, безвредность (на морских свинках), активность (на белых мышах).
Ассоциированная (поливалентная) вакцина против паратифа, пастереллеза и диплококковой септицемии поросят включает в себя кроме P. multocida и S. cholerasuis бактериальную массу S. pneumoniae.
Сыворотку против диплококковой септицемии телят, ягнят и поросят получают гипериммунизацией волов убитыми и живыми культурами возбудителя.
Инактивированные вакцины из стрептококков серологической группы С.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
1. Приготовить мазки из культур стафилококков, стрептококков, окрасить по Граму, промикроскопировать, зарисовать.
2. Описать культуральные свойства стафилококков и стрептококков.
3. Изучить ферментативные свойства стафилококков и стрептококков.
4. Ознакомиться с биопрепаратами.
Контрольные вопросы
1. По каким критериям дифференцируют патогенные и непатогенные стафилококки?
2. Каковы основные виды патогенных стрептококков?
3.По каким критериям дифференцируют гноеродные гемолитические и фекальные стрептококки?
4.Каковы культуральные, морфологические и тинкториальные свойства стрептококков?
5.Какие биопрепараты выпускают против диплококковой септицемии молодняка сельскохозяйственных животных?
Тема 23
ЛАБОРАТОРНАЯ ДИАГНОСТИКА РОЖИ СВИНЕЙ И ЛИСТЕРИОЗА. БИОПРЕПАРАТЫ
Цель занятия. Ознакомить студентов с этапами лабораторной диагностики и свойствами возбудителей рожи свиней, листериоза, биопрепаратами.
Оборудование и материалы. Культуры вакцинных штаммов возбудителя рожи свиней и листериоза на МПА, в МПБ с индикаторными бумажками на сероводород, культуры на средах Гисса с углеводами, перекись водорода, реактив Эрлиха, стерильные МПА, МПБ в пробирках, пипетки Пастера, трупы мышей, павших после заражения вакцинными штаммами возбудителей, инструменты для вскрытия трупов животных, люминесцентный микроскоп, люминесцирующие сыворотки листериозные и рожистые, биопрепараты.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Рожа свиней. Инфекционная болезнь, преимущественно свиней в возрасте З...12мес. Спорадически встречается у крупного рогатого скота, ягнят, пушных зверей, грызунов, птицы; восприимчив человек. Болезнь протекает остро и хронически. Острое течение характеризуется признаками септицемии, воспалительной эритемой, хроническое — эндокардитами и артритами.
Возбудитель рожи свиней — бактерия Erysipelothrix rhusiopathiae, род Erysipelothrix.
Лабораторная диагностика рожи свиней основана на результатах бактериологического исследования.
Бактериологическое исследование включает в себя обнаружение возбудителя в исходном материале методом световой и люминесцентной микроскопии, выделение чистой культуры посевом на питательные среды и методом биопробы и идентификацию возбудителя по культурально-морфологическим, ферментативным, серологическим и патогенным признакам.
Материал для исследования. В лабораторию направляют труп животного целиком или сердце (при хроническом течении обязательно), печень, селезенку, почку, трубчатую кость. Материал не консервируют или помещают в стерильный 30%-й раствор глицерина.
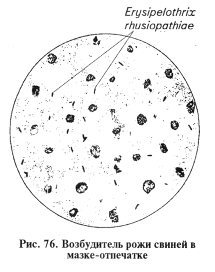
Микроскопия препаратов из исходного материала. Возбудитель представляет собой прямую или слегка изогнутую тонкую палочковидную грамположительную бактерию без спор, капсул и жгутиков размером (0,2...0,3) х (0,8...2,5) мкм (рис. 76). Мазки-отпечатки из органов окрашивают по Граму и противорожистой люминесцирующей сывороткой. В положительных случаях в материале находят мелкие грамположительные палочки, располагающиеся одиночно, попарно или в виде скоплений. В препаратах из пораженных клапанов сердца при хроническом течении болезни возбудитель обнаруживают в форме нитей. В мазках, окрашенных люминесцирующей сывороткой, в положительных случаях находят светящиеся клетки бактерий типичной морфологии.
Выделение и идентификация культуры возбудителя. Возбудитель рожи — факультативный анаэроб, в первых генерациях ведет себя как микроаэрофил. Температурный оптимум 36...37 °С, рН 7,2...7,5. С целью выделения культуры возбудителя исследуемый материал засевают в МПБ или на МПА. Посевы культивируют 24...48 ч.
В МПБ возбудитель растет с очень слабым помутнением питательной среды, без образования пристеночного кольца или поверхностной пленки, через 48...72ч среда просветляется, на дне пробирки формируется незначительный осадок, поднимающийся при встряхивании в виде облачка. На плотных средах возбудитель образует мелкие росинчатые колонии (S-форма), иногда крупные, с неровными краями и поверхностью (R-форма). Посевы на плотных средах из-за малых размеров колоний лучше просматривать при помощи лупы. Из культур, выросших на питательных средах, готовят и микроскопируют мазки, окрашенные по Граму и люминесцирующей сывороткой. При обнаружении бактерий, типичных для возбудителя рожи свиней по морфологическим, тинкториальным и культуральным свойствам, у выделенных культур изучают ферментативные, серологические и патогенные свойства.
Возбудитель рожи разлагает с образованием кислоты без газа глюкозу, лактозу, галактозу, мальтозу; не ферментирует эскулин, сахарозу, маннит, дульцит, рамнозу; не образует каталазу, индол; выделяет сероводород; не растет в МПБ с 8,5 % хлорида натрия; вирулентные штаммы синтезируют гиалуронидазу.
Вид Е. rhusiopathiae подразделяют на 22 серовара, которые обозначают цифрами. Наиболее распространены серовары 1-й и 2-й, которые ранее обозначали А и В. Для видовой серологической идентификации на практике используют обычную лечебно-профилактическую противорожистую сыворотку (см. «Биопрепараты»).
На предметное стекло наносят каплю иммунной сыворотки, разведенной физиологическим раствором (1:50), в которой затем тщательно суспендируют бактериологической петлей суточную агаровую исследуемую культуру. Через 1...2мин учитывают результат: возбудитель рожи агглютинирует в сыворотке.
Биопроба. Метод применяют для изоляции возбудителя из исследуемого материала, а также для определения патогенных свойств выделенных культур бактерий. Тканевый материал измельчают в ступке со стерильным физиологическим раствором в соотношении 1:10 и вводят подкожно по 0,1...0,2 мл белым мышам массой 16...18 г. При наличии возбудителя животные погибают через 2...4сут после заражения. Заражение мышей слабовирулентными культурами, например выделенными от свиней с хроническим течением болезни, может приводить к гибели животных в более поздние сроки или не вызывать летального исхода. Материал из трупов мышей подвергают бактериологическому исследованию.
Биопрепараты. Концентрированная гидроокисьалюминиевая формолвакцина против рожи свиней содержит культуры возбудителя серовара В, выращенные в бульоне Хоттингера, инактивированные формалином, сорбированные на гидроксиде алюминия. После формирования осадка вакцину концентрируют, сливая треть надосадочной жидкости. Вакцину контролируют на стерильность, безвредность и активность (на голубях).
Депонированная вакцина против рожи свиней представляет собой живую культуру матрикса Конева, сорбированную на гидроксиде алюминия. Вакцину контролируют на чистоту роста, безвредность и остаточную вирулентность (считают пригодной для использования, если вакцина безвредна для голубей и вирулентна для мышей).
Сухая живая вакцина против рожи свиней ВГНКИ из штамма ВР-2 представляет собой лиофильно высушенную культуру вакцинного штамма ВР-2. Вакцину контролируют на чистоту роста, концентрацию микробных клеток (5*109/мл), безвредность и активность на белых мышах. Так же готовят жидкую вакцину из штамма ВР-2.
Лечебно-профилактическую сыворотку против рожи свиней получают гипериммунизацией свиней; контролируют на стерильность, безвредность и активность на белых мышах и признают активной, если она предохраняет от гибели мышей в дозах 0,01...0,02 и 0,03 мл.
Сухие рожистые люминесцирующие сыворотки для прямого метода иммунофлуоресценции предназначены для серологической идентификации возбудителя непосредственно в материале и в культуре.
Листериоз. Бактериальная инфекция сельскохозяйственных животных многих видов, грызунов, птиц и человека. Характеризуется поражением центральной нервной системы, репродуктивных органов (аборты), молочной железы (маститы), признаками септицемии. Протекает остро и хронически.
Возбудитель листериоза — бактерия Listeria monocytogenes, род Listeria.
Лабораторная диагностика листериоза основана на результатах бактериологического исследования, в отдельных случаях применяют серологическую диагностику.
Бактериологическое исследование включает в себя обнаружение возбудителя в исходном материале методами световой и люминесцентной микроскопии и биопробы, выделение чистой культуры посевом на питательные среды и идентификацию возбудителя по культурально-морфологическим, ферментативным, серологическим и патогенным признакам (методом биопробы).
Материал для исследования. В лабораторию направляют трупы мелких животных (целиком), от крупных животных: голову (головной мозг), печень, селезенку, почки, пораженные участки легких; для прижизненной диагностики — абортированный плод с оболочками, истечения из половых органов, секрет пораженной доли вымени, в случае необходимости кровь или сыворотку крови от больных или подозреваемых в заболевании животных.
Микроскопия препаратов из исходного материала. Возбудитель представляет собой грамположительную палочковидную бактерию с закругленными концами, без спор, размером 0,5...2мкм (рис.77). Листерии при 20.-.22*С, но не при 37...38 °С образуют жгутики. При выращивании на сывороточных средах формируют капсулу. Из исследуемого материала готовят и микроскопируют мазки, окрашенные по Граму, а также флуоресцирующими лис-териозными сыворотками. В тканевом материале листерии обнаруживают в виде грамположительных, нередко полиморфных палочек, располагающихся одиночно, парами, напоминающими римскую цифру пять, или по нескольку штук параллельно.
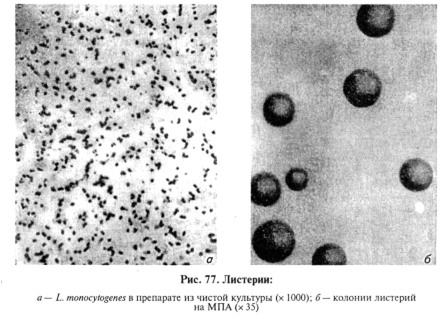
Выделение и идентификация культуры возбудителя. Листерии — факультативные анаэробы, температурный оптимум 36...38 "С, диапазон 4...45 "С, способны расти на средах с повышенным содержанием хлорида натрия. Посевы из исследуемого материала делают в МПБ или печеночный бульон и на агар с добавлением глюкозы (1%) и глицерина (2...3%), на кровяной агар. При исследовании загрязненного материала используют среды с селективными свойствами: МПА с теллуритом калия и полимиксином, среды, содержащие 10 % хлорида натрия. Для увеличения концентрации возбудителя в исследуемом материале рекомендуют часть материала хранить при 4°С до 30 сут. При получении отрицательных результатов в первичных посевах следует с интервалом 10 сут делать повторные высевы на среды, что увеличивает вероятность выделения возбудителя. Посевы инкубируют при 37 °С до двух недель.
На плотных питательных средах возбудитель растет в виде мелких росинчатых колоний, в косопроходящем свете — голубоватого цвета с зеленоватым оттенком и мелкозернистой структурой; на кровяном агаре вокруг колоний некоторых штаммов образуется зона бета-гемолиза. В МПБ рост возбудителя характеризуется слабым помутнением среды, через 5...7 дней на дне пробирки образуется слизистый осадок.
Дата добавления: 2016-07-22; просмотров: 2422;











