Химические свойства
Основные свойства у хинолина и изохинолина выражены слабо. С сильными кислотами образуют соли хинолиния и изохинолиния:

Электрофильное присоединение. Этот тип реакций протекает по гетероатому азота с образованием четвертичных солей:

Электрофильное замещение. Необходимым условием электрофильного замещения (по атому углерода бензольного кольца) является наличие положительного заряда на гетероатоме азота. Это значит, что гетероатом азота должен быть протонирован или же его неподелённая электронная пара должна быть связана иным образом.
При использовании нитрующей смеси (смесь HNO3 и H2SO4) при 0°С образуются примерно равные количества 5-нитро- и 8-нитрохинолинов, а в более жестких условиях образуются 5,7-динитро- и 6,8-динитрохинолины:

Нитрование азотной кислотой в уксусном ангидриде приводит к 3-нитрохинолину:

Бромирование хинолина в сернокислом растворе и в присутствии сульфата серебра приводит к образованию примерно равных количеств 5-Br (51%) и 8-Br (49%) хинолинов.
Нуклеофильное замещение. Аминирование по положению 2 с выходом до 80% 2-аминохинолина (реакция Чичибабина) можно осуществлять амидом натрия в жидком аммиаке под высоким давлением и при комнатной температуре.

При нагревании хинолина с гидроксидом калия до 2500С происходит гидроксилирование по положению 2:

Реакции аминирования и гидроксилирования хинолина могут протекать также по положению С-4.
Гидрирование в первую очередь протекает по пиридиновому гетероциклу и приводит к тетрагидрохинолину:
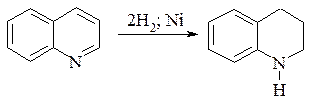
Окисление. При высокой температуре сильные окислители разрушают ароматическое ядро и образуются соответствующие пиридиндикарбоновые кислоты:

Гомологи окисляются легко с образованием соответствующих хинолинкарбоновых кислот:

Дата добавления: 2020-10-01; просмотров: 691;











