Синморфология сообществ
Сообщества микроорганизмов формируют морфологически определенные образования. При рассмотрении синморфологии микробных сообществ разного происхождения можно отметить принципиальные черты сходства. Они обусловлены общими требованиями к топографии системы.
Во-первых, продуцентами являются фототрофы, и, следовательно, сообщество должно иметь поверхность, развернутую к свету.
Во-вторых, в сообществе должна осуществляться регенерация биогенных элементов из некромассы продуцентов, находящихся вне фотосинтезирующего слоя. Это осуществляется бактериями-деструкторами, образующими сложную трофическую сеть.
В-третьих, внутри такого сообщества образуются геохимические барьеры — окислительный, щелочной, сероводородный. Если на сообщество накладывается поток вещества,— а этот приток необходим для поддержания сообщества вследствие неполной замкнутости циклов,— то балластные элементы могут осаждаться на барьерах, приводя к литификации (затвердевание, литос - камень) сообщества, образованию биогенной породы.
Последовательность реакций фотосинтеза и этапов деструкции допускает их пространственное разделение. Связь между ними осуществляется транспортом вещества. Поэтому в сообществе могут создаваться слои с преимущественным развитием микроорганизмов, имеющих определенную физиологическую функцию. При этом в сообществе возникают микрозоны, иногда характеризующиеся отложением того или иного минерала. Особенно наглядны отложения минералов железа — окисного, сульфидного, магнетита. Таким образом, происходит образование биогенных горных пород, отражающих структуру микробного сообщества чередованием слоев минералов.
3.3 Кооперативные взаимоотношения микробов в сообществе
Кооперативные трофические взаимоотношения в сообществе могут быть рассмотрены по списку веществ, поступающих как субстраты, и списку продуктов, образуемых в этом блоке. Наиболее наглядны кооперативные отношения в разнообразной группе органотрофов, осуществляющих деструкционную ветвь в цикле углерода.
Осуществляемая микроорганизмами химическая реакция должна обеспечить достаточную энергию для существования организма. В трофической системе микробного сообщества образуется сеть взаимосвязанных химических реакций.
Под сообществом мы понимаем набор организмов, занимающих определенные фундаментальные ниши в экосистеме и связанных между собой трофическими взаимоотношениями. Среди этого набора типов взаимоотношений нас интересуют те, которые приводят к формированию микробного сообщества как, способного взаимодействовать со средой обитания как некое кооперативного целого единство. Прежде всего, сообщество как целое должно соответствовать требованиям термодинамики и в данных условиях обитания обеспечивать необходимую энергию всем своим компонентам. Для бактерий и их сообществ термодинамика осуществляемых ими химических процессов играет определяющую роль. Доминировать будут только те организмы, кинетические характеристики которых более всего соответствуют условиям, складывающимся в сообществе.
Микроорганизмы получают энергию для своей жизнедеятельности от окислительно-восстановительных реакций, представляющих перенос электрона от донора к акцептору. Микробиологам такие расчеты особенно удобны для выяснения обмена литотрофных организмов. Общее правило такое: хемалитотрофный организм может развиваться в области термодинамической устойчивости продукта энергодающей реакции. Однако работает и обратная закономерность: в местообитании сообщества, создающего определенные Eh-pH условия, химические соединения переходят в формы, соответствующие области их устойчивости в так называемых биологически опосредованных реакциях.
Для сообщества действует закон Гесса, согласно которому для системы сопряженных реакций важна только разность между исходным и конечным состояниями. При этом допускается множество путей между исходными субстратами и конечными продуктами, лишь бы выход энергии был достаточен. Тот же закон действует и для системы реакций внутри клетки. Однако для сообщества имеется ограничение, заключающееся в том, что для каждого вида, входящего в метаболическую систему сообщества, выход энергии должен быть достаточен для его существования. Таким образом, в многоступенчатой системе реакций деструкции органического вещества каждая ступень, осуществляемая видом микроорганизмов, должна быть выше некоторого минимального уровня.
Для того чтобы реакция могла быть энергодающей, во-первых, выход энергии должен быть достаточен для синтеза АТФ, в том числе и за счет протонного насоса, во-вторых, плотность потока вещества должна быть достаточна для поддержания популяции соответствующих организмов, т. е. их урожай для данной реакции должен обеспечить поддержание популяции организмов вопреки их естественному отмиранию и гибели. Если поток энергии от реакции превращения определенного вещества через локальное местообитание организмов недостаточен для поддержания популяции, то маловероятно и существование специализированной группы организмов.
Сообщество, осуществляющее замкнутый цикл (точнее, замкнутые по биогенным элементам циклы) является автономным и способно развиваться в течение длительного, даже в геологических масштабах, времени. Это достигается взаимодействием различных по функциям организмов, составляющих сообщество.
При рассмотрении цепи реакций важно заметить, что в условиях сообщества концентрация промежуточных метаболитов снижается до минимума, обусловленного их потреблением следующим в цепи организмом.
3.4 Первичная продукция органических веществ
Первый этап в сообществе осуществляют первичные продуценты — автотрофы, ассимилирующие СО2 и, таким образом, представляющие четко очерченную на биохимическом уровне группу. В подавляющем большинстве случаев это оксигенные фотоавтотрофы, представленные физиологически узкими группами цианобактерий, водорослей, высших растений. Оксигенные фототрофы определяют вход в систему биогеохимических циклов реакциями синтеза биомассы и образования кислорода. Они конкурируют между собой за свет, воду, биогены. Фототрофный путь питания обусловлен ограничением фотосинтетически активной радиацией (ФАР), спектральный состав которой различается для разных групп организмов в зависимости от дополнительного набора пигментов. Нерегулярное поступление света, зависящее от сезона, времени суток и погоды, обусловливает необходимость для фототрофов первоначального накопления ассимилятов в запасных веществах, как полиглюкоза или жиры. Отсюда возникает возможность формирования клеток больших размеров.
Для фототрофов не представляют первостепенной необходимостью высокая интенсивность обмена с окружающей средой, потому что они обладают возможностью запасания веществ: фосфаты в форме полифосфатов; азот в форме цианофицина (полимера аргинина и аспаргиновой кислоты). Вследствие чего кинетика роста фототрофов более зависит от общего содержания питательных веществ в системе «клетки + среда».
Первичные продуценты, осуществляющих практически весь вход энергии в экосистему, ограничены конструктивным обменом, анаболизмом, и синтезом биомассы. Вторым продуктом реакции после биомассы является кислород. Выделение О2 определяет формирование окислительной зоны для аэробов.
3.5 Деструкция органических веществ
Вторую часть цикла составляет деструкция, возвращающая первичным продуцентам-автотрофам исходные вещества за счет их минерализации. Деструкцию осуществляют прежде всего микроорганизмы; животные-консументы в наземных экосистемах ответственны лишь за 3% круговорота углерода. В микробных сообществах почвы, морских экосистемах системах цикл деструкции орган. в.в. можно полагать замкнутым за счет реакции дыхания, обратной оксигенному фотосинтезу:
 [СН2О] + О2 СО2 + Н2О,
[СН2О] + О2 СО2 + Н2О,
осуществляется частично прямо консументами зоопланктона, частично многоступенчато под действием бактерий.
Трофическая структура микробного сообщества определяется взаимодействиями между функциональными группами микроорганизмов, обладающих специализированными наборами ферментов, дающими им возможность использовать те или иные вещества. Допустим, что рассматриваемое микробное сообщество получает в качестве субстрата мортмассу фотоавтотрофов, состоящую из белков, жиров, углеводов и других соединений клеток.
Соответственно трем основным компонентам мортмассы рассматриваются пептолитический, липолитический, сахаролитический пути. Согласно первому постулату Виноградского, «функции микробов в природе специализированы; для каждой работы есть свой специалист, приспособивший к ней весь химизм своего существования», каждый путь обслуживается своей функциональной группой организмов.
Первый этап деструкции представляет гидролиз, осуществляемый бактериями-гидролитиками. Стратегией гидролитиков является заселение поверхности субстрата, и их развитие прямо зависит от доступной поверхности. Бактерии-гидролитики переводят вещества твердой фазы в раствор, гидролизуя их вне клетки под действием соответствующих экзоферментов-гидролаз, соответственно протеаз, липаз, целлюлаз. Общая картина гидролиза сводится к появлению вместо индивидуальных полимеров унифицированных мономеров, поступающих в общий резервуар растворенных веществ.
Низкомолекулярные соединения поступают в клетки бактерий-осмотрофов и окисляются в зависимости от доступного окислителя. Особое место среди продуктов деструкции занимает ацетат, образующийся из большинства соединений и поступающий для окончательного окисления в С2-метаболическом пути в сообществе.
Таким образом, деградация мортмассы дает возможность существования нескольких специализированных групп организмов:
· гидролитиков,
· диссипотрофов, использующих низкомолекулярные соединения,
· вторичных окислителей, использующих конечные продукты обмена.
Возникает вопрос, зачем столько разных специалистов, не может ли все эти реакции осуществить один организм, последовательно адаптируясь к использованию сначала наиболее доступных веществ, а затем труднее разлагаемых? Такой процесс известен для чистых культур, использующих набор субстратов, и носит название диауксии. В сообществе, однако, времени для адаптации нет, и вещество, используемое с запозданием, съест другой организм.
Организация трофической системы микробного сообщества складывается таким образом, что для каждого соединения есть свой специалист.
3.6 Межвидовой перенос водорода и синтрофия
Помимо прямого окисления ЛЖК вторичными анаэробами, существует иной термодинамически возможный процесс разложения этих соединений, обусловленный бинарным взаимодействием между группами микроорганизмов.
Принципиальным открытием в этой области было катаболической синтрофии, под которой подразумевалось осуществление реакции катаболизма только в случае взаимодействия двух организмов. Явление катаболической синтрофии означает, что сообщество микроорганизмов можно и следует рассматривать как биологическое единство, обусловленное термодинамическими возможностями совокупности его компонентов.
Наиболее ясно дело обстоит с водородом. История такова. В 1936 г. Г. Баркер (Н. Barker) описал под названием «Methanobacillus omelianskii» споровый организм, который образовывал метан из этанола. Потом в Калифорнии ученица Баркера описала еще ряд культур метаногенов, которые превращали в метан органические кислоты (бутират, пропионат). Таким образом, была, казалось бы, решена задача описания биологического процесса метанового сбраживания органических кислот, который с очевидностью наблюдался на практике при метаногенезе. В 1970-х гг. с развитием строго анаэробной техники было подтверждено утверждение Н. Зёнгена, что большинство метанобразующих бактерий использует водород и есть только два организма, способных использовать ацетат, Methanosarcina и Methanothrix (Methanosaeta). Было доказано, что на самом деле культура «Methanobacillus omelianskii» содержит два организма: один («форма S»), споровый, близкий к Clostridium kluyveri, разлагающий этанол с образованием ацетата и выделением Н2, и второй (штамм «М.о.Н.»), превращающий Н2 в инертный метан. Реакция выделения Н2 из этанола термодинамически невыгодна и становится возможной лишь при глубоком удалении Н2 из сферы реакции. В результате суммарная реакция термодинамически возможна и способна обеспечить оба организма необходимой энергией. Реакция была названа межвидовым переносом водорода.
Организмы, способные к развитию при условии, что Н2 удаляется из сферы реакции, получили название синтрофов и составили особую функциональную группу в сообществе. Из несбраживаемых соединений они образуют ацетат и водород. Синтрофы развиваются совместно с Н2-использующими анаэробными организмами. Среди Н2-использующих бактерий важны две группы: литотрофные метаногены и литотрофные сульфидогены.
Развитие синтрофов обусловлено выигрышем свободной энергии за счет уменьшения концентрации продукта. Для реакции даже при недостаточном или же положительном значении свободной энергии в стандартных условиях возможен выигрыш, если концентрация продуктов мала.
Поскольку окислительно-восстановительная реакция может быть представлена как реакция дегидрогенизации, то ключевой оказывается реакция удаления Н2. Снижение концентрации Н2 может осуществляться например: продувкой газом, реакцией с окислителем (например, с серой), но наиболее важным способом удаления служит использование Н2 гидрогенотрофами. В этом случае процесс принципиально может осуществляться только в присутствии двух организмов: одного, обладающего «выделяющей гидрогеназой», и другого, с «поглощающей гидрогеназой», хотя функции фермента зависят от сопряжения с системой реакций внутри организма.
Для термодинамического разрешения роста за счет удаления Н2 из сферы реакции важен тот нижний предел концентрации, до которого тот или иной организм способен удалять Н2. Повышение концентрации Н2 является первым сигналом разбалансированности в работе сообщества вследствие какого-либо стресса.
Как известно, выделение и потребление Н2 осуществляется гидрогеназами, катализирующими обратимую реакцию:
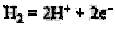
Следовательно, можно предположить, что устанавливаются некоторые равновесные концентрации Н2. Впервые такая равновесная концентрация была установлена Т. Н. Жилиной при разложении метанола Methanosarcina. При выделении чистой культуры метаногена упорным спутником ее оказался Desulfovibrio vulgaris, не использующий метанол, как и другие сульфатредук-торы, но растущий с Н2. Выяснилось, что метилотрофные метаногены при росте на метиламинах поддерживают стационарную концентрацию Н2 за счет его выделения. Таким образом, в бинарной культуре Methanosarcina + Desulfovibrio метаноген выполнял роль синтрофа по отношению к сульфидогену, имеющему большее сродство к Н2.
Термодинамический выигрыш при удалении продукта реакции может быть получен не только для Н2, но и для других соединений.
Катаболическая синтрофия с межвидовым переносом водорода представляет один из ключевых процессов в анаэробном сообществе. Таким образом, водородный путь с участием гидрогенотрофных вторичных анаэробов в сочетании с явлением синтрофии оказывается принципиальным для сообщества в целом.
3.7 Взаимодействие гидролитиков и диссопотрофов
Рассеиваемый при гидролизе полимера олигомерный продукт может быть использован «микрофлорой рассеяния», теперь получившей название диссипотрофов. Эти организмы легче всего выделяются в культуру и лучше всего известны в лабораторной практике. Диссипотрофы представлены в основном одиночными клетками, часто подвижными. В анаэробном сообществе они нагляднее всего представлены спирохетами с очень выгодным отношением поверхности к объему. Зависимость диссипотрофов от гидролитиков очевидна. Необходимость взаимодействия двух групп организмов при разложении даже такого простого вещества, как линейный полимер глюкозы — целлюлоза — лучше рассмотреть на конкретном примере анаэробных термофильных целлюлозолитических организмов.
Разложение целлюлозы представляет важнейший маршрут в наземных и многих морских экосистемах, поскольку целлюлоза образуется в больших количествах как структурный компонент клеточной оболочки растениями и водорослями. Способностью к разложению целлюлозы обладают многие грибы, из которых наиболее подробно была изучена Trichoderma, некоторые актиномицеты, часть которых специализирована на разложении хитина, в том числе грибной стенки, аэробные бактерии, как, например, цитофаги, некоторые миксобактерии, бациллы, целлуломонас, целлвибрио. Среди анаэробов наиболее легкими для исследования объектами оказались клостридии.
Использование целлюлозы обусловлено взаимодействием с нерастворимым гидрофильным субстратом, представляющим структурно-организованные волокна. Отсюда следуют необходимость физического контакта клеток с нерастворимым субстратом и обрастание его биопленкой. Деградация целлюлозы требует действия внеклеточных ферментов целлюлаз. Доступность для фермента сильно коррелирует с пористостью целлюлозного материала. Физический предел пор для действия фермента составляет величина в 40-50 ангстрем.
Разложение целлюлозы было подробно исследовано на примере Clostridium thermocellum в связи с организацией производства этанола на целлюлозе. Гидролиз осуществляется внеклеточным целлюлазным комплексом (целлюлосомой), включающим ряд ферментов, прежде всего эндоглюконазу, гидролизующую р-1,4 связь в разных местах с образованием случайных по длине целлодекстринов, которые могут быть далее гидролизованы до более коротких олигомеров и поступать в клетку. У С. thermocellum эндоглюконазный комплекс наиболее активен. Менее активна у этого организма экзоглюконаза, отщепляющая с редуцирующего конца полимерной цепочки дисахарид целлобиозу.
Соотношение эндоглюконаза/экзоглюконаза различно у разных организмов. Например, у гриба Trichoderma преобладает экзоглюконаза. Целлюлазный комплекс по-разному ингибируется конечными продуктами у разных целлюлозолитиков.
Продукты гидролиза целлюлозы переносятся в клетку двумя разными путями с участием необычных ферментов: фосфорилазыцеллобиозы или целлодекстрин-фосфорилазы. Обе эти реакции фосфорилирования термодинамически обусловлены гидролитическим выбросом глюкозы вне клетки при АТФ-независимом транспорте остающейся части полиглюкозы внутрь клетки. Там она подвергается сбраживанию, по обычному пути брожения, с образованием летучих жирных кислот и, прежде всего, бутирата, ацетата, этанола, Н2.
Сходные пути гидролиза действуют и с другими полисахаридами, требуя специфических ферментных систем. Легче всего гидролизуются растворимые полисахариды, для которых есть соответствующие ферменты: крахмал с амилазой, пуллулан с пуллуланазой, ксилан с ксиланазой и т. д.
Из описания действия целлюлазного комплекса с очевидностью следует, что целлюлозолитические организмы должны развиваться в тесных симбиотических отношениях с другими организмами. Прежде всего это относится к необходимости удаления глюкозы диссипотрофами. В исследованной бинарной культуре с С. thermocellum глюкозу использовал Thermoanaerobacter. Аэробным целлюлозолитикам цитофагам сопутствуют типичные диссипотрофы простекобактерии. Таким образом, образование пары «гидролитик — диссипотроф» представляет правило. Для анаэробных целлюлозолитиков необходимо удаление продуктов брожения, так же как для многих первичных анаэробов. Поэтому целлюлозолитические организмы развиваются в тесных синтрофных отношениях с рядом сопутствующих форм.
Помимо катаболических взаимодействий, спутники обеспечивают анаболические нужды целлюлозолитиков. А. А. Например, сопутствующие диссопотрофы обеспечивают анаболические целлюлозолитиков связанным азотом, а также различными факторами роста. В результате целлюлозолитическое сообщество взаимодополняющих организмов представляет функционально нечто совершенно иное, чем чистая культура, где необходимо специальными приемами восполнять недостающие потребности организма. Поэтому в каждых экологических условиях формируется своя группировка, связанная с разложением целлюлозы, включающая функционально сходные, но различные но происхождению организмы.
Молекулярные методы позволили разобраться в происхождении целлюлозолитической активности на примере узкой группы экстремально термофильных целлюлозолитиков. Гены, определяющие целлюлозолитическую активность, часто полифункциональны, несколько различаются по последовательностям, но вместе с тем существует высокая вероятность того, что горизонтальный перенос генов имел большое значение в эволюции этой функциональной группы организмов.
3.8 Метаногенное сообщество
В трофическую систему входят немногие функциональные группы организмов. Разложение мортмассы начинают гидролитики, специализированные по определенным полимерам, например, целлюлозолитические, пектинолитические, пептолитические и т. д., образующие разнообразные маршруты, сходящихся к немногим промежуточным олигомерам. В сочетании с ними действуют лишенные гидролитической активности диссипотрофы, использующие растворенные олигомеры. Если гидролитики ограничены поверхностью гидролизуемых веществ твердой фазы, то для диссипотрофов ограничение обусловлено притоком рассеиваемых веществ. Анаэробные гидролитики и диссипотрофы составляют группировку первичных анаэробов-бродилыциков, осуществляющих водородную или кислотогенную фазу с образованием несбраживаемых продуктов.
Образуемые гидролитиками и диссипотрофами Н2 и ацетат могут использоваться соответственно гидрогенотрофными и ацетокластическими метаногенами. Другие продукты брожения и гидролиза, суммарно обозначенные как летучие жирные кислоты, разлагаются при межвидовом переносе водорода с участием ацетогенных синтрофных бактерий (при условии эффективного удаления Н2 гидрогенотрофными метаногенами).
Если же Н2 не используется гидрогенотрофными метаногенами в силу каких-либо причин, например низкой температуры, то начинает действовать гомоацетатный шунт (анг. ответвление), в котором гидрогенотрофные гомоацетатные бактерии образуют ацетат по реакции:
ЗН2 + 2СО2 = СН3СООН + Н2О
В рассмотренном сообществе необходимо взаимодействие всех групп, причем гидрогенотрофные метаногены играют роль конечного стока для Н2, обеспечивающего возможность разложения ЛЖК синтрофами. В противном случае Н2 ингибирует разложение ЛЖК. Сходную роль выполняют и диссипотрофы по отношению к гидролитикам. Таким образом, здесь имеются и термодинамически обусловленные обратные связи, и регуляторные связи. Если в сообществе имеется дисбаланс между группами организмов, например, вследствие избытка легкодоступных углеводов, то происходит ингибирование микроорганизмов образующимися органическими кислотами вследствие снижения рН.
Один из вариантов связей для рассмотренного участка трофической цепи наблюдается в психроактивном сообществе тундры. За короткий вегетационный период глубокий гидролиз растительных оболочек не успевает осуществиться, и поэтому возникает короткая пищевая цепь, свойственная копиотрофам, в которой используются легко гидролизуемые и растворимые вещества, преимущественно по пути маслянокислого брожения с обильным выделением Н2. Водород используется гидрогенотрофными гомоацетатными бактериями с образованием ацетата. Водородные метаногены отсутствуют. Разложение ацетата протекает медленно за счет накопленной биомассы ацетокластических метаногенов с очень медленным ростом.
3.9 Сульфидогенное сообщество
Сообщество развивается в условиях поступления сульфата. Тогда место метаногенов занимают сульфидогены. Они осуществляют сток Н2, обеспечивая работу синтрофов и благоприятный термодинамический баланс сообщества. Они же способны использовать лактат, образуемый из углеводов молочнокислыми бактериями и в результате удерживают рН системы, не давая закислиться среде. Группа ацетотрофных сульфидогенов использует ацетат, однако с некоторым запозданием относительно гидрогенотрофных организмов. ЛЖК разлагаются либо консорциумом синтрофов и гидрогенотрофов, либо напрямую — ацетат и ЛЖК-использующими сульфидогенами, из которых особое внимание следует обратить на род Desulfotomaculum. Сульфидогенная трофическая система накладывается на метаногенную и доминирует над ней.
Ценой участия сульфидогенов служит образование H2S, который оказывает подавляющее действие на большинство сообществ, за исключением тиофильных. Для метаногенного сообщества обычна концентрация 2-3 мМ H2S и превышение ее требует смены сообщества с появлением других видов в тех же функциональных группах микроорганизмов.
Сульфидогенное сообщество играет чрезвычайно большую роль в морских условиях, причем большая часть органического вещества в донных осадках разлагается по этому пути. Ограничивающим фактором служит приток сульфата извне. Регенерация сульфата возможна двояким путем: либо H2S окисляется в аэробных условиях, либо анаэробно окисляется в сульфат аноксигенными фототрофными бактериями.
Характерным во взаимодействии сульфидогенного и метаногенного сообществ служит существование так называемого «неконкурентного С пути». Например, при разложении пектина образуется метанол, не используемый сульфатредукторами, но окисляемый метилотрофными метаногенами. Даже при избытке сульфата и подавлении других метаногенов, например, в гиперсоленых водоемах, метилотрофные метаногены продолжают действовать в «неконкурентном пути» метаногенеза и служить источником метана.
3.10 Бактериальный окислительный фильтр и изотрофы
Если продукты анаэробного обмена поступают в область, где присутствует О2, то они становятся доступны для окисления аэробами. Эта группировка микроорганизмов получила название «бактериального окислительного фильтра» или, в связи с тем что важная часть продуктов анаэробного обмена представлена восстановленными газами, «газотрофов». Аэробное окисление продуктов обмена вторичных анаэробов представляет альтернативу их фототрофному окислению. Сообщество газотрофов не образует столь четких связей между собой, как анаэробы-органотрофы, поскольку, по сути, использует аллохтонное вещество, поступающее в его область развития извне. Общим субстратом, за который идет конкуренция, является О2. Соответственно газотрофы составляют ряд градаций от аэробов до микроаэрофилов и факультативных анаэробов. Этот ряд находит свое выражение в расположении газотрофов в виде пленок или тонких зон в области оксиклина, или кислородного скачка — обусловленного ими резкого снижения концентрации O2. Поэтому они относятся к так называемым градиентным организмам, развивающимся в переходной зоне от восстановленных к окислительным условиям. Наиболее характерными представителями этой группы служат бесцветные серобактерии, слои которых часто окрашены в ярко белый цвет отложениями серы. Градиентные организмы очень трудно поддаются культивированию в лабораторных условиях.
Газотрофы выполняют роль защитного фильтра от кислорода для анаэробного сообщества, препятствуя проникновению O2 в нижележащие слои.
Среди организмов окислительного фильтра характерны хемо-литотрофы и метанотрофы. Окисляемыми соединениями являются СН4 для метанотрофов, Н2 для водородных бактерий, СО — для карбоксидобактерий, NH3 — для нитрификаторов, H2S — для серобактерий, устойчивые к окислению соединения серы, как тиосульфат — для тионовых бактерий. Большинство газотрофов — высокоспециализированные организмы, но часть из них, как водородные бактерии, относится к факультативно автотрофным организмам. Газотрофы представляют критически важную группу для состава атмосферы, предотвращая выход в нее таких газов, как метан.
3.11 Аэробное сообщество
Центральное место в аэробном сообществе занимают первичные продуценты — оксигенные фотоавтотрофы. Они в дневное время служат источником О2 и экскретируемых органических веществ, которые могут быть использованы сопутствующими органотрофами. В ночное время фотоавтотрофы используют запасные вещества для дыхания. В тех бентосных сообществах цианобактерий или водорослей, которые оказываются ночью в аноксической зоне, темновой метаболизм может быть обеспечен брожением запасных углеводов в виде полиглюкозы, а у цианобактерий и брожением аргинина. Главным продуктом первичных продуцентов служит мортмасса фотоавтотрофов, включающая в себя две категории веществ: легко разлагаемые запасные вещества и компоненты цитоплазмы, преимущественно растворимые (РОВ) и нерастворимые структурные компоненты, прежде всего клеточной стенки (ВОВ), поступающие в виде опада.
Аэробные органотрофы очень разнообразны и представляют группу, привлекшую более всего внимания на уровне чистых культур. Для системы трофических связей характерна структура сходящихся пищевых маршрутов в виде перевернутого «веера», где каждое вещество имеет своего специалиста. «Веер» сходится к СО2 как конечному продукту и суммарное действие аэробов определяется по дыханию: образованному СО2 и/или потребленному О2. В трофической системе, помимо специализации по субстратам, можно различить группы зимогенов-копиотрофов, гидролитиков, диссипотрофов, автохтонов.
Использование веществ, экскретируемых оксигенными фототрофами, ведет органотрофов к временной экспозиции в условиях гипероксии, и поэтому аэробы этой группы должны иметь эффективную защиту от токсического действия О2, усиливающегося действием света. Характерным признаком служит образование антиоксидантов каротиноидов, свойственных, например, бактериям, развивающимся в сообществе с литофильными лишайниками, особенно в высокогорье.
Растворенные вещества служат субстратом зимогенной микрофлоры, представленной копиотрофами. Белковые соединения разлагаются протеолитическим путем гниения, с участием аммонифицирующих организмов; аммиак поступает нитрификаторам. В природе этапы деградации можно наблюдать при самоочищении водотоков, в которых выделяются зоны сапробности от сильно загрязненных к очищенным водам. Моделью интенсивного разложения легкодоступного органического вещества служат аэрируемые очистные сооружения. Критическим фактором служит доступность кислорода: при высоком содержании органических веществ поступление его путем диффузии становится недостаточным и преимущество получают факультативно анаэробные организмы. Практическим приемом определения дыхания за счет растворенных веществ служит определение «биохимического потребления кислорода». Обычно определяется потребление О2 за 5 суток в исследуемой природной воде или после ее разбавления аэрированной водой. ВПК служит очень надежной мерой определения доступного органического вещества.
Особую роль среди экскретируемых растениями веществ представляют летучие органические соединения, например терпены, выделяемые растениями и токсичные для бактерий.
Нерастворимые вещества подвергаются гидролизу специализированными группами организмов. В водоемах взвешенное органическое вещество в значительной степени оседает на дно и, вследствие медленной диффузии 02, поступает в анаэробную зону. В наземных экосистемах ведущую роль играет гидролиз лигноцеллюлозы растительных остатков. Наземные гидролитические организмы часто имеют мицелиальное строение и представлены эукариотными микромицетами и актиномицетами. Последние доминируют при разложении мортмассы грибного мицелия, представленного полимером глюкозамина хитином. Из бактерий характерными целлюлозолитическими организмами являются цитофаги, некоторые миксобактерии. Особый путь представляет разложение лигнина, осуществляемое только грибами с помощью перекисного механизма, принципиально зависящего от доступности кислорода. Образующиеся при этом фенольные соединения используются бактериями. Сообщество грибов как важнейших деструкторов одревесневшей растительной массы работает на главных трофических маршрутах в лесных экосистемах.
Гидролитические организмы образуют сложные сообщества с диссипотрофами, в которых важны не только связи по основному субстрату, но и взаимозависимость по анаболизму, обмен факторами роста. Группировка аэробных диссипотрофов, характерным представителем которых служат простекобактерии, очень важна в сообществе, начиная доминировать на поздних стадиях микробной сукцессии деструкторов.
В системе аэробных деструкторов характерным продуктом оказываются остаточные вещества, например, лигнин и трудно разложимые соединения, которые дают начало гумусовым веществам. В цикле углерода эти устойчивые соединения играют первостепенную роль при переходе ко времени геологических масштабов и эволюции биосферы в целом. Они разлагаются «автохтонной» микрофлорой. Разложение идет преимущественно по пути соокисления, когда образующиеся при дыхании перекиси хаотически разрушают углеродный скелет устойчивого соединения, а продукты, часто циклические, используются автохтонной микрофлорой.
Таким образом, представленная схема взаимоотношений трофических групп, в микробном сообществе должна с той или иной степенью полноты реализовываться в сообществах, населяющие разные биотопы. Соответственно перечисленные группы организмов должны содержать виды, приспособленные к развитию при высокой температуре в термофильном сообществе, при низкой — в психрофильном. В пресных водоемах, в море развиваются свои сообщества; при повышенной солености в лагунах — галофильное сообщество; в почве, в горных породах — свои. Особенно велико разнообразие продуцентов — цианобактерий, водорослей, растений — и органотрофов, аэробных и анаэробных, лежащих на маршрутах разложения органического углерода в сообществе. В сообществе с обилием органического вещества, например в сточных водах, число культивируемых видов составляет многие сотни. Доминируют, однако, немногие десятки.
3.12 Сообщество и филогения
Сообщество микроорганизмов действует как метаболическая целостность, объединяя организмы с разными трофическими функциями. Эти функции имеют первостепенное значение в отношениях организма со средой и соответственно могут рассматриваться как благоприобретенные.
Рассматривая совокупность обитателей одной экологической ниши, можно сделать заключение, что они часто близки между собой и большое число их представлено организмами, филогенетически родственными, например, органотрофные анаэробные копиотрофы в значительной степени представлены клостридиями и родственными им организмами. Другими примерами могут служить сульфатредукторы, составляющие филогенетически обособленные группы, хотя способность к сульфатредукции, распространена и среди других филогенетических линий.
Если же рассматривать трофические связи между функциональными группами в сообществе, то оказывается, что тесно взаимосвязанные, а иногда и прямо взаимозависящие группировки, как правило, представлены филогенетически удаленными друг от друга организмами (Г. А. Заварзин). Например, в анаэробном сообществе гидролитики представлены клостридиями, а взаимодействующие с ними диссипотрофы — спирохетами; взаимодействующие с грамположитель<
Дата добавления: 2020-10-01; просмотров: 719;











