Ферментативные методы анализа пищевых продуктов
Ферментативный анализ представляет собой один из основных аналитических инструментов в международной и отечественной практике научных исследований, современного производственного и сертификационного контроля качества продуктов питания, пищевого сырья и биологических материалов.
Ферментативный анализ является составной частью энзимологии и аналитической химии и служит для специфического определения веществ с помощью высокоочищенных препаратов ферментов.
В основе ферментативного анализа лежат природные биохимические процессы обмена веществ, которые воспроизводятся in vitro: реакция фермента с субстратом, причем в качестве субстрата выступает анализируемое вещество пробы.
Основными преимуществами применения ферментативных методов в научных исследованиях при разработке новых пищевых технологий и биотехнологических процессов, а также при анализе качества, идентификации и установления фальсификации продуктов питания и пищевого сырья являются:
§ высокая специфичность и достоверность результатов. Высокоспецифичные ферментативные методы анализа дают, как правило, более достоверные результаты, чем неспецифические химические методы. Специфичность действия ферментов, основанная на комплементарности пространственной конфигурации активного центра и субстрата, является гарантом достоверности и надежности ферментативного метода при исследовании отдельных соединений в многокомпонентных смесях, имеющих сложный состав и строение, таких, какими и являются пищевые продукты.
При разработке ферментативных методов и подборе реагентов, в первую очередь, выбирают ферменты с наибольшей специфичностью действия, для которых подбираются оптимальные условия проведения анализа. Кроме того, при разработке методов ферментативного анализа отдельных компонентов продуктов питания обычно используют несколько ферментов, которые последовательно функционируют в данной системе.
§ простые способы подготовки проб, которые исключают потерю исследуемых компонентов. Основная задача, которую необходимо выполнить при подготовке пробы — по возможности наиболее полно сохранить для анализа исследуемый компонент без его количественной потери или изменения структуры. В некоторых случаях возможен прямой анализ пробы без ее предварительной подготовки (например, при абсолютной специфичности фермента к исследуемому веществу и отсутствии в пробе каких-либо мешающих факторов). Обычно же для ферментативного анализа используются простые и хорошо известные способы подготовки проб, такие как разбавление, фильтрация (центрифугирование), нейтрализация (подкисление), экстракция, обезжиривание, осветление, обесцвечивание. Только в определенных случаях применяют специальные способы подготовки проб, например, при определении водонерастворимых соединений (холестерин, лецитин, крахмал), нестабильной L-аскорбиновой кислоты в твердых материалах и др.
§ простая и быстрая процедура изменений, которая исключает использование долгосрочного оборудования. В большинстве ферментативных определений используют фотометрические способы измерения результатов. Для этого все компоненты искусственной тестовой системы, например, буфер, коферменты, активаторы, вспомогательные ферменты и пробу смешивают в фотометрической кювете. После измерения начальной оптической плотности добавляют стартовый фермент, который инициирует реакцию. В конце реакции (через определенный промежуток времени) повторно измеряют оптическую плотность тестовой системы. Из разницы оптических плотностей в начале и в конце реакции по уравнению закона Ламберта–Бера рассчитывают концентрацию С (г/л) искомого соединения:
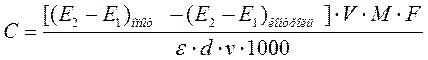 ,
,
где (Е2 – Е1)опыт — разница конечной и начальной оптической плотности в кювете с пробой;
(Е2 – Е1)контроль — разница конечной и начальной оптической плотности в кювете без пробы;
V — общий объем реакционной смеси, мл;
M — молярная масса искомого соединения, г/моль;
F — фактор разведения пробы;
ε — молярный коэффициент оптической активности соединения реакционной смеси, например, кофермента НАДФ+, НАД+ при λ = 340 нм, ε = 6,3 л/ммоль · см);
d — толщина кюветы, см;
v — объем пробы, добавляемый в кювету, мл.
В большинстве ферментативных методов прямому фотометрическому контролю доступно измерение таких вспомогательных компонентов тестовой системы, как коферментов НАД+/НАД·Н или НАДФ+/НАДФ·Н. Количество восстановленных или окисленных коферментов прямо пропорционально количеству искомого соединения. Система конечных значений с фотометрическим измерением результата настолько надежна, что служит в качестве стандарта для оценки других методик.
Для проведения ферментативного анализа используется стандартное оборудование, которое имеется практически в любой производственной лаборатории: спектрофотометры или фотометры с интервалом измерений от 325 до 800 нм, кюветы для фотометрических измерений, мерные пипетки и дозаторы, весы, центрифуга, рН-метр, водяной термостат, фильтры и т.п.
§ высокая чувствительность метода и хорошая воспроизводимость результатов. Высокая чувствительность позволяет использовать ферментативные методы для определения следовых количеств веществ. Например, в продуктах питания могут быть определены следующие концентрации компонентов: этанол — 0,001 г/л; ацетоальдегид — 0,001 г/л; лимонная кислота — 0,002 г/л; глицерин — 0,001 г/л; D-глюкоза — 0,002 г/л; D-сорбит — 0,001 г/л; лактоза — 0,005 г/л; нитраты — 0,001 г/л.
Кроме выше перечисленных достоинств ферментативных методов анализа можно назвать и универсальность применения, высокую надежность и устойчивость к мешающим факторам, низкие затраты на проведение анализа (время, оборудование, расходуемые материалы), а также использование безопасных реактивов.
Области применения ферментативного анализа на практике многообразны. Это и производственный контроль, и контроль качества готовой продукции, а также контроль сырья, анализ состава пищевого продукта с целью установления их свойств и соответствия законодательным нормам, оценка гигиенического статуса, идентификация и установление фальсификации.
В таблице 4 приведены некоторые группы продуктов питания, а также их компоненты, для анализа которых разработаны специфические ферментативные методы.
Таблица 4. Применение ферментативных методов для анализа различных компонентов пищевых продуктов
| Группа продуктов | Анализируемые компоненты |
| Детское питание, диетические продукты Пиво, вино, игристые вина Хлеб, хлебобулочные изделия, шоколад, мороженное и кондитерские изделия | Сахароза, D-глюкоза, D-фруктоза, лактоза, мальтоза, крахмал, L-аскорби-новая кислота, лимонная кислота, D-, L-молочные кислоты, D-сорбит, ксилит, лецитин, холин D-глюкоза, D-фруктоза, сахароза, глюкозный сироп, этанол, глицерин, D-сор-бит, сульфит, нитраты, L-, D-молочные кислоты, D-глюконовая кислота, уксусная кислота, лимонная кислота, янтарная кислота, L-аскорбиновая кислота Сахароза, D-глюкоза, D-фруктоза, лактоза, мальтоза, крахмал, этанол, глицерин, D-сорбит, ксилит, холестерин, лецитин |
Окончание таблицы 4
| Яйца и яичные продукты Соки, фруктовые продукты, безалкогольные напитки Мясо и мясные продукты Молоко и молочные продукты Пищеконцентраты (например, супы) Сахар и сахаристые изделия | Янтарная кислота, L- молочная кислота, D-3-гидроксимасляная кислота, холестерин Сахароза, D-глюкоза, D-фруктоза, лимонная кислота, D-изолимонная кислота, L-аскорбиновая кислота, D-, L-мо-лочные кислоты, этанол, уксусная кислота, глюкозный сироп, щавелевая кислота, глицерин, D-, L-яблочные кислоты, муравьиная кислота, D-глюконовая кислота, D-сорбит, нитраты Сахароза, лактоза, D-глюкоза, D-галак-тоза, крахмал, лимонная кислота, уксусная кислота, D-глюконовая кислота, L-глутаминовая кислота, D-, L-молоч-ные кислоты, муравьиная кислота, глицерин, аммиак (мочевина), креатин/креатинин, пирофосфаты, холестерин Лактоза, D-глюкоза, D-фруктоза, D-га-лактоза, крахмал, сахароза, лимонная кислота, уксусная кислота, L-яблочная кислота, янтарная кислота, L-глутами-новая кислота, D-, L-молочные кислоты, этанол, ацетоальдегид, триглицериды, мочевина, нитраты Креатинин, L-глутаминовая кислота, сахароза, крахмал Сахароза, D-глюкоза, D-фруктоза, рафиноза, муравьиная кислота, лимонная кислота, D-, L-молочные кислоты, этанол, D-сорбит |
Источник: Колеснов А. Ю. Ферментативный анализ в пищевой промышленности //
Пищевая промышленность, 1996, № 11.
По словам одного из основоположников ферментативного анализа Г. Бергмана: «Ферментативный анализ, как принцип, свободен от недостатков и ошибок, так как он представляет систему для измерений, которую успешно использует живая клетка уже в течение миллионов лет».
Контрольные вопросы
- Что такое ферменты, какова их химическая природа?
- В чем заключаются особенности ферментов, как биологических катализаторов?
- Какие факторы влияют на активность ферментов?
- Как определяют начальную скорость ферментативной реакции? Почему начальная скорость является мерой количества фермента?
- На чем основана классификация ферментов?
- Дайте краткую характеристику каждому классу ферментов.
- Что такое ферментные препараты и чем они отличаются от ферментов?
- Какова роль ферментов — оксидоредуктаз при хранении и производстве пищевых продуктов?
- Какова роль гидролитических ферментов при хранении и производстве пищевых продуктов?
- Какие ферменты наиболее широко применяются в пищевой промышленности? Приведите примеры.
Список рекомендуемой литературы
1. Бекер М. Е. Введение в биотехнологию. – М.: Пишевая промышленность, 1978. – 229 с.
2. Берхард С. Структура и функции ферментов. – М.: Мир, 1971. – 334 с.
3. Витол И. С., Кобелева И. Б., Траубенберг С. Е. Ферменты и их применение в пищевой промышленности. – М.: ИК МГУПП, 2000. – 80 с.
4. Грачева И. М., Кривова А. Ю. Технология ферментных препаратов. – М.: Элевар, 2000. – 521 с.
5. Диксон М., Уэбб Э. Ферменты: в 3 т., 3-е изд. – М.: Мир, 1982. – 1120 с.
6. Жеребцов Н. А., Корнеева О. С., Фараджаева Е. Д. Ферменты: их роль в технологии пищевых продуктов. – Воронеж: Изд-во ВГУ, 1999. – 120 с.
7. Иванова Л. А., Войно Л. И., Иванова И. С. Пищевая биотехнология. Кн. 2: Переработка растительного сырья. – М.: КолосС, 2008. – 472 с.
8. Кислухина О. В. Ферменты в производстве пищи и кормов. – М.: ДеЛи принт, 2002. – 336 с.
9. Колеснов А. Ю. Биохимические системы в оценке качества продуктов питания. – М.: Пищевая пром-сть, 2000. – 414 с.
10. Кретович В. Л. Введение в энзимологию. – М.: Наука, 1986. – 332 с.
11. Микробные ферменты в биотехнологии / Под ред. М. В. Фогарти. – М.: Агропромиздат, 1986. – 318 с.
12. Нечаев А. П., Траубенберг С. Е., Кочеткова А. А., Колпакова В. В., Витол И. С., Кобелева И. Б. Пищевая химия. – СПб.: ГИОРД, 2012. – 672 с.
13. Номенклатура ферментов. Рекомендации Международного биохимического союза. – М., 1979. – 319 с.
14. Рид Д. Ферменты в пищевой промышленности. – М.: Пищевая пром-сть, 1971. – 414 с.
15. Рогов И. А., Антипова Л. В., Дунченко Н. И. Химия пищи. – М.: КолосС, 2007. – 853 с.
16. Техническая биохимия / Под ред. В. Л. Кретовича. – М.: Высшая школа, 1973. – 456 с.
17. Тривен М. Иммобилизованные ферменты. – М.: Мир, 1983. – 213 с.
18. Уэстли Дж. Ферментативный катализ. – М.: Мир, 1972. – 270 с.
19. Ферментные препараты в пищевой промышленности / Под ред. В. Л. Кретовича. – М.: Пищевая пром-сть, 1975. – 515 с.
[1] Дыхательный коэффициент — отношение выделившейся при дыхании СО2 к количеству поглощенного О2.
Дата добавления: 2020-10-01; просмотров: 622;











