Ингибиторы ферментов
Действие ферментов можно полностью или частично подавить (ингибировать) определенными химическими веществами (ингибиторами). По характеру действия ингибиторы могут быть обратимыми и необратимыми. В основе этого деления лежит прочность соединения ингибитора с ферментом. Другой способ деления ингибиторов основывается на характере места их связывания. Одни из них связываются с ферментом в активном центре, а другие - в удаленном от активного центра месте. Они могут связывать и блокировать функциональную группу молекулы фермента, необходимую для проявления его активности. При этом они необратимо, часто ковалентно, связываются с ферментом или фермент - субстратным комплексом и необратимо изменяют нативную конформацию. Это, в частности, объясняет действие Hg2+, Pb2+, соединений мышьяка. Ингибиторы такого рода могут быть полезны при изучении природы ферментативного катализа. Например, диизопропилфторфосфат ингибирует ферменты, имеющие серин в активном центре. Таким ферментом может быть ацетилхолинэстераза.
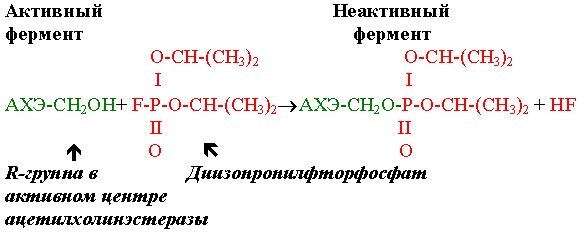
Ацетилхолинэстераза, катализирующая следующую реакцию:
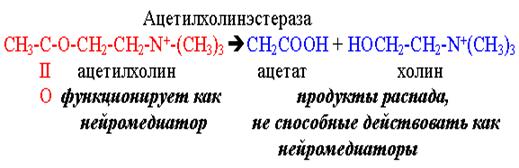
|
Реакция происходит каждый раз после проведения нервного импульса, прежде чем второй импульс будет передан через синапс.
Диизопропилфторфосфат - одно из отравляющих веществ нервно-паралитического действия, так как приводит к утрате способности нейронов проводить нервные импульсы.
Терапевтическое действие аспирина как жаропонижающего и противовоспалительного средства объясняется тем, что аспирин ингибирует один из ферментов, катализирующий синтез простагландинов (ПГ). Простагландины - вещества, участвующие в развитии воспаления. Ингибирование обусловлено ковалентной модификацией одной из аминогрупп фермента - простагландинсинтетазы.
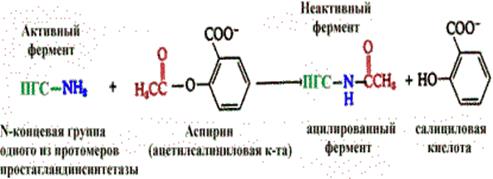 Взаимодействие аспирина с ферментом простагландинсинтетазой
Взаимодействие аспирина с ферментом простагландинсинтетазой
|
Обратимые ингибиторы. Существует два типа подобных ингибиторов - конкурентные и неконкурентные. Конкурентный ингибитор конкурирует с субстратом за связывание с активным центром. Это происходит потому, что ингибитор и субстрат имеют сходные структуры (рис. 2.3).
В отличие от субстрата связанный с ферментом конкурентный ингибитор не подвергается ферментативному превращению. Более того, образование EI уменьшает число молекул свободного фермента, и скорость реакции снижается. Связывание S и I происходит взаимоисключающим образом. Образуется либо ES, либо EI, но не EIS. Так как конкурентный ингибитор обратимо связывается с ферментом, то можно сдвинуть равновесие реакции E + I ↔ EI влево простым увеличением концентрации субстрата. Конкурентными ингибиторами являются многие химиотерапевтические средства.

|
Рис. 2.3. Конкурентное ингибирование.
S-субстрат, I- ингибитор (своей трехмерной структурой похож на субстрат).
Например, сульфамидные препараты, используемые для лечения инфекционных болезней. Сульфаниламиды – это структурные аналоги парааминобензойной кислоты, из которой в клетке микроорганизма синтезируется кофермент (Н4 - фолат), участвующий в биосинтезе нуклеиновых оснований. Нарушение синтеза нуклеиновых кислот приводит к гибели микроорганизмов.
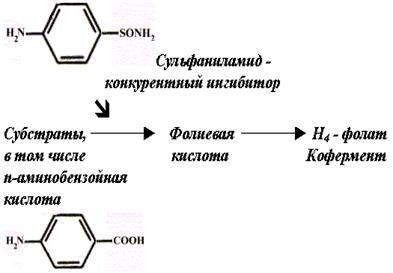
|
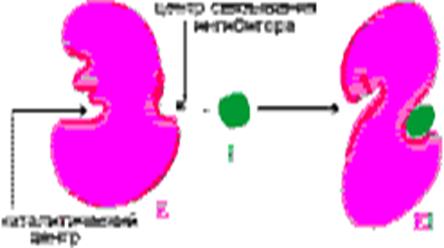
Неконкурентное обратимое ингибирование не может быть ослаблено или устранено повышением концентрации субстрата, так как эти ингибиторы присоединяются к ферменту не в активном центре, а в другом месте (рис. 2.4). Связывание приводит к изменению конформации фермента и нарушению комплементарности к субстрату. Неконкурентные ингибиторы могут обратимо связываться как со свободным ферментом, так и с комплексом ES. Наиболее важными неконкурентными ингибиторами являются образующиеся в живой клетке промежуточные продукты метаболизма, способные обратимо связываться с определенными участками ферментов (аллостерические центры) и изменять их активность, что является одним из способов регуляции метаболизма.
|
Рис. 2.4. Неконкурентное обратимое ингибирование: E + S ↔ ES → E + P; E + I ↔ EI; ES + I → ESI.
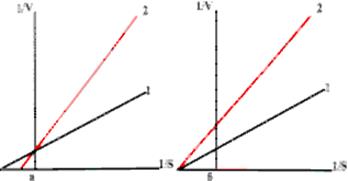
Исследование действия ингибиторов используется при изучении механизма действия фермента, кроме того, помогает в поисках более эффективных лекарственных средств, так как лечебное действие многих лекарств обусловлено тем, что они являются ингибиторами определенных ферментов. Структурные аналоги коферментов тоже могут быть ингибиторами. Кинетические тесты позволяют отличить конкурентное ингибирование от неконкурентного (рис. 2.5) .
|
Рис. 2.5. Зависимость I/V от I/S. 1 - без ингибитора, 2 - в присутствии ингибитора
(а - конкурентное; б - неконкурентное ингибирование)
Дата добавления: 2019-02-08; просмотров: 1311;











