Структурно-чувствительные и структурно-нечувствительные реакции. Дисперсность металлов.
Помимо взаимного расположения атомов катализатора на кристаллографических плоскостях, большое влияние также оказывает место расположения атомов на дефектах поверхности катализатора.
Так, например, при гидрогенолизе циклогексана до н-гексана на платине, атомы на изломах имеют активность на порядок выше, чем атомы на ступенях, а наименее активны - атомы на террасах. Таким образом по активности поверхностные атомы платины можно разделить на три группы:
- Высоко координационно-насыщенные атомы на террасах: низкая активность;
- Атомы на ступенях: более активны, катализируют разрыв С-Н и Н-Н связей;
- Сильно координационно-ненасыщенные атомы на изломах: высоко активны, катализируют разрыв С-С связей.
По причине высокой активности атомы ступеней и изломов не закоксовываются во время реакции. Предполагается, что образующийся на них слой карбонизированного продукта немедленно удаляется по реакции гидрирования.
Методом ИК-спектроскопии была изучена хемосорбционная активность платины по отношению к СО. Были выявлены следующие комплексы СО на поверхности Pt:
n (СО) на ступенях: 2066 см-1, низкая степень покрытия поверхности, разрыхленная связь СО;
n (СО) на террасах: 2090 см-1, высокая степень покрытия поверхности.
Эти данные объясняют высокую активность атомов Pt на ступенях в реакциях с участием СО.
Еще один пример влияния структуры поверхности на каталитическую активность - разложение ацетонитрила на никеле (Рис. 5.31).
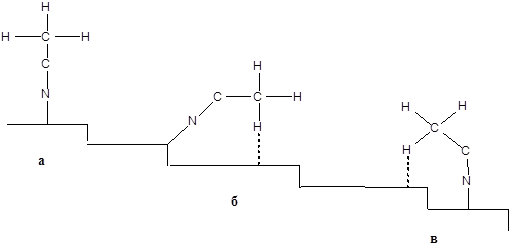
Рис. 5.31. Адсорбция и разложение ацетонитрила на поверхности Ni.
Было установлено, что на гладких поверхностях (111) адсорбция ацетонитрила слабая и обратимая, а расщепление протекает значительно медленнее, чем на плоскости (110), которая имеет более высокую плотность ступенек.
Это объясняется тем, что молекула ацетонитрила всегда адсорбируется через атом азота и нитрильная группа располагается перпендикулярно поверхности. Таким образом, на ровной поверхности (Рис. 5.31а) геометрически не может произойти взаимодействие СН3-группы с поверхностью, и молекула остается не достаточно активированной. На изломе, ступени или рядом со ступенью происходит активирование водорода метильной группы и молекула легко подвергается разложению (Рис. 5.31 б,в).
Как следует из рассмотренных примеров, скорость каталитической реакции во многих случаях сильно зависит от геометрического строения активного центра. Наблюдаемая скорость гетерогенно-каталитической реакции складывается из суммы скоростей реакций, протекающих на разных каталитических центрах поверхности. Очевидно, что суммарная, наблюдаемая скорость реакции пропорциональна концентрации активных центров (на единицу массы катализатора), которая, в свою очередь пропорциональна удельной поверхности частиц катализатора.
Удельную поверхность металлических нанесенных катализаторов характеризуют дисперсностью.
Дисперсность (степень дисперсности) - это отношение числа поверхностных атомов к общему числу атомов активного компонента.
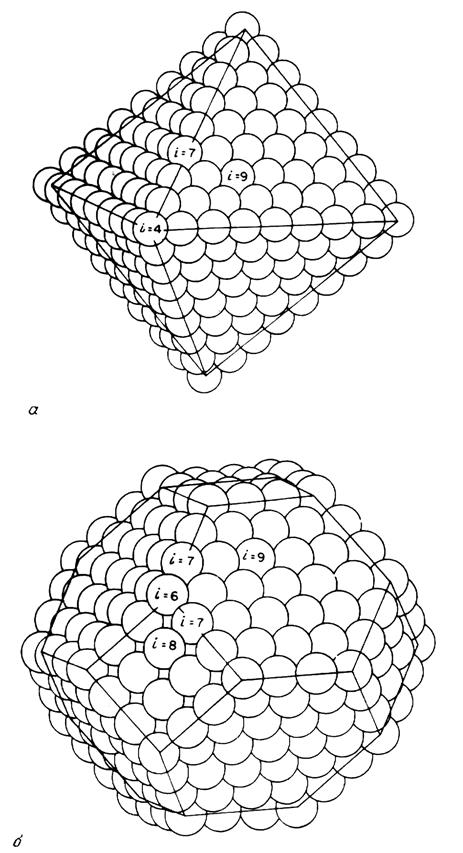
Рис. 5.32. Расположение поверхностных атомов в кристаллитах платины: а) октаэдрической конфигурации; б) кубоктаэдрической конфигурации.
Рассмотрим зависимость дисперсности от размера частицы на примере идеального октаэдрического кристалла платины (Рис. 5.32 а). Самый маленький кристалл представляет собой октаэдр из шести атомов (по 2 атома в каждом ребре), каждый из которых расположен на поверхности кристалла. Значит дисперсность равна 1 (или 100%), так как:
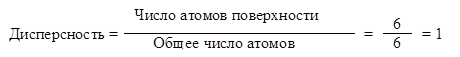
Следующий по размеру кристалл платины содержит по 3 атома в ребре и состоит из 19 атомов, из которых 18 атомов находятся на поверхности. Соответственно дисперсность, в данном случае, составляет 18:19 = 0,947 » 0,95 (или 95%). В Таблице 5.10 приведены данные по дисперсности для следующих, более крупных, кристаллов платины. Для частицы платины размером 1 мкм дисперсность составляет 0,001. В высокоэффективных промышленных платиновых катализаторах дисперсность нанесенной платины, как правило, выше 0,5.
На Рисунке (5.32 а) видно, что атомы поверхности платины можно разделить на три типа по координационному числу:
- атомы на гранях имеют координационное число 9;
- атомы на ребрах имеют координационное число 7;
- атомы на углах имеют координационное число 4.
Соотношение поверхностных атомов с различным координационным числом также зависит от размера кристалла, то есть от дисперсности. Например, самый маленький октаэдрический кристалл (число атомов = 6) состоит только из угловых атомов с координационным числом 4. В Таблице 5.10 приведено среднее координационное число атомов поверхности для кристаллов различной дисперсности.
Таблица 5.10.
Дисперсность и среднее координационное число поверхностных атомов в октаэдрических кристаллах платины.
| Ребро кристалла | Дисперсность, % | Общее число атомов в кристалле | Среднее координационное число поверхностных атомов | |
| Число атомов в ребре | Длина ребра, нм | |||
| 0,550 0,895 1,100 1,375 1,650 1,925 2,200 2,475 2,750 3,025 3,300 3,575 3,850 4,125 4,400 4,675 4,950 | 4,00 6,00 6,94 7,46 7,76 7,97 8,12 8,23 8,31 8,38 8,44 8,47 8,53 8,56 8,59 8,62 8,64 |
Установлено, что для благородных металлов при высокой дисперсности преобладают угловые атомы; максимальное количество атомов на ступеньках достигается при средней дисперсности; террасы преобладают при низкой дисперсности. Поскольку каталитическая активность поверхностных атомов зависит от их координационной насыщенности, то естественно ожидать, что с уменьшением размеров частиц катализатора (т.е. с увеличением дисперсности) в некоторых реакциях должна изменяться наблюдаемая каталитическая активность.
По этому признаку каталитические реакции делят на:
Структурно-чувствительные - это реакции, для которых удельная активность или число оборотов на одном активном центре зависит от размера частиц катализатора;
Структурно-нечувствительные - это реакции для которых удельная активность или число оборотов на одном активном центре не зависит от размера частиц катализатора.
К структурно-чувствительным реакциям, как правило относятся те, которые протекают с разрывом связей в молекуле реагента, и активация реагентов происходит на полиядерных центрах.
Структурно-нечувствительные реакции, это, как правило, реакции в которых активированный реагент связан с одним атомом поверхности катализатора (одноцентровая хемосорбция).
Причем, одна и та же реакция может быть структурно-чувствительной на одном катализаторе и структурно-нечувствительной на другом. Примеры реакций обоих типов приведены в Таблице 5.11.
Таблица 5.11.
Примеры структурно-чувствительных и структурно-нечувствительных реакций.
| Структурно-чувствительные реакции | Структурно-нечувствительные реакции |
| Гидрогенолиз: Этан (Ni); Метилциклопентан (Pt) Циклогексан (Pt) Гидрирование: Бензол (Ni) Этилен (Ni) Изомеризация: Бутан, Гексан (Pt) Окисление: углеводородов (Pt); аммиака (Pt); Дегидролциклизация: Гексан, Гептан (Pt) Синтез аммиака (Fe) Гидродесульфирование (Re) | Гидрирование: Бензол (Pt) Этилен (Pt) Кетоны (Cu) Дегидрирование: Циклогексан (Pt) Окисление: СО Этилена до этиленоксида (Ag) Гидродесульфирование (Mo) |
Дата добавления: 2020-07-18; просмотров: 686;











