ПРОИЗВОДСТВО АММИАКА
Для нормальной жизнедеятельности растений и животных азот необходим только в усвояемой форме. Однако из-за высокой химической инертности азота его неисчерпаемые ресурсы * живой природе практически недоступны. Для решения продовольственной проблемы человечество переводит азот в усвояемую форму, «связывая» его до простейшего соединения — аммиака, из которого затем получают азотную кислоту и минеральные удобрения.
Темпы роста производства аммиака постоянно увеличиваются. При этом количественный рост производства сопровождается качественными изменениями структуры производственной базы. Укрупняются мощности единичных агрегатов синтеза аммиака **[6] внедряются новые эффективные катализаторы и сорбенты, разрабатываются прогрессивное оборудование и технологические схемы, обеспечивающие более полное использование сырья и топлива. В последние годы за счет лучшей утилизации теплоты производство аммиака удается организовать по энерготехнологическому принципу, в котором процесс полностью самообеспечивает себя паром и механической энергией.
Производство аммиака состоит из трех стадий: получение азотоводородной смеси, ее очистка и собственно синтез аммиака.
Первая стадия — получение азотоводородной смеси. Сырьем для производства аммиака являются азот и водород. Азот выделяют из воздуха — газовой смеси, содержащей по объему 78,05% азота, 20,95% кислорода, 0,94% аргона и в незначительных количествах углекислый газ, неон, гелий, криптон и ксенон. Для этого воздух глубоким охлаждением переводят в жидкое состояние, а затем ректификацией, основанной на различии температур кипения отдельных газов, разделяют на составные части.
Водород получают одним из способов: электролизом воды или водных растворов поваренной соли; из коксового газа последовательным сжижением всех его компонентов, кроме водорода; конверсией оксида углерода генераторного газа; конверсией метана или его гомологов.
Получение водорода — наиболее дорогая стадия производства. В настоящее время большую часть водорода для синтеза аммиака получают из наиболее дешевых видов сырья — газов, содержащих метан и его гомологи. К ним относятся попутные газы нефтедобычи, природный газ, газы нефтепереработки. В присутствии водяного пара и кислорода метан превращается в водород:
 СН4 + Н2О СО + Н2 - Q
СН4 + Н2О СО + Н2 - Q
 СН4+ 0.5O2 СО + 2Н2 + Q
СН4+ 0.5O2 СО + 2Н2 + Q
а образовавшийся оксид углерода конвертируется до СО2 и Н2:
 СО + Н20 С02 + Н2 + Q
СО + Н20 С02 + Н2 + Q
Конверсию природного газа проводят при атмосферном или повышенном давлении с применением катализаторов (каталитическая конверсия) или без них (высокотемпературная конверсия). Часто процесс на никелевом катализаторе ведут так, чтобы остаточная концентрация метана составляла 8 — 10%. При такой концентрации метана его дальнейшее конвертирование воздухом (т. е. смесью азота и кислорода в соотношении 4:1) позволяет получить сразу азотоводородную смесь с соотношением N2: Н2 = = 1:3. Это исключает необходимость строительства дорогостоящих и энергоемких установок разделения воздуха и значительно улучшает технико-экономические показатели процесса.
Однако полученные азот, водород и азотоводородная смесь загрязнены попавшими из природного газа соединениями серы, а также оксидами и диоксидами углерода, образовавшимися при конверсии. Из-за высокой чувствительности катализатора синтеза аммиака к этим примесям, сильно снижающим его активность и вызывающим необратимые отравления (особенно соединения, содержащие серу), газ подвергают тщательной очистке.
Вторая стадия — очистка газа. Для удаления примесей сернистых соединенийтипа сероуглерода CS2, сероокиси углерода COS и меркаптанов R —SH их гидрируют на кобальтмолибденовом катализаторе при температуре 350-450 °С до легкоулавливаемого сероводорода
 9Н2 + примеси (CS2 + COS + R - SH) 4H2S + 2CH4 4+ H2O
9Н2 + примеси (CS2 + COS + R - SH) 4H2S + 2CH4 4+ H2O
Образовавшийся сероводород удаляют из газа с помощью различных поглотителей, например оксида цинка: ZnO + H2S à ZnS + Н2О
После такой очистки газ содержит сероводорода не более 1 мг/м3.
Очистка газа от СО2 производится с помощью жидких поглотителей. На смену водной очистке, потреблявшей большое количество воды и энергии на ее перекачку, пришла более эффективная очистка с помощью водных растворов этаноламинов либо горячих растворов поташа, активированных мышьяком. При промывке газа указанными водными растворами примеси СО2 образуют карбонаты и бикарбонаты. Регенерация поглотителей с удалением СО2 в десорбере производится: для этаноламинов — нагреванием до 120 °С, для растворов поташа — снижением давления.
Примеси СО удаляются из газа поглощением мед-ноаммиачным раствором слабой уксусной или муравьиной кислоты. Эффективность очистки увеличивается с повышением давления до 30 МПа и понижением температуры до 25 — 0 °С. После очистки в газе остается не более 0,003% СО. При очистке азотоводородной смеси, получаемой из коксового газа, остатки СО удаляют промывкой жидким азотом. При этом часть азота испаряется и переходит в азотоводородную смесь, обеспечивая соотношение N2 : Н2, близкое 1:3. Разбавляя смесь дополнительным количеством азота, ее доводят до необходимого для синтеза аммиака точного соотношения N2: Н2 = 1:3. В тех случаях, когда остаточные количества СО и СО2 в газе небольшие (до 1 %), удаление примесей осуществляется их гидрированием (метанирова-нием) по реакциям

 СО + ЗН2 СН4 + Н2О; СО2 + 4Н2 СН4 + 2Н2О
СО + ЗН2 СН4 + Н2О; СО2 + 4Н2 СН4 + 2Н2О
Температура процесса 200 — 400 °С, катализатор — никель, нанесенный на оксид алюминия.
Третья стадия — синтез аммиака. Образование аммиака по реакции
 N2+3H2 2NH3 + Q протекает достаточно быстро только в присутствии катализаторов, содержащих в качестве активаторов оксиды алюминия, калия и кальция. Тепловой эффект реакции растет с увеличением температуры, а равновесный выход зависит не только от температуры, но и от давления.
N2+3H2 2NH3 + Q протекает достаточно быстро только в присутствии катализаторов, содержащих в качестве активаторов оксиды алюминия, калия и кальция. Тепловой эффект реакции растет с увеличением температуры, а равновесный выход зависит не только от температуры, но и от давления.
Синтез аммиака является обратимым экзотермическим процессом. В соответствии с принципом Ле-Шателье отвод теплоты должен смещать реакцию вправо. С этой целью промежуточное охлаждение газовой смеси менее нагретым встречным потоком производится после каждого ее контакта с катализатором. Это обеспечивает автотермичность процесса. Однако несмотря на отвод теплоты, температура по ходу процесса все же несколько увеличивается. Поэтому в колонне синтеза аммиака используются катализаторы, эффективно работающие в различных диапазонах температур.
Современные колонны синтеза аммиака большой единичной мощности имеют четыре полки с катализаторами. На первой (по ходу газа) находится низкотемпературный катализатор (350— 500 °С), на второй — средне-температурный (400 —550 °С); на третьей и четвертой — высокотемпературные (550 — 700 °С).
На фактический выход аммиака кроме перечисленных факторов оказывают влияние активность катализатора, состав газовой смеси, конструктивные особенности аппарата (чем меньше в них гидравлическое сопротивление, тем выше пропускная способность и ниже энергетические затраты) и продолжительность соприкосновения газа с катализатором (или обратная величина, называемая объемной скоростью газа). С увеличением объемной скорости съем аммиака с 1 м3 контактной массы резко возрастает. Но одновременно с этим увеличивается объем непрореагировавшей азотоводородной смеси. Во избежание потерь эту смесь необходимо многократно прокачивать через катализатор по замкнутому циклу. Это повышает расход энергии на перекачку. С экономической точки зрения подобные затраты могут быть сведены к минимуму при некоторых оптимальных значениях объемной скорости газа (от 15000 до 30000 м3 газовой смеси через 1 м3 катализатора в час).
Технико-экономические показатели этого производства могут быть улучшены переходом к энерго-, ресурсо-и трудосберегающей технологии. Это достигается применением агрегатов большой единичной мощности, маловодных схем и АСУТП. Особое внимание уделяется утилизации теплоты топочных газов, выходящих из печи нагрева метана, а также газовых потоков, покидающих реактор гидрирования органической серы, конвертеры метана и оксида углерода, колонны синтеза аммиака, метанатора и т. д.
Утилизированная высокопотенциальная теплота используется для получения пара высокого давления. Энергия этого пара в турбинах преобразуется в механическую для сжатия и перемещения газов с помощью компрессоров. Низкопотенциальная теплота утилизируется для получения технологического пара низкого давления, подогрева воды, получения холода и т. п. Подобный принцип энергосбережения самообеспечивает процесс паром и механической энергией. Для районов, испытывающих недостаток в топливе, это позволяет организовать производство с минимальными энергозатратами. Замена же водяного охлаждения воздушным значительно сокращает и водопотребление. Указанные принципы используются в современных схемах производства аммиака на агрегатах большой (1500 т/сут) единичной мощности. Один такой агрегат обеспечивает годовую экономию эксплуатационных затрат в сумме 15 млн. руб. и капиталовложений до 25 млн. руб. Указанная схема включает блоки получения азотоводородной смеси, очистки газа и синтеза аммиака.
|
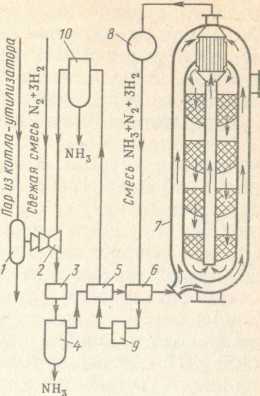
В блоке синтеза аммиака для сжатия азотоводородной смеси до 30 МПа и ее циркуляции утилизированная теплота превращается в механическую энергию сжатия и перемещения (рис. 7.6). Для этого водяной пар высокого давления и температуры, полученный в котле-утилизаторе, направляют на паровую турбину 7, на валу которой установлен турбокомпрессор 2. Турбокомпрессор сжимает свежую азотоводородную смесь, а в последней ступени еще и смешивают ее с непрореагировавшей на катализаторе возвратной смесью N2 + 3H2, содержащей до 2 - 3 % NH3. Для улавливания аммиака газ после турбокомпрессора пропускают через аммиачный холодильник 3, где он конденсируется и в виде жидкости легко отделяется в сепараторе 4. После сепаратора смесь азота и водорода проходит через два теплообменника 5 и 6, нагревается до 425 °С
и направляется в полочную колонну синтеза 7. По сравнению с традиционным контактным аппаратом с двойной теплообменной трубкой в полочных радиальных колоннах гидравлическое сопротивление, а следовательно, и энергопотери значительно снижены. В такой колонне с внутренним диаметром до 2,1 м, высотой до 25 м и толщиной стенок из хромомолибденовой стали 10 — 30 см имеется четыре полки. Полки загружаются катализатором в возрастающем количестве и с возрастающим диапазоном рабочих температур от первой к последней.
Для поддержания заданного температурного режима по высоте колонны после каждой полки производят отвод теплоты экзотермической реакции в котел-утилизатор. Тонкое регулирование температуры достигается введением в горячую газовую смесь определенного количества холодной смеси.
Примерно 15-20% азотоводородной смеси на катализаторе превращается в аммиак. Выйдя из колонны синтеза с температурой 320 — 380 °С, смесь последовательно отдает теплоту питательной воде котла-утилизатора в водоподогревателе 8, а затем нагревает встречный холодный газовый поток в «горячем» теплообменнике 6. Далее она охлаждается в аппарате воздушного охлаждения 9 и «холодном» теплообменнике 5. При давлении около 30 МПа в такой газовой смеси аммиак конденсируется уже при температуре 25 — 40 °С и после отделения в сепараторе 10 направляется в хранилище.
Газовая смесь, содержащая до 2 - 3 % несконденсировавшегося аммиака, и непрореагировавшие азот и водород турбокомпрессором 2 возвращаются в производственный цикл.
Степень превращения азотоводородной смеси в аммиак в колонне синтеза колеблется от 15 до 20%. Но благодаря многократной ее циркуляции по замкнутой схеме фактический выход аммиака в системах среднего давления составляет 91 — 95%. По сравнению с системами, работающими при низком (10 МПа) и высоком (100 МПа) давлении, в системах среднего давления, получивших в мировой практике наибольшее распространение, удачно решаются вопросы выделения аммиака при достаточной скорости процесса в контактном аппарате. Помимо жидкого аммиака получают и газообразный, который обычно тут же перерабатывается в мочевину, аммиачную селитру, азотную кислоту.
Дата добавления: 2016-06-22; просмотров: 7559;











