ПРИНЦИП ЛЕ–ШАТЕЛЬЕ.
Как отмечалось ранее, химические равновесия являются динамичными и подвижными. При изменении внешних условий может происходить сдвиг равновесия в сторону образования либо продуктов реакции, либо исходных веществ. Впервые принцип смещения равновесия сформулировал А. Ле-Шателье.
Принцип Ле–Шателье: если на систему, находящуюся в равновесии, оказывать внешнее воздействие, то равновесие смещается в сторону того процесса, который уменьшает это воздействие.
Теоретически этот принцип был основан Ф. Брауном и теперь известен, как принцип Ле-Шателье – Брауна.
Математически этот принцип может быть представлен в виде:
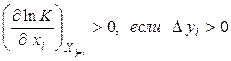 ,
,
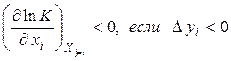 , (4.11)
, (4.11)
где 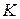 – константа равновесия, xi– обобщенная сила, yi– обобщенная сопряженная данной силе xi координата. Неравенство (4.11) имеет следующий смысл: изменение обобщенной силы (интенсивный параметр) при постоянстве остальных сил смещает равновесие в таком направлении, при котором изменение сопряженной обобщенной координаты препятствует изменению обобщенной силы. Если рассматривают влияние температуры (обобщенной силы) при постоянстве других интенсивных параметров на химическое равновесие, то в качестве сопряженной координаты используют тепловой эффект реакции. Чем больше по величине тепловой эффект реакции, тем сильнее влияет на положение равновесия изменение температуры. При изменении давления – обобщенной силы – сопряженной обобщенной координатой будет изменение объёма в ходе реакции, взятое с обратным знаком.
– константа равновесия, xi– обобщенная сила, yi– обобщенная сопряженная данной силе xi координата. Неравенство (4.11) имеет следующий смысл: изменение обобщенной силы (интенсивный параметр) при постоянстве остальных сил смещает равновесие в таком направлении, при котором изменение сопряженной обобщенной координаты препятствует изменению обобщенной силы. Если рассматривают влияние температуры (обобщенной силы) при постоянстве других интенсивных параметров на химическое равновесие, то в качестве сопряженной координаты используют тепловой эффект реакции. Чем больше по величине тепловой эффект реакции, тем сильнее влияет на положение равновесия изменение температуры. При изменении давления – обобщенной силы – сопряженной обобщенной координатой будет изменение объёма в ходе реакции, взятое с обратным знаком.
Итак, повышение (или понижение) температуры системы смещает равновесие в том направлении (прямом или обратном), в котором поглощается (или выделяется) теплота. Повышение давления смещает равновесие в направлении уменьшения объёма системы.
Пример 3.2.Рассмотрим реакцию
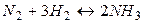 (
( 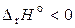 )
)
1. Увеличим температуру: так как реакция экзотермическая, т. е. идёт с выделением тепла, равновеие смещается в сторону исходных веществ (обратная реакция идёт с поглощением тепла).
2. Увеличим давление: так как прямая реакция идёт с уменьшением числа молей газобразных веществ (т.е. объем уменьшается), то равновесие смещается в сторону продуктов реакции.
Дата добавления: 2016-06-18; просмотров: 1879;











