Растворимость твердых веществ в жидкостях
Количество растворенного вещества в насыщенном растворе, отнесенное к определенному количеству раствора или растворителя, называется растворимостью (табл. 1.1). ?
Растворимость твердых веществ в воде не является постоянной величиной, а изменяется в значительных пределах в зависимости от температуры. Растворимость-это функция от температуры.
Для большинства солей растворимость в воде с повышением температуры растет; для некоторых солей она понижается (CaCrO4, MnSO4, NaSO4 и др.), и избыток соли выпадает в виде кристаллов.
У поваренной соли NaCI растворимость от температуры практически не зависит [1].
Присутствие кристаллов в растворе при выпаривании нежелательно, так как они осаждаются на стенках аппарата и поверхностях нагрева кипятильников и образуют слой накипи или осадка, которые снижают теплопередачу и ухудшают работу выпарных аппаратов.
Таблица 1.1. Растворимость некоторых веществ в воде при температуре 20 оС
| Вещество | Растворимость в воде г/100 г H2О | Концентрации насыщенного раствора, % | Вещество | Растворимость в воде г/100 г H2О | Концентрации насыщенного раствора, % |
| NaCI | 35,8 | 26,4 | BaSO4 | 0,00023 | 0,00023 |
| КCI | 34,2 | 25,5 | Mg(OH)2 | 0,001 | 0,001 |
| Na2СO3 | 21,2 | 17,6 | CaCO3 | 0,0014 | 0,0014 |
| NaOН | 107,0 | 51,7 | Ca(OH)2 | 0,16 | 0,16 |
| ВаCI | 35,6 | 26,3 | NaSO4 | 32,8 | 24,7 |
| СаSO4 | 0,2 | 0,2 | MgCI2 | 35,3 | 26,1 |
Процесс выпаривания характерен значительным изменением физико-химических свойств растворов, связанных с изменением его концентрации.
С повышением концентрации
1. увеличиваются плотность и вязкость,
2. понижаются удельная теплоемкость ср, теплопроводность и интенсивность теплоотдачи,
3. изменяется теплота растворения [1].
Плотность раствора
Плотность раствора можно легко определить по правилу аддитивности, зная его концентрацию и плотности чистых компонентов при данной температуре:
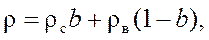 , (1.2)
, (1.2)
где 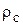 - плотность безводного нелетучего вещества, кг/м3;
- плотность безводного нелетучего вещества, кг/м3;
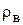 - плотность растворителя (воды), кг/ м3.
- плотность растворителя (воды), кг/ м3.
Дата добавления: 2016-05-28; просмотров: 4308;











