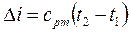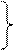Термодинамічні процеси ідеальних газів
Ізохорний процес
Ізохорним називають процес, який протікає з постійним об'ємом V=const.
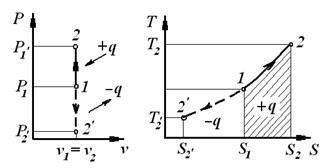
| 1. 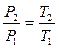 - закон Шарля.
2. - закон Шарля.
2. 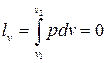 3.
3. 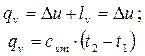
| |||
Процеси:
1– 2 – підведення теплоти;
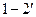 – відведення теплоти. – відведення теплоти.
|
6. 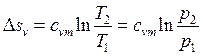
7. Схема енергобалансу: теплота, що підводиться, витрачається на зміну внутрішньої енергії.
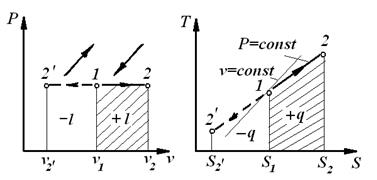
Ізобарний процес
Ізобарним називається процес, який протікає з постійним тиском P=const.
| 1. 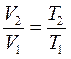 – закон Гей-Люссака.
2. – закон Гей-Люссака.
2. 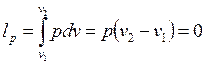 .
3. .
3. 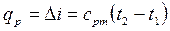 .
6. .
6. 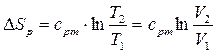 . .
|
Процеси:
1– 2 – розширення, підведення теплоти;
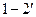 – стиск, відведення теплоти. – стиск, відведення теплоти.
| |
| 7. Схема енергобалансу: теплота, що підводиться, витрачається на здійснення роботи і зміну внутрішньої енергії. |
Ізотермічний процес
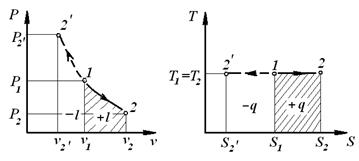
Ізотермічним називають процес, який протікає з постійною температурою T=const. Підкоряється рівнянню 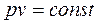 . У P-V координатах ізотерма являє собою рівнобічну гіперболу.
. У P-V координатах ізотерма являє собою рівнобічну гіперболу.
| 1. Закон Бойля – Маріотта.
2. 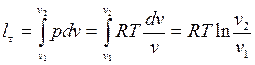 ΔuT=0; ΔiT=0.
3.
ΔuT=0; ΔiT=0.
3. 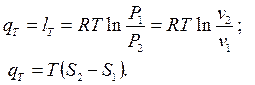 6.
6. 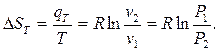
|
Процеси: 1-2 – розширення, підведення теплоти;
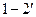 - стиск, відведення теплоти. - стиск, відведення теплоти.
|
7. Схема енергобалансу: теплота, що підводиться, витрачається на зміну внутрішньої енергії.
Адіабатний процес
Адіабатним (ізоентропним) називається процес, який протікає без теплообміну з навколишнім середовищем, з постійною ентропією S=const. У P-V координатах адіабата являє собою нерівнобічну гіперболу, показник адіабати 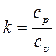 .
.
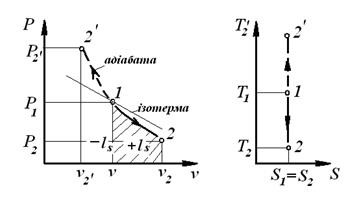 Процеси: 1-2 – розширення,
Процеси: 1-2 – розширення,
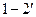 - стиснення. - стиснення.
| 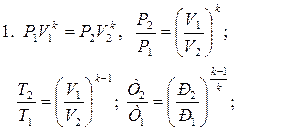 2. ls=Δu;
2. ls=Δu;
|
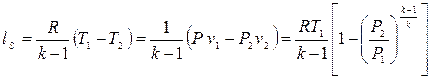
3. qs=0.
6. 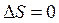 .
.
7. Схема енергобалансу: робота здійснюється за рахунок зменшення внутрішньої енергії.
Політропний процес
Політропним називається процес, який протікає з постійною теплоємністю 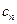 =const і підкоряється рівнянню Pvn=const, де n-показник політропи.
=const і підкоряється рівнянню Pvn=const, де n-показник політропи.
| 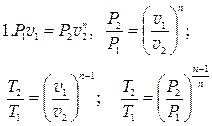 
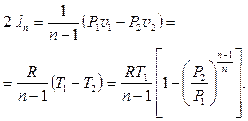
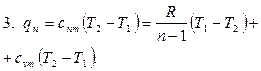
|
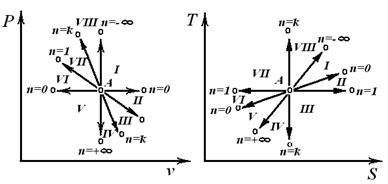
| Області: I÷IV – розширення робочого тіла, позитивна робота; V÷VIII – стиск робочого тіла, негативна робота; I÷III,VIII – підведення теплоти; IV÷VIII – відведення теплоти; VII, VIII, I, II – підвищення температури тіла; III, IV, V, VI – зниження температури тіла. | |
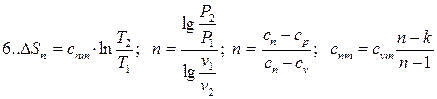
| |
В залежності від величини n поле діаграми P-v і T-S ділиться на вісім частин. Усі процеси починаються в точці А. 
|
Дата добавления: 2020-02-05; просмотров: 1267;

 5.
5.