Физико – химические характеристики природных вод
Природные воды – это сложные системы, содержащие:
1) растворенные вещества в виде ионов и молекул, минеральные и органические соединения в форме коллоидов, суспензий и эмульсий;
2) растворенные газы, входящие в состав атмосферы;
3) вещества, образующиеся в результате жизнедеятельности водных организмов и протекания процессов химического взаимодействия в самой воде.
Формирование состава природных вод происходит в результате взаимодействия воды с окружающей средой. При этом протекают процессы:
А) растворение соединений;
Б) химическое взаимодействие веществ с водой;
В) биохимические реакции;
Г) коллоидно – химические взаимодействия.
Эти процессы определяются:
1) температурой,
2) давлением,
3) геологическими особенностями.
На формирование природных вод заметно влияет хозяйственная деятельность человека.
Многообразие природных вод по химическому составу отражено в классификации Вернадского В.И. По ней выделено 485 видов вод с учетом солесодержания, преобладающего иона, наличия специфических компонентов.
По солесодержанию природные воды делятся на следующие виды:
1) пресные до 1 г/кг;
2) солоноватые до 25 г/кг;
3) воды с морской соленостью – 25 -50 г/кг;
4) соленые воды > 50 г/кг.
По химическому составу достаточно полной является классификация О.А. Алексеева.
По преобладающему аниону воды делятся на 3 класса:
1. Карбонатные (С).
2. Сульфатные (S).
3. Хлоридные (Cl).
По преобладающему катиону классы делятся на 3 группы:
1. Кальциевая группа (Ca).
2. Магниевая группа (Mg).
3. Натриевая группа (Na).
Группы делятся на типы, указывающие на соотношение между ионами (мг –экв.).
I тип – HCO3- < Ca2+ + Mg2+ - это мягкие воды с небольшим солесодержанием с преобладанием ионов Na+ и К+.
II тип - HCO3- < Ca2+ + Mg2+ < HCO3- + SO42- - это воды большинства рек и озер, и подземные воды с малым или средним солесодержанием.
III тип - HCO3- + SO42 < Ca2+ + Mg2+ или Cl- > Na+ - это воды морей и океанов и минеральные воды.
IV тип - HCO3- = О - это кислые воды. Они могут быть только в сульфатных (S) или хлоридном (Сl) классах в группах Сa и Mg.
По этой классификации можно кратко характеризовать воды: например,
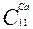 - вода гидрокарбонатного класса, группы Сa тип II.
- вода гидрокарбонатного класса, группы Сa тип II.
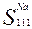 - сульфатный класс, группа натрия III тип.
- сульфатный класс, группа натрия III тип.
Концентрация основных ионов в природных водах зависит от солесодержания. Содержание ионов лимитируется образованием труднорастворимых соединений.
Дата добавления: 2020-02-05; просмотров: 844;











