Происходит дальнейшее хлорирование
С6Н5Сl + Сl2 → С6Н4Сl2 + НСl
или
С6Н6 + 2Сl2 → С6Н4Сl2 + 2НСl (2)
С6Н4Сl2 + Сl2 → С6Н3Сl3 + НСl или С6Н6 + 3Сl2 → С6Н3Сl3 + 3НСl (3)
Чтобы предотвратить образование больших количеств полихлоридов хлорирование следует прекращать при содержании в реакционной смеси несколько больше половины непрореагировавшего бензола (60 – 65%). Мол. масса: С6Н6 – 78; С6Н5Сl – 112,5; С6Н4Сl2 – 147; С6Н3Сl3 – 181,5; Сl2 – 71; НСl - 36,5.
Согласно заданному составу жидких продуктов реакции, в продукционной (жидкой) смеси находится С6Н5Сl – 1000 кг; С6Н4Сl2 –  = 78 кг; С6Н3Сl3 –
= 78 кг; С6Н3Сl3 –  = 15,6 кг
= 15,6 кг
В составе продукционной смеси кроме того находится хлористый водород, полученный:
по реакции (1)
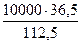 = 324 кг
= 324 кг
по реакции (2)
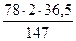 = 39 кг
= 39 кг
по реакции (3)
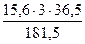 = 9,4 кг
= 9,4 кг
Всего хлористого водорода в продукционной смеси 372,4 кг.
Для получения 1т С6Н5Сl требуется чистого бензола:
на образование С6Н5Сl
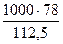 = 693 кг
= 693 кг
на образование С6Н4Сl2
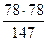 = 41 кг
= 41 кг
на образование С6Н3Сl3
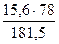 = 6,7 кг
= 6,7 кг
непрореагировавшего бензола
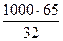 = 2031,0 кг
= 2031,0 кг
Всего бензола 2771,7 кг.
Технического бензола расходуется
 = 2842,8 кг
= 2842,8 кг
Расход хлора.
На образование С6Н5Сl
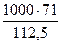 = 631 кг
= 631 кг
на образование С6Н4Сl2
 = 75 кг
= 75 кг
на образование С6Н3Сl3
 = 18,3 кг
= 18,3 кг
Всего расходуется хлора 724,3 кг.
Технического хлора расходуется
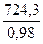 = 739 кг
= 739 кг
Результаты расчетов сведены в таблицу:
Дата добавления: 2021-12-14; просмотров: 648;











