Структурна класифікація білків, які взаємодіють із ДНК
Так само, як більшість глобулярних білків можна вписати в обмежений набір стандартних укладок глобули, структурні елементи білків, які безпосередньо взаємодіють з ДНК, можна розділити на досить обмежену кількість стандартних типів – ДНК-зв’язувальних структурних мотивів.
Мотив НТН (helixturn helix, спіраль–поворот–спіраль), приклад якого зображено на рис. 13, є найбільш розповсюдженим. Мотив складається із двох α-спіралей, часто майже перпендикулярних одна до одної, з’єднаних короткою перемичкою. Одна із цих спіралей (яка впізнає) виконує роль головки, що читає, взаємодіючи з екзоциклічними групами азотистих основ у великому жолобку подвійної спіралі. Орієнтація цієї спіралі відносно ДНК може варіювати для різних білків від приблизно перпендикулярної відносно осі подвійної спіралі до паралельної цукрофосфатному остову. Друга α-спіраль часто утворює допоміжні контакти з цукрофосфатним остовом. Взаємодія α-спіралі з великим жолобком часто зустрічається і для інших ДНК-зв’язувальних мотивів. Причина полягає в майже точній просторовій відповідності між цими двома елементами − можна сказати, що α-спіраль є просторово комплементарною великому жолобку.
Двоспіральний НТН-мотив утримується в структурі того чи іншого структурного домену − у випадку репресора фага λ, у структурі α-спірального пучка (рис. 14, а). Часто білки, що містять НТН-мотив, взаємодіють з ДНК у вигляді гомодимеру (дві однакові субодиниці) − це особливо характерно для прокаріотичних білків. Тоді дві однакові читаючі головки впізнають дві однакові послідовності, що симетрично розташовані в сайті взаємодії.
Інший приклад такого ж типу − катаболітний активаторний білок (CAP − Catabolite Activator Protein) Escherichia coli (рис. 14, б). При взаємодії гомодимеру САР зі специфічним сайтом відбувається досить значний вигин ДНК у бік білка (подвійна спіраль огортає білок). Спорідненість білка до цього сайта залежить від ліганду − сАМР (циклічного АМР − 5′ фосфат у складі нуклеотиду утворює внутрішній ковалентний зв’язок з 3′-ОН-групою рибози). Зв’язування сАМР індукує структурні змінив молекулі білка, у результаті змінюється робоча поверхня і білок набуває здатності впізнавати специфічну послідовність.
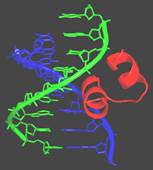
Рис. 13. НТН-мотив репресора бактеріофага λ у комплексі з ДНК (1LMB).
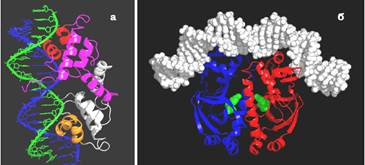
Рис. 14. Комплекси з ДНК гомодимерів репресора бактеріофага λ (а, 1LMB) і білка САР E. coli
(б, 1CGP − зеленим кольором позначено молекули сАМР).
Розповсюджений клас білкових мотивів, що взаємодіють із ДНК, − Zn-координуючі мотиви. Це дуже невеличкі структурні елементи, які складаються з обмеженої, недостатньої для формування жорсткої глобули, кількості сегментів вторинної структури. Іон цинку надає жорсткості такому мотиву, утворюючи координаційні зв’язки з чотирма амінокислотними залишками, частіше Cys або His. Координаційний зв’язок формується неподіленою парою електронів атомів O, N або S, яка узагальнюється з атомом металу шляхом часткового перетікання на його низьку незаповнену орбіталь. Чотири такі зв’язки створюють жорсткий каркас, який утримує білкову поверхню, що має взаємодіяти з ДНК.
Один зі структурних мотивів такого типу, що часто зустрічається, − цинковий палець (Zn finger, рис. 15, а). Він має дуже просту будову: одна α-спіраль і маленький β-шар із двох β-ділянок; одна з них і α-спіраль містять залишки, що утворюють координаційні зв’язки з Zn.
Як правило, кілька таких пальців (три на рис. 15, а), з’єднаних перемичкою, спірально обгортають великий жолобок.
Інший приклад – ДНК-зв’язувальний домен гормонового рецептора (рис. 15, б). Гормонові рецептори − це еукаріотичні фактори транскрипції, здебільшого гомодимери, які набувають споріденості з певними елементами послідовності ДНК після зв’язування з білком стероїдного гормону. ДНК-зв’язувальний домен має дві пари структурних елементів, а саме α-спіраль − суміжна нерегулярна петля, кожна пара координує іон Zn. Одна пара елементів бере участь у димеризації, інша − у взаємодії з ДНК. Зустрічаються також інші Zn-координуючі мотиви, але всі вони, як і розглянуті, реалізують взаємодію α-спіралі з великим жолобком.
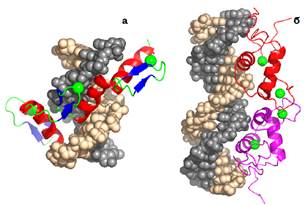
Рис. 15. Три цинкових пальця у складі ДНК-зв’язувального білка (а, 1ZAA) і ДНК-зв’язувальний домен (димер) глюкокортикоїдного рецептора (б, 1GLU). Зелені сфери − іони Zn.
Ще один мотив, який взаємодіє з великим жолобком ДНК за рахунок α-спіралей − лейциновий зіпер (Leu zipper, рис. 16). Він являє собою дві довгі α-спіралі, кожну з яких можна розділити на дві частини. Одна частина обох спіралей здійснює димеризацію − за рахунок гідрофобних взаємодій між неполярними амінокислотними залишками (часто Leu, звідки назва мотиву) утворюється трохи закручена подвійна спіраль (coiled coil). Друга частина кожної α-спіралі взаємодіє з великим жолобком ДНК.
Варіацією лейцинового зіпера є мотив спіраль−петля−спіраль (helix − loop − helix) − різниця лише в тому, що кожна довга α-спіраль розділена на дві коротші, з’єднані петлею: одна пара спіралей взаємодіє між собою, інша − з ДНК.
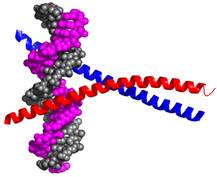
Рис. 16. Лейциновий зіпер (1NWQ)
Усе це не означає, що тільки α-спіраль використовується для взаємодії білків з великим жолобком ДНК. У великий жолобок добре вкладається також β-шар із двох β-ділянок − саме такий шар є взаємодіючим елементом для білків типу метіонінового репресора. Численний клас білків становить родину імуноглобуліноподібних траскрипційних факторів (глобула має укладку імуноглобулінового типу), які реалізують взаємодії перемичок між ділянками β-структури з великим жолобком. Отже, хоча α-спіраль використовується частіше, реалізуються і всі інші можливості.
Усе описане не означає також, що білки взаємодіють з ДНК тільки через великий жолобок (хоча через великий − частіше). На рис. 17 зображено приклади взаємодії перемичок між α-спіралями (а) чи витягнутого поліпептидного ланцюга (б) з маленьким жолобком. У першому випадку − димер гістонів у складі нуклеосоми − маємо ще один структурний мотив, який зустрічається і в інших ДНК-зв’язувальних білках, а саме гістонову укладку: одна довга α-спіраль фланкована двома короткими. Димер двох таких укладок взаємодіє з ~2,5 витками подвійної спіралі. У випадку гістонів ця взаємодія не є специфічною: утворюються електростатичні контакти позитивно заряджених амінокислотних залишків з фосфатами ДНК, але з боку маленького жолобка.
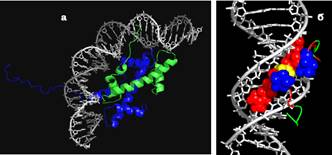
Рис. 17. Димер гістонів Н3Н4 (а, 1AOI) і АТ-гак у складі білка HMGA (б, 2EZD).
Другий приклад (рис 17, б) стосується білків HMGA – білків групи високої рухливості (High Mobility Group) типу А (HMG − історична назва для білків різних структурних класів, мається на увазі рухливість при електрофорезі). Білки HMGA взагалі не мають глобулярної структури − є невпорядкованими. Вони містять 3 пентапептидні елементи (Pro-Arg-Gly-Arg-Pro), що називаються АТ-гаками (АТhook). Такий гак добре укладається у звужений маленький жолобок невеликої ділянки подвійної спіралі, збагаченої АТ-парами (тобто АТ-гак має специфічність до невеликих АТ-збагачених сайтів, завдяки чому він і отримав свою назву).
Наступні приклади стосуються дуже важливих випадків взаємодії елементів регулярної вторинної структури білків з маленьким жолобком. Оскільки α-спіраль і дволанцюговий β-шар добре укладаються у великий жолобок, це автоматично означає, що в маленькому жолобку їм не вистачає місця. Відповідно, така взаємодія буде можливою тільки за умови суттєвої деформації подвійної спіралі ДНК (розширення жолобка) − ефект, що має важливі функціональні наслідки.
На рис. 18 зображено досить розповсюджений мотив – HMG-бокс, який, зокрема, входить до складу білків HMGВ (ще один клас білків HMG). Мотив складається з трьох α-спіралей, дві з них (позначені червоним) вбудовуються (інтеркалюють) у маленький жолобок. Це супроводжується розкрученням подвійної спіралі й вигином на ~80° у протилежний щодо білка бік. Серед HMG-боксів є як специфічні до певних послідовностей пар основ, так і неспецифічні.
У складі білка ТВР (TATA-box Binding Protein) − важливого елемента ініціації транскрипції в еукаріотів − досить широкий β-шар взаємодіє з маленьким жолобком подвійної спіралі в зоні ТАТА-боксу − регуляторного елемента послідовності ДНК. Наслідком цієї взаємодії також є значна деформація подвійної спіралі з її розкрученням і значним вигином у протилежний від білка бік (рис. 19).
Вигин, як і у випадку HMG-боксу, підсилюється інтеркаляцією двох гідрофобних амінокислотних залишків між парами основ. У місці інтеркаляції порушуються стекінг-взаємодії та утворюється кінк (kink) − різкий злам подвійної спіралі.
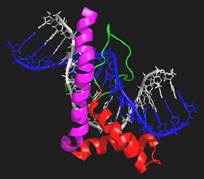
Рис. 18. HMG-бокс у складі білка HMGВ (1J5N).
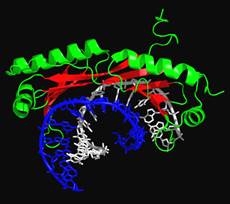
Рис. 19. ДНК-зв’язувальний домен ТВР у комплексі з ТАТА-боксом (1QNE).
На відміну від розглянутих факторів транскрипції та структурних білків, ферменти, які працюють на ДНК, досить важко описати в термінах простих структурних мотивів. Ферменти використовують складні комбінації різноманітних елементів білкової структури для впізнання ДНК і зв’язування з нею. Два приклади – мономерна ДНК-аза І (неспецифічна ендонуклеаза, яка здійснює одноланцюговий розріз в ділянці маленького жолобка) і гомодимерна рестриктаза EcoRV − зображені на рис. 20.
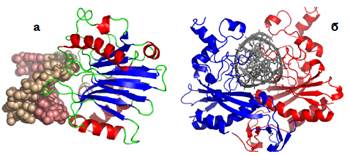
Рис. 20. Комплекси з ДНК ДНК-ази І (а, 1DNK) і рестриктази EcoRV (б, 1AZ0).
Дата добавления: 2018-05-10; просмотров: 1307;











