Атомно-кристаллическое строение (АКС) - это строго определенное закономерное расположение атомов в пространстве.
АТОМНО-КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ И СПЛАВОВ
Общее свойство металлов и сплавов - их кристаллическое строение, характеризующееся закономерным расположением атомов в пространстве.
Атомно-кристаллическое строение (АКС) - это строго определенное закономерное расположение атомов в пространстве.
Для количественногоописания и оценки АКС вводится понятие кристаллической решетки - воображаемой пространственной сетки, в узлах которой находятся атомы. Атомно-кристаллическая структура может быть представлена изображением одной элементарной ячейки, повторяющейся во всех трех измерениях.
Элементарная ячейка- наименьший объем, трансляцией которого можно полностью воспроизвести структуру кристалла (рис.1.1).
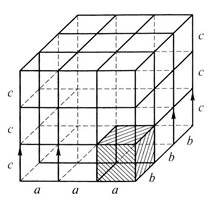 Рис.1.1
Рис.1.1
В кристалле атомы сближены до соприкосновения. Для упрощения пространственное изображение АКС и кристаллических решеток принято заменять схемами, где центры тяжести частиц представлены точками. В точках пересечения прямых линий располагаются атомы; они называются узлами решетки (рис.1.2).
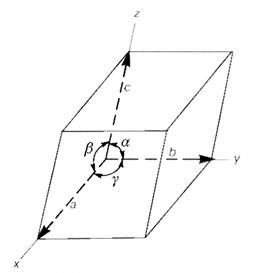
Рис.1.2
Расстояния между центрами ближайших атомов (a, b, c ) называются параметрами (периодами) решетки.
Величина периодов в металлах порядка 0,1…7 нм. Размеры элементарных ячеек 0,2…0,3 нм.
Для кубической кристаллической решетки а=b=с.
Координационное число — количество атомов, находящихся на одинаковом и наименьшем расстоянии от данного.
Период решетки характеризует ее размеры, координационное число - характеризует плотность упаковки элементарной ячейки.
Углы между гранями кристаллической решетки (α, β, γ) характеризуют тип кристаллической решетки.
Для кубической решетки α=β=γ= 90о.
Плоскость, проходящая через узлы кристаллической решетки, называется кристаллографической плоскостью.
Прямая, проходящая через узлы кристаллической решетки, называется кристаллографическим направлением.
Типы кристаллических решеток.
Существует 14 типов кристаллических решеток (решетки Бравэ). Рассмотрим 3 из них, которые наиболее часто встречаются у основной группы металлов и наиболее распространены в природе:
1. Объемоцентрированная кубическаярешетка (ОЦК).
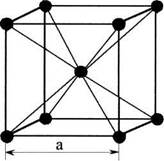 Рис.1.3
Рис.1.3
В кристаллической решетке ОЦК (рис.1.3) атомы расположены в вершинах элементарной ячейки и в центре куба. Такая ячейка содержит 9 атомов.
Кубическую объемоцентрированную решетку имеют хром, вольфрам, железо, ванадий, молибден и другие металлы.
2. Гранецентрированная кубическая решетка (ГЦК)
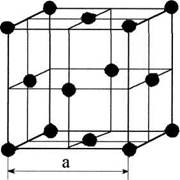 Рис.1.4
Рис.1.4
В ячейке кубической гранецентрированной решетки (рис.1.4) атомы находятся в вершинах куба и на пересечении диагоналей каждой плоскости. Такая ячейка имеет 14 атомов.
Решетку ГЦК имеют свинец, никель, медь, железо, серебро и другие металлы.
| <== предыдущая лекция | | | следующая лекция ==> |
| Переход от геоцентрических в промежуточные координаты | | |
Дата добавления: 2018-05-10; просмотров: 1952;











