Газообразное состояние вещества
Полимеры бывают естественного (растительные и животные ткани) и искусственного (пластмассы, целлюлоза, стекловолокно и др.) происхождения.
Так же, как и в случае обычных молекул, система макромолекул. образующих полимер, стремится к наиболее вероятному состоянию - устойчивому равновесию, соответствующему минимуму свободной энергии. Следовательно, в принципе полимеры также должны иметь структуру в виде кристаллической решетки. Однако ввиду громоздкости и сложности макромолекул лишь в немногих случаях удалось получить совершенные макро- молекулярные кристаллы. В большинстве случаев полимеры состоят из кристаллических и аморфных областей.
Жидкое состояние характерно тем, что потенциальная энергия притяжения молекул несколько превосходит по абсолютному значению их кинетическую энергию. Силы притяжения между молекулами в жидкости обеспечивает удержание молекул в объеме жидкости. Вместе с тем молекулы в жидкости не связаны между собой стационарными устойчивыми связями, как в кристаллах. Они плотно заполняют занимаемое жидкостью пространство, поэтому жидкости практически несжимаемы и обладают достаточно высокой плотностью. Группы молекул могут изменять свое взаимное положение, что обеспечивает текучесть жидкостей. Свойство жидкости сопротивляться течению называется вязкостью. Жидкостям свойственна диффузия и броуновское движение, однако в значительно меньшей степени, чем газам.
Объем, занимаемый жидкостью, ограничен поверхностью. Так как при заданном объеме минимальной поверхностью обладает шар, то жидкость в свободном состоянии (например, в невесомости) принимает форму шара.
Жидкости обладают некоторой структурой, которая, однако, выражена гораздо слабее, чем у твердых тел. Важнейшим свойством жидкостей является изотропия свойств. Простая идеальная модель жидкости пока не создана.
Существует промежуточное состояние между жидкостями и кристаллами, которое называется жидкокристаллическим. Особенностью жидких кристаллов с молекулярной точки зрения является вытянутая, веретенообразная форма их молекул, что приводит к анизотропии их свойств.
Выделяют два типа жидких кристаллов - нематики и смектики. Смектики характерны наличием параллельных слоев молекул, отличающихся друг от друга упорядоченностью структуры. У нематиков упорядоченность обеспечивается ориентацией молекул. Анизотропия свойств жидких кристаллов обусловливает их важные оптические свойства. Жидкие кристаллы могут, например, быть прозрачными в одном направлении и непрозрачными в другом. Важно, что ориентацией молекул жидких кристаллов и их слоев легко можно управлять с помощью внешних воздействий (например, температуры, электрических и магнитных полей).
Газообразное состояние вещества возникает в том случае, когда
кинетическая энергия теплового движения молекул превосходит потенциальную энергию их связи. Молекулы при этом стремятся удалиться друг от друга. Газ не имеет структуры, занимает весь предоставленный ему объем, легко сжимаем; в газах легко происходит диффузия.
Свойства веществ, находящихся в газообразном состоянии, объясняет кинетическая газовая теория. Основные ее постулаты состоят в следующем:
- все газы состоят из молекул;
- размеры молекул пренебрежимо малы по сравнению с расстояниями между ними;
- молекулы постоянно находятся в состоянии хаотического (броуновского) движения;
- между столкновениями молекулы сохраняют постоянную скорость движения; траектории между столкновениями - отрезки прямых линий;
- столкновение между молекулами и молекул со стенками сосуда являются идеально упругими, т.е. полная кинетическая энергия соударяющихся молекул остается неизменной.
Рассмотрим упрощенную модель газа, подчиняющегося приведенным постулатам. Такой газ называется идеальным газом. Пусть идеальный газ в количестве N одинаковых молекул, каждая из которых имеет массу m, находится в сосуде кубической формы с длиной ребра l (рис. 5.14). Молекулы движутся хаотически; средняя скорость их движения <v>. Для упрощения разобьем все молекулы на три равные группы и предположим, что они движутся только в направлениях, перпендикулярных двум противоположным стенкам сосуда (рис. 5.15).
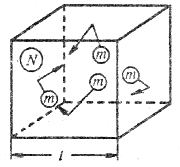 |
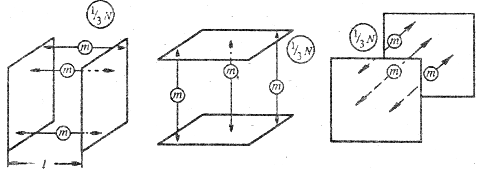 Рис. 5.14.
Рис. 5.14.
Рис. 5.15.
Каждая из молекул газа, движущаяся со скоростью <v> при абсолютно упругом соударении со стенкой сосуда, изменит направление движения на обратное, не изменив скорость. Импульс молекулы <р> = m<v> становится равным при этом - m<v>. Изменение импульса в каждом столкновении, очевидно, равно 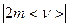 . Сила, действующая во время этого столкновения, равна F= -2m<v>/Δt. Полное изменение импульса при столкновении со стенками всех N/3молекул равно
. Сила, действующая во время этого столкновения, равна F= -2m<v>/Δt. Полное изменение импульса при столкновении со стенками всех N/3молекул равно 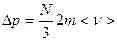 . Определим интервал времени Δt, в течение которого произойдут все N/3 столкновения: Д t = 2//< v >. Тогда среднее значение силы, действующей на любую стенку,
. Определим интервал времени Δt, в течение которого произойдут все N/3 столкновения: Д t = 2//< v >. Тогда среднее значение силы, действующей на любую стенку,
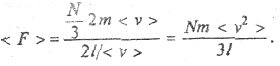
Давление р газа на стенку определим как отношение силы <F> к площади стенки l2:
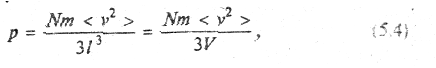
где V = l3 – объем сосуда.
Таким образом, давление газа обратно пропорционально его объему (напомним, что эмпирически этот закон установили Бойль и Мариотт).
Перепишем выражение (5.4) в виде

Здесь 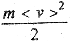 - средняя кинетическая энергия молекул газа. она пропорциональна абсолютной температуре Т:
- средняя кинетическая энергия молекул газа. она пропорциональна абсолютной температуре Т:

где k – постоянная Больцмана.
Подставив (5.6) в (5.5), получим
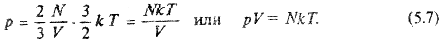
Удобно перейти от числа молекул N к числу молей n газа, напомним, что 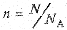 (NА – число Авогадро), и тогда
(NА – число Авогадро), и тогда

где R = kNA - - универсальная газовая постоянная.
Выражение (5.8) есть уравнение состояния классического идеального газа для п молей. Данное уравнение, записанное для произвольной массы m газа

где М - молярная масса газа, называется уравнением Клапейрона-Менделеева (см. (5.3)).
Реальные газы подчиняются этому уравнению в ограниченных пределах. Дело в том, что уравнения (5.8) и (5.9) не учитывают межмолекулярное взаимодействие в реальных газах - силы Ван- дер-Ваальса.
Фазовые переходы. Вещество, в зависимости от условий, в которых оно находится, может изменять агрегатное состояние, или, как говорят, переходить из одной фазы в другую. Такой переход называется фазовым переходом.
Как указывалось выше, важнейшим фактором, определяющим состояние вещества, является его температура Т, характеризующая среднюю кинетическую энергию теплового движения молекул и давление р. Поэтому, состояния вещества и фазовые переходы анализируют по диаграмме состояний, где по осям откладываются значения Т и р, а каждая точка на координатной плоскости определяет соответствующее этим параметрам состояние данного вещества. Проанализируем типичную диаграмму (рис. 5.16). Кривые ОА, АВ, АК разделяют состояния вещества. При достаточно низких температурах практически все вещества находятся в твердом кристаллическом состоянии.
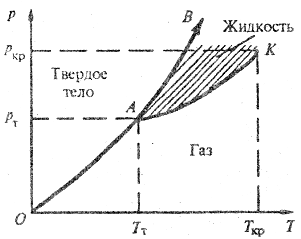 |
Рис. 5.16.
На диаграмме выделены две характерные точки: А и К. Точка А называется тройной точкой; при соответствующих температуре (Тт) и давлении (Рт) в ней находится в равновесии одновременно газ, жидкость и твердое тело.
Точка К обозначает критическое состояние. В этой точке (при Ткр и Ркр) исчезает разница между жидкостью и газом, т.е. последние имеют одинаковые физические свойства.
Кривая ОА является кривой сублимации (возгонки); при соответствующих давлении и температуре осуществляется переход газ - твердое тело (твердое тело - газ), минуя жидкое состояние.
При давлении Рт < Р < Ркр переход из газообразного в твердое состояние (и наоборот) может осуществляться только через жидкую фазу.
Кривая АК соответствует испарению (конденсации). При соответствующих давлении и температуре осуществляется переход «жидкость – газ» (и обратно).
Кривая АВ является кривой перехода «жидкость - твердое тело» (плавления и кристаллизации). Данная кривая не имеет конца, так как всегда жидкое состояние отличается от кристаллического по структуре.
Приведем для иллюстрации форму поверхностей состояний вещества в переменных р, V, Т (рис. 5.17), где V - объем вещества
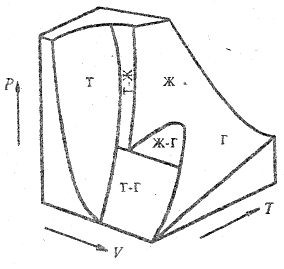 |
Рис. 5.17.
Буквами Г, Ж, Т обозначены участки поверхностей, точки которых, соответствуют газообразному, жидкому или твердому состояниям, а участки поверхностей Т-Г, Ж-Т, Т-Ж - двухфазным состояниям. Очевидно, если спроецировать линии раздела между фазами на координатную плоскость РТ, получим фазовую диаграмму (см. рис. 5.16).
Квантовая жидкость - гелий. При обычных температурах в макроскопических телах из-за выраженного хаотического теплового движения квантовые эффекты неощутимы. Однако с уменьшением температуры эти эффекты могут выходить на первый план и проявляются макроскопически. Так, например, кристаллы характерны наличием тепловых колебаний ионов, находящихся в узлах кристаллической решетки. С уменьшением температуры амплитуда колебаний уменьшается, однако даже при приближении к абсолютному нулю колебания, вопреки классическим представлениям, не прекращаются.
Объяснение этого эффекта следует из соотношения неопределенностей. Уменьшение амплитуды колебаний означает уменьшение области локализации частицы, т. е. неопределенности ее координат. В соответствии с соотношением неопределенностей это приводит к увеличению неопределенности импульса. Таким образом, «остановка» частицы запрещена законами квантовой механики.
Этот сугубо квантовый эффект проявляется в существовании вещества, остающегося в жидком состоянии даже при температурах, близких к абсолютному нулю. Такой «квантовой» жидкостью является гелий. Энергии нулевых колебаний оказывается достаточно, чтобы разрушить кристаллическую решетку. Однако при давлении порядка 2,5 МПа жидкий гелий все-таки кристаллизуется.
Плазма. Сообщение атомам (молекулам) газа извне значительной энергии приводит к ионизации, т. е. распаду атомов на ионы и на свободные электроны. Такое состояние вещества называется плазмой.
Ионизация возникает, например, при сильном нагреве газа, что приводит к значительному увеличению кинетической энергии атомов, при электрическом разряде в газе (ударная ионизация заряженными частицами), при воздействии на газ электромагнитного излучения (автоионизация). Плазма, получаемая при сверхвысоких температурах, называется высокотемпературной.
Поскольку ионы и электроны в плазме несут некомпенсированные электрические заряды, их взаимное влияние существенно. Между заряженными частицами плазмы существует не парное (как в газе), а коллективное взаимодействие. Благодаря этому плазма ведет себя как своеобразная упругая среда, в которой легко возбуждаются и распространяются различные колебания и волны
Плазма активно взаимодействует с электрическими и магнитными полями. Плазма - наиболее распространенное состояние вещества во Вселенной. Звезды состоят из высокотемпературной плазмы, холодные туманности - из низкотемпературной. Слабо ионизированная низкотемпературная плазма имеется в ионосфере Земли.
Литература к главе 5
1. Ахиезер А. И., Рекало Я. П. Элементарные частицы. - М.: Наука, 1986.
2. Азшлов А. Мир углерода. - М.: Химия, 1978.
3. Бронштейн М. П. Атомы и электроны. - М.: Наука, 1980.
4. Бениловский В. Д. Эти удивительные жидкие кристаллы. - М: Просвещение, 1987.
5. Власов Н. А. Антивещество. - М.: Атомиздат, 1966.
6. Кристи Р., Питти А. Строение вещества: введение в современную физику. — М.: Наука, 1969.
7. Крейчи В. Мир глазами современной физики. - М.: Мкр, 1984.
8. Намбу Е. Кварки. - М.: Мир, 1984.
9. Окунь Л. Б. α, β, γ, …,: элементарное введение в физику элементарных частиц. - М.: Наука, 1985.
10. Петров Ю. И. Физика малых частиц. - М.: Наука, 1982.
11. И, Пурмалъ А. П. и др. Как превращаются вещества. - М.: Наука, 1984.
12. Розенталь И. М. Элементарные частицы и структура вселенной. — М.: Наука, 1984.
13. Смородинский Я. А. Элементарные частицы. - М.: Знание, 1968.
| <== предыдущая лекция | | | следующая лекция ==> |
| Уравнений классической электродинамики (уравнения Максвелла) | | | Распространение электромагнитного поля в вакууме. Электромагнитные волны |
Дата добавления: 2017-11-21; просмотров: 4414;











