Стереохимия аминокислот
Получаемые из белков аминокислоты, за исключением глицина, оптически активны, так как они содержат асимметрический атом углерода. Это α-углерод в цепи аминокислоты. Поэтому, аминокислоты существуют в двух пространственных конфигурациях (D и L), являющихся зеркальными изомерами (рис. 5-1).
|
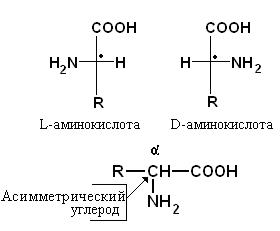
2 изомера аминокислоты аланин:
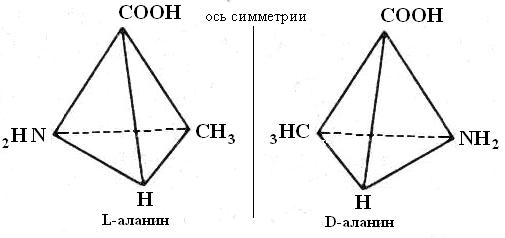
Рис. 5-1. Стереоизомерия аминокислот на примере аланина
Ι. Аминокислоты с гидрофобным радикалом
(содержат группы –СН2–, –СН3, ароматические кольца)
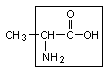
1. Аланин – ала
|
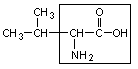
2. Валин – вал
|
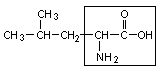
3. Лейцин – лей
|
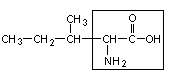
4. Изолейцин – иле
|
5. Метионин – мет
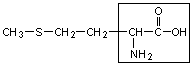
|
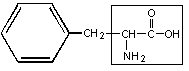
6. Фенилаланин – фен
|
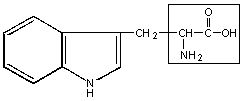
7. Триптофан – три
|
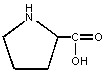
8. Пролин – про
|
ΙΙ. Аминокислоты с гидрофильным не заряженным радикалом
(содержат группы –ОН, –SН, амидную)
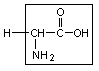
1. Глицин – гли
|
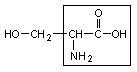
2. Серин – сер
|
3. Треонин – тре
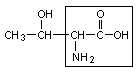
|
4. Цистеин – цис
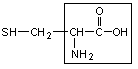
|
5. Тирозин – тир
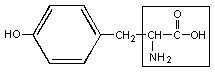
|
6. Аспарагин – асн
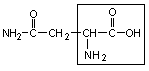
|
7. Глутамин – глн
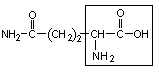
|
ΙΙΙ. Аминокислоты с гидрофильным, заряженным отрицательно, радикалом
1. Аспарагиновая кислота – асп
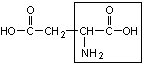
|
2. Глутаминовая кислота – глу
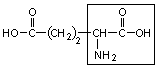
|
Рис. 5-2. Классификация аминокислот
ΙV. Аминокислоты с гидрофильным, заряженным положительно, радикалом
1. Лизин – лиз
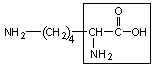
|
2. Аргинин – арг
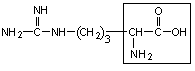
|
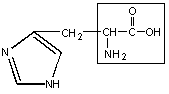
3 Гистидин – гис
|
Дата добавления: 2021-10-28; просмотров: 613;











