Принципы лечения ожогового шока
Терапия ожогового шока строится на следующих принципах.
• Коррекция гиповолемии, гипопротеинемии и дисэлектролитемии.
• Уменьшение сосудистой проницаемости.
• Ограничение избыточной активации синдрома системного воспалительного ответа и протекция функции органов.
• Антибактериальная терапия.
• Анальгезия.
На догоспитальном этапепри отсутствии возможности проведения инфузионной терапии и при сохраненном сознании пациенту дают пить солевые растворы, проводят анальгезию и накладывают на ожоговые поверхности стерильные повязки, обильно смоченные фурациллином.
На госпитальном этапепоследовательность лечебных мероприятий должна быть следующей.
• Восстановление проходимости верхних дыхательных путей, оксигенотерапия, решение вопроса об интубации трахеи и проведении ИВЛ у пациентов с ожогом верхних дыхательных путей, у пациентов, которым на месте проводились реанимационные мероприятия, при глубоком ожоге площадью более 60-80% с целью уменьшения потребления и увеличения доставки тканям кислорода, а также при тяжелом отравлении угарным газом.
• Анальгезия ненаркотическими или наркотическими анальгетиками.
• Болюсная инфузия 20 мл/кг раствора Рингера или 0,9% раствора хлористого натрия. Учитывая тот факт, что продолжительность ожогового шока может составлять сутки и более, дальнейшая инфузионная терапия должна быть направлена на восполнение физиологической потребности и продолжающейся потери жидкости. Качественный состав инфузионной терапии определяется патогенезом ожогового шока - плазмопотерей с ожоговой поверхности на фоне выраженного катаболизма и выведения из организма калия, что требует восполнение теряемой воды, натрия, калия и белка. Следовательно, основу инфузионной терапии ожогового шока должны составлять глюкозосолевые и белковые препараты. Необходимо помнить о том, что вследствие выраженного синдрома капиллярной утечки в первые 8 ч идет интенсивная потеря альбумина в ожоговую рану, поэтому не рекомендуется использовать белковые препараты в первые 6-8 ч терапии ожогового шока. В объем инфузионной терапии могут быть включены коллоиды, однако на фоне выраженного синдрома капиллярной утечки нельзя исключить вероятность их выхода в интерстициальный сектор с развитием клиники отека бронхов, легких и головного мозга. В стадии инфицирования ожоговой раны всегда имеет место перегрузка ретикулоэндотелиальной системы (РЭС) неконтролируемо накапливающимися микроорганизмами. Поэтому дополнительная нагрузка на РЭС в виде декстранов может привести к быстрой декомпенсации ее функции. По мере восстановления диуреза в инфузионную терапию включают раствор калия хлорида - 30-40 ммоль/л. Нормализация содержания калия в крови имеет значение в плане профилактики развития пареза кишечника и синдрома транслокации кишечной микрофлоры, что лежит в патогенезе развития сепсиса.
• Устанавливают назогастральный зонд, опорожняют желудок и вводят антациды 30 мл/м2через каждые 1-2 ч. В настоящее время придерживаются тактики раннего начала энтерального введения жидкости и кормления, так как это предотвращает образование стрессовых язв и транслокацию кишечной микрофлоры.
• С целью уменьшения сосудистой проницаемости используют этамзилат натрия в дозе 0,1 мл/кг/сут, преднизолон, который при ожоге более 30% поверхности тела назначают в дозе 3 мг/кг/сут на 3 дня, а при ожоге более 50% - 5 мг/кг/сут на 5 дней. Аскорбиновую кислоту назначают в дозе 1 г/м2 ожоговой поверхности в сутки.
• Профилактика столбняка осуществляется у иммунизированных пациентов, получивших последнюю дозу более 5 лет назад, введением 0,5 мл столбнячного анатоксина, а у неиммунизированных пациентов - введением противостолбнячного человеческого иммуноглобулина в дозе 250-500 тыс. Ед в/м.
• Антибактериальную терапию препаратами широкого спектра назначают с целью санации хронических очагов инфекции и подавления транслоцированной микрофлоры. В первые сутки ожоговой болезни проницаемость антибиотиков в ожоговую рану значительно снижена, в связи с чем для профилактики и лечения раневой инфекции нужно использовать местные антибактериальные препараты.
• С самого начала терапии необходим строгий контроль диуреза.
• С целью улучшения перфузии тканей, особенно подлежащих к ожоговой поверхности, и доставки кислорода, а также с целью улучшения почечного, мезентериального, легочного кровотока в стадию ожогового шока показано использование трентала в дозе 5-10 мг/кг, который одновременно уменьшает выработку фактора некроза опухоли - одного из пусковых медиаторов синдрома системного воспалительного ответа.
СЕПТИЧЕСКИЙ ШОК
Септический шок является одним из самых тяжелых видов шоков. Летальность при нем составляет от 50 до 75%. По своему патогенезу септический шок является одновременно сосудистым, кардиогенным и гиповолемическим. В основе его развития лежит накопление провоспалительных медиаторов, вызывающих повреждение эндотелия, активацию ДВС-синдрома, выраженные нарушения микроциркуляции с генерализованным спазмом одних зон и паралитической вазодилатацией других, в том числе вследствие накопления в тканях оксида азота (NO). Накопление эндотоксинов микроорганизмов и выраженный метаболический ацидоз препятствуют взаимодействию катехоламинов с сосудистыми рецепторами, вызывают депрессию миокарда, активизируют катаболизм и приводят к значительному повышению потребности тканей в кислороде, которая не может быть обеспечена в результате снижения его доставки. Выраженный синдром капиллярной утечки, вызванный действием медиаторов воспаления на сосудистый эндотелий, обусловливает за счет пропотевания жидкой части крови в интерстиций формирование тяжелой и быстро прогрессирующей гиповолемии.
Для септического шока клинически характерно наличие двух стадий. В стадию теплого шокаимеет место гипердинамия кровообращения за счет активации работы сердца и раскрытия артериовенозных шунтов (рис. 18-8). Так, если в нормальных условиях через A-Vшунт проходит около 5% органного кровотока, то при септическом шоке эта величина неуклонно возрастает, что способствует формированию кислородного дефицита в системе капилляров. Усиленный сброс артериальной крови через A-Vшунт вызывает формирование весьма нехарактерного для шоковых состояний признака: кожные покровы становятся теплыми, иногда даже горячими на ощупь. Отмечается гиперемия кожи, гипертермия, тахикардия, ранним признаком септического шока может быть повышенное выделение гипотоничной мочи. Кроме этого, бактериальные токсины нарушают усвоение кислорода посредственно в клетках. В ответ организм реагирует увеличением МОС посредством повышения УО и ЧСС с одновременным снижением ПСС. Эту стадию теплого шока иногда обозначают как гипердинамическую фазу(Э.К. Айламазян, 1995).
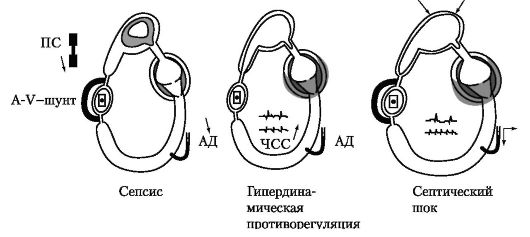
Рис. 18-8. Патогенез септического шока
На пике развития септического шока (стадия теплого шока, гипердинамическая фаза)основные показатели центральной гемодинамики будут следующие: АД, УО, ЦВД, ДН в пределах верхней границы нормы или незначительно увеличены, умеренная тахикардия, сниженное ПСС. По мере нарастания интоксикации УО приходит к нормальным величинам, а затем начинает прогрессивно уменьшаться, что способствует переходу шока в стадию холодного шока, гиподинамическую фазу (Э.К. Айламазян, 1995). В ее основе лежит переход к гиподинамическому типу кровообращения и развитие синдрома малого выброса вследствие прогрессирующего ухудшения контрактильности миокарда и падения общего периферического сопротивления. Больной становится вялым, безучастным к окружающим, кожа приобретает серый, с выраженным нарушением микроциркуляции в виде мраморности, резко положительного симптома бледного пятна, отмечается прогрессирующая гипотония, тахикардия, олигоанурия, быстро нарастает синдром острого повреждения легких. Летальность в холодную стадию шока приближается к 80-90%.
Данный вариант патологии наиболее часто встречается в акушерско-гинекологической практике у молодых женщин и протекает крайне бурно - летальный исход может наступить буквально через несколько часов. Ключевыми звеньями в патогенезе септического шока являются высокий СВ, низкие ДЗЛК и ОПСС, что вызывает неадекватную оксигенацию тканей.
Дата добавления: 2016-06-05; просмотров: 3543;











