Дефекты кристаллической решетки
В любом реальном кристалле всегда имеются дефекты строения. Дефекты кристаллического строения подразделяют на точечные (нульмерные), линейные (одномерные), поверхностные (двумерные), объемные (трехмерные).
 Точечными дефектами называются такие нарушения периодичности кристаллической решетки, размеры которых во всех измерениях сопоставимы с размерами атома.
Точечными дефектами называются такие нарушения периодичности кристаллической решетки, размеры которых во всех измерениях сопоставимы с размерами атома.
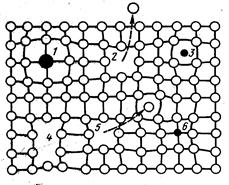
Рис.7. Схема точечных дефектов в кристалле: 1-примесный атом замещения, 2- дефект Шоттки, 3- примесный атом внедрения, 4- дивакансия, 5- дефект Френкеля (вакансия и межузельный атом), 6- примесный атом замещения.
К точечным дефектам относят вакансии (узлы в кристаллической решетке, свободные от атомов), или дефект Шотки, межузельные атомы (атомы, находящиеся вне узлов кристаллической решетки), а также примесные атомы, которые могут или замещать атомы основного металла (примеси замещения) или внедряться в свободные места решетки (поры, межузлия) аналогично межузельным атомам (примеси внедрения) (рис.7).
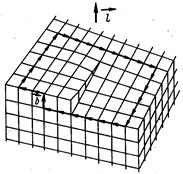
Линейные дефекты в кристаллах характеризуются тем, что их поперечные размеры не превышают нескольких межатомных расстояний, а длина может достигать размера кристалла. К линейным дефектам относятся дислокации – линии, вдоль и вблизи которых нарушено правильное периодическое расположение атомных плоскостей кристалла. Различают краевую и винтовую дислокации (рис.8). Краевая дислокация представляет собой границу неполной атомной плоскости (экстраплоскости). Винтовую дислокацию можно определить как сдвиг одной части кристалла относительно другой.
Поверхностные дефекты малы только в одном измерении. Они представляют собой поверхности раздела между отдельными зернами или субзернами в поликристаллическом материале, а также дефекты упаковки (локальные изменения расположения плотноупакованных плоскостей в кристалле).
К объемным дефектам относят такие, которые имеют размеры в трех измерениях: макроскопические трещины, поры и т.д.
 Наличие различных дефектов кристаллической решетки объясняет несоответствие реальной и теоретической прочности металлических материалов. Реальная прочность металлов падает с увеличением числа дислокаций.
Наличие различных дефектов кристаллической решетки объясняет несоответствие реальной и теоретической прочности металлических материалов. Реальная прочность металлов падает с увеличением числа дислокаций.
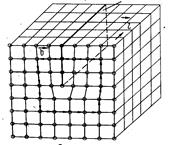
а б
Рис.8.Дислокации: а) краевая, б) винтовая
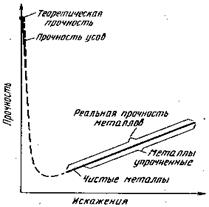 Достигнув минимального значения при некоторой плотности дислокаций, реальная прочность возрастает. Такого рода зависимость между реальной прочностью и плотностью дислокаций (и других несовершенств) схематически показана на рис.9.
Достигнув минимального значения при некоторой плотности дислокаций, реальная прочность возрастает. Такого рода зависимость между реальной прочностью и плотностью дислокаций (и других несовершенств) схематически показана на рис.9.
Рис.9. Прочность кристаллов в зависимости от искажений решетки
Повышение реальной прочности с возрастанием плотности дислокаций объясняется тем, что при этом возрастают не только параллельные друг другу дислокации, но и дислокации в разных плоскостях и направлениях. Такие дислокации будут мешать друг другу перемещаться, а реальная прочность металла повысится.
Резюме
Все металлы и металлические сплавы – тела кристаллические, атомы (ионы) расположены в металлах закономерно в отличие от аморфных тел.
Металлы представляют собой поликристаллические тела, состоящие из большого числа мелких, различно ориентированных по отношению друг к другу кристаллов. В процессе кристаллизации они приобретают неправильную форму и называются кристаллитами, или зернами.
Между ионами и коллективизированными электронами проводимости возникают электростатические силы притяжения, которые связывают ионы. Такая связь называется металлической.
В металле атомы располагаются закономерно, образуя правильную кристаллическую решетку, что соответствует минимальной энергии взаимодействия атомов.
Наименьший объем кристалла, дающий представление об атомной структуре металла в любом объеме, получил название элементарной кристаллической ячейки.
Для однозначной ее характеристики используются величины: три ребра (a, b, c) и три угла между осями α, β, γ.
Большинство металлов образует одну из следующих высокосимметричных решеток с плотной упаковкой атомов: кубическую объемно центрированную (ОЦК), кубическую гранецентрированную (ГЦК) и гексагональную плотноупакованную (ГПУ).
Расстояния a, b, c между центрами ближайших атомов в элементарной ячейке называются периодами решетки.
Для определения положения атомных плоскостей (проходящих через атомы) в кристаллических пространственных решетках пользуются индексами h, k, l. Для определения атомных направлений пользуются индексами направлений [uvw].
Неодинаковость свойств монокристалла в разных кристаллографических направлениях называется анизотропией.

 Дефекты кристаллического строения
Дефекты кристаллического строения
 |  |
| точечные | линейные | поверхностные | объемные |
| -вакансии -межузельные атомы -примесные атомы (примеси замещения, примеси внедрения) | -дислокации (краевая, винтовая) |  -поверхности раздела между зернами
-дефекты упаковки -поверхности раздела между зернами
-дефекты упаковки
| -макротрещины -поры |
Наличие различных дефектов кристаллической решетки объясняет несоответствие реальной и теоретической прочности металлических материалов.
Вопросы для повторения
1. Объяснить строение твердых тел. Чем отличаются кристаллические и аморфные тела?
2. В чем отличие кристаллов и кристаллитов (зерен)?
3. Какая связь называется металлической?
4. Что собой представляет кристаллическая решетка? Каковы ее характеристики? Какие типы кристаллических решеток Вы знаете?
5. Дать определение кристаллографическим плоскостям и направлениям?
6. Что такое анизотропия, и как она влияет на свойства материала?
7. Какие дефекты кристаллической решетки Вы знаете?
8. Чем вызвано несоответствие реальной и теоретической прочности металлических материалов?
КРИСТАЛЛИЗАЦИЯ
Кристаллизацией называется переход металла из жидкого состояния в твердое (кристаллическое). Кристаллизация протекает в условиях, когда система переходит к термодинамически более устой-
чивому состоянию с меньшей энергией Гиббса (свободной энергией) G, т.е. когда энергия Гиббса кристалла меньше, чем энергия Гиббса жидкой фазы (рис.10). Если превращение происходит с небольшим изменением объема, то G=U-TS, где U – внутренняя энергия системы, T – абсолютная температура, S – энтропия.
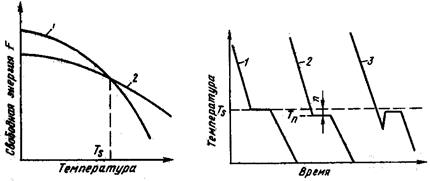
Рис.10 Изменение свободной энергии жидкого (1) и кристаллического (2) состояния в зависимости от температуры
Рис.11. Кривые охлаждения при кристаллизации: теоретический (1) и реальный (2) процессы кристаллизации, (3) – процесс кристаллизации со скачкообразным повышением температуры кристаллизации
Выше температуры Тs меньшей свободной энергией обладает вещество в жидком состоянии, ниже этой температуры – вещество в твердом состоянии. Тs – есть равновесная (теоретическая) температура кристаллизации, при которой металл в обоих состояниях находится в равновесии. Для начала кристаллизации необходимо, чтобы процесс был термодинамически выгоден системе и сопровождался уменьшением свободной энергии системы. Это возможно при некотором переохлаждении жидкости. Температура, при которой практически начинается кристаллизация, называется фактической температурой кристаллизации. Разность между теоретической и фактической температурой кристаллизации есть величина или степень переохлаждения.
Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах температура – время (рис.11). Охлаждение металла в жидком состоянии сопровождается плавным понижением температуры и может быть названо простым
охлаждением, так как при этом нет качественного изменения состояния. При достижении температуры кристаллизации на кривой температура – время появляется горизонтальная площадка, связанная с выделением скрытой теплоты кристаллизации. По окончании кристаллизации, т.е. полного перехода в твердое состояние, температура снова начинает снижаться, а твердое кристаллическое вещество охлаждается. Теоретически процесс кристаллизации изображен кривой 1. Кривая 2 показывает реальный процесс кристаллизации с переохлаждением. Кривая 3 иллюстрирует процесс кристаллизации для некоторых металлов, когда из-за большого переохлаждения скрытая теплота выделяется в первый момент настолько бурно, что температура кристаллизации скачкообразно повышается.
Процесс кристаллизации состоит из двух элементарных процессов: возникновение зародышей, или центров кристаллизации и рост кристаллов из этих центров. Схематически процесс зарождения и роста кристаллов показан на рис.12. По мере развития процесса кристаллизации в нем участвует все большее число кристаллов. Поэтому процесс вначале ускоряется, а затем, когда взаимное столкновение растущих кристаллов начинает препятствовать их росту, замедляется. Кроме того, при столкновении и срастании кристаллов их правильная форма нарушается. Поэтому реальные зерна имеют неправильную форму.
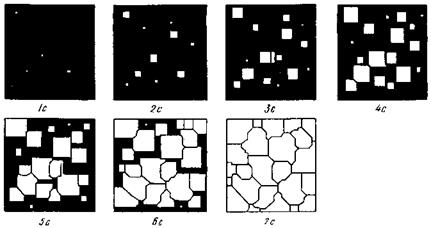
Рис.12. Модель процесса кристаллизации. Под рисунком указано время течения процесса в секундах
 Процесс кристаллизации, как уже было сказано выше, может протекать только при условии уменьшения свободной энергии.
Процесс кристаллизации, как уже было сказано выше, может протекать только при условии уменьшения свободной энергии.
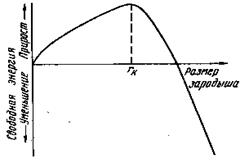
Рис.13. Изменение свободной энергии в зависимости от размера зародыша, rк – критический размер зародыша
Поэтому размер возникшего зародыша должен быть больше некоторого rk (рис.13), называемого критическим (устойчивым) размером.
Кроме самопроизвольного (гомогенного) образования зародышей кристаллизации может происходить и гетерогенное образование, когда в расплавленном материале присутствуют частички примесей, имеющих одинаковую кристаллическую решетку с исходным материалом. Эти примесные частицы и будут центрами кристаллизации.
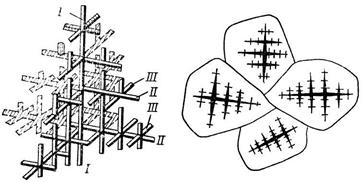
Кристаллы, образующиеся в процессе затвердевания металла, могут иметь различную форму в зависимости от скорости охлаждения, характера и количества примесей. Чаще всего в процессе кристаллизации образуются разветвленные (древовидные) кристаллы, получившие название дендритов (рис.14).
а б
Рис.14. Схема роста кристалла и образования зерна: а – дендрит с осями I, II, III порядка; б – зерна из дендритов
При образовании кристаллов их развитие идет в основном в направлении, перпендикулярном к плоскостям с максимальной плотностью упаковки атомов. Это приводит к тому, что первоначально образуются длинные ветви, так называемые оси первого (I) порядка. Одновременно с удлинением осей первого порядка на их ребрах зарождаются и растут перпендикулярные к ним такие же ветви второго (II) порядка и т.д. Дендритное строение характерно для литого материала.
Структура литого слитка состоит из трех основных зон (рис.15). Первая зона – наружная мелкозернистая корка 1, состоящая из дезориентированных мелких кристаллов – дендритов. При первом соприкосновении со стенками формы в тонком прилегающем слое жидкого металла возникает сильное переохлаждение, сопровождающееся зарождением большого числа центров кристаллизации, что приводит к образованию мелкозернистой структуры. Вторая зона – зона столбчатых кристаллов 2. Степень переохлаждения меняется. В результате из небольшого числа центров кристаллизации начинают расти нормально ориентированные к поверхности корки столбчатые кристаллы. Третья зона – зона равноосных кристаллов 3. Температура застывающего металла почти полностью уравнивается во всем объеме слитка, что и вызывает образование равноосной структуры.
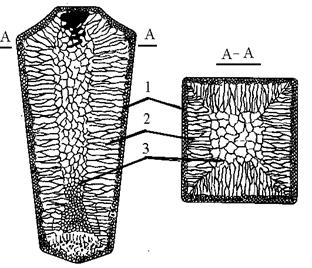
Рис.15. Схема строения стального слитка:
1 – мелкозернистая корка, 2 – столбчатые кристаллы, 3-равноосные кристаллы
Жидкий металл имеет больший объем, чем закристаллизовавшийся, поэтому залитый в форму металл в процессе кристаллизации сокращается в объеме, что приводит к образованию пустот, называемых усадочными
раковинами. Усадочная раковина обычно окружена наиболее загрязненной частью металла, в котором после затвердевания образуются микро- и макропоры и пузыри.
Резюме
Кристаллизацией называется переход металла из жидкого состояния в твердое (кристаллическое). Кристаллизация протекает в условиях, когда система переходит к термодинамически более устойчивому состоянию.
Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах время – температура.
Процесс кристаллизации состоит из двух элементарных процессов: возникновение зародышей, или центров кристаллизации и рост кристаллов из этих центров.
Процесс образования зародышей кристаллизации может происходить самопроизвольно (гомогенное образование), а может идти и по гетерогенному пути образования.
Чаще всего в процессе кристаллизации образуются разветвленные (древовидные) кристаллы, получившие название дендритов.
Кристаллизовавшийся слиток имеет три основных зоны.
Первая зона – наружная мелкозернистая корка, состоящая из дезориентированных мелких кристаллов – дендритов. Вторая зона – зона столбчатых кристаллов. Третья зона – зона равноосных кристаллов.
В процессе кристаллизации происходит образование пустот, называемых усадочными раковинами. Усадочная раковина обычно окружена наиболее загрязненной частью металла, в котором после затвердевания образуются микро- и макропоры и пузыри.
Вопросы для повторения
1. Что такое кристаллизация? В каких условиях происходит этот процесс? Объяснить термодинамику процесса.
2. Какие элементарные процессы составляют процесс кристаллизации?
3. Что представляют собой образовавшиеся кристаллы? Какие основные зоны затвердевшего слитка Вы знаете?
4. Какая часть слитка является наиболее загрязненной?
Дата добавления: 2017-09-01; просмотров: 4991;











