Растворимость газов в воде. Физические методы удаления из воды растворенных газов. Условия равновесия в системе жидкость-газ
Представим себе, что над жидкостью находится газ с каким-то парциальным давлением, а в жидкости этой газ растворен. Если эта система находится в равновесии, то передачи между жидкой и газообразной фазой не происходит. Точнее сказать, количество молекул газа, переходящих из газовой фазы в жидкую, будет больше, чем количество молекул газа, поступающих в газовую фазу, т.е. будет наблюдаться процесс растворения газа в жидкости (абсорбция).
Если парциальное давление газа снизить, то равновесие нарушится в другую сторону. Количество молекул, поступающих в единицу времени из жидкой фазы в газообразную, будет больше, чем из газообразной в жидкую и будет наблюдаться процесс десорбции газа. Процессы растворения и десорбции газа будут идти до тех пор, пока не установится новое равновесное состояние.
Таким образом, каждому значению парциального давления газа над жидкостью при прочих равных условиях должно соответствовать строго определенное количество растворенного газа в этой жидкости. При небольших парциальных давлениях и концентрациях это соответствие определяется законом Генри:
Ср=a(P/Po) (15)
где Cp - равновесная концентрация растворенного газа в жидкости;
Р - парциальное давление газа над жидкостью;
Р0- нормальное атмосферное давление (10333 кг/м2 или 10,3 мм.вод.ст);
a - коэффициент абсорбции (десорбции) газа, зависящий от температуры, природы газа и жидкости.
С повышением температуры коэффициент абсорбции уменьшается и при температуре кипения становится равным нулю.
Как следует из вышеизложенного, при отсутствии равновесия между газовой и жидкой фазой, наблюдается процесс массопередачи, который сопровождается либо растворением, либо десорбцией газа. Движущей силой перехода газа из одной фазы в другую является DР=Рж-РГ, если идет десорбция и DР=РГ-Рж, если идет растворение. Здесь:
Рж - парциальное давление газа над жидкостью, соответствующее по закону Генри его концентрации в жидкости;
РГ - действительное парциальное давление газа над жидкостью.
При равновесном состоянии DР=0.
Растворимость разных газов в воде, следовательно, и предельные их концентрации весьма различны. На эффект дегазации существенно влияет повышение температуры воды, это обусловлено тем, что с повышением температуры уменьшается коэффициент абсорбции газа водой. На рис. 19 показана зависимость коэффициента абсорбции от температуры для кислорода, углекислоты и азота.
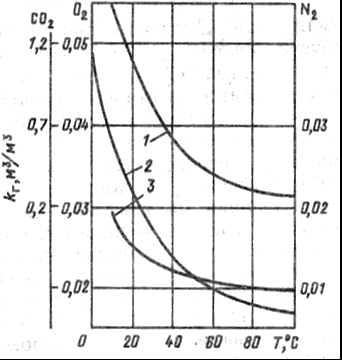
Рисунок 19. Коэффициенты абсорбции СО2 (1), N2 (2) и О2 (3) водой
В практике применяются физические и химические методы удаления из воды растворенных газов.
Физические методы удаления из воды растворенных газов основаны на контакте воды, содержащей растворенный газ с воздухом (аэрация) или другим газом, парциальное давление в котором удаляемого газа очень мало, и на создании таких условий, при которых резко снижается растворимость в воде удаляемого газа.
С помощью аэрации обычно удаляют из воды растворенные углекислоту, метан и сероводород.
Растворенный кислород аэрацией из воды удалить нельзя, так как парциальное давление его в воздухе достаточно высоко - вода при длительном контакте с воздухом содержит при температуре 15° С около 10 мг/л растворенного кислорода. Поэтому растворенный кислород удаляют из воды либо кипячением (при атмосферном давлении или в вакууме), либо химическими методами.
При нагреве воды до температуры кипения растворимость газов в ней снижается до нуля. Поэтому кипячением воды при атмосферном давлении или в вакууме, когда температура кипения в том числе и кислород.
Удаление из воды растворенных газов физическими методами осуществляют:
а) в брызгальных бассейнах, в которых обрабатываемая вода разбрызгивается в воздухе с помощью специальных разбрызгивающих насадок;
б)в пленочных дегазаторах, в которых обрабатываемая вода стекает сверху вниз тонкой пленкой по поверхности насадки из деревянных реек, кокса или колец Рашига, омываемых потоком движущегося снизу вверх воздуха;
в)в барботажных дегазаторах, в которых вода продувается сжатым воздухом, подаваемым в нижнюю часть дегазатора через тонкопористые фильтросные плиты или трубы;
г) в пенных дегазаторах, в которых вода, двигающаяся горизонтально по дырчатым листам, продувается воздухом, подаваемым вентилятором под эти листы;
д) в вакуумных дегазаторах, в которых с помощью вакуум-насосов или эжекторов создается пониженное давление, соответствующее точке кипения воды при данной температуре; вода стекает тонкой пленкой по поверхности насадки дегазатора.
Брызгальные бассейны применяют обычно для удаления из воды углекислоты только на установках большой производительности. Барботажные дегазаторы неэкономичны из-за высокой стоимости компремирования воздуха. Наиболее часто применяют пленочные вентиляторные дегазаторы, которые представляют собой цилиндрические резервуары, заполненные насадкой из колец Рашига или деревянной хордовой насадкой.
Удаление растворенного газа из жидкости при аэрации сопровождается массопередачей его через границу раздела фаз. Наиболее распространенной теорией, объясняющей механизм этой передачи является теория двухслойного поглощения, разработанная Уитманом. Сущность теории двухслойного поглощения заключается в том, что между движущимися жидкостью и газом образуются два пограничных слоя: газовый и жидкостный. Толщина этих пограничных слоев зависит от числа Рейнольдса, а прохождение удаляемого газа через них происходит посредством молекулярной диффузии. Вследствие наличия интенсивных конвенктивных токов как в жидкой, так и в газообразной фазах происходит быстрое выравнивание концентраций в объемах обеих фаз. Следовательно, как основная масса газа, так и основная масса жидкости е представляет собой сопротивления для процесса переноса вещества.
Поэтому согласно теории двухслойного поглощения процесс переноса сводится к последовательной диффузии молекул газа через два неограниченных слоя - жидкостный и газовый.
Изменение концентраций и парциальных давлений на границе раздела фаз можно представить схемой, изображенной на рис. 20.
Рисунок 20. Схема массопереноса газа на границе раздела фаз жидкость-газ
В соответствии со схемой концентрация растворенного газа в жидкости С1 одинакова по всему объему жидкости, исключая жидкостный пограничный слой. В пограничном слое эта концентрация падает от С1 до С2, причем С2 и парциальное давление Р2 на границе раздела двух фаз находятся в зависимости, определяемой законом Генри.
В газовом пограничном слое парциальное давление уменьшается с Р2 до Р1, которое равно парциальному давлению во всем объеме газа.
По теории двухслойного поглощения общее сопротивление массопередачи R есть сумма сопротивлений, оказываемых пограничными диффузионными слоями.
R=R1+R2 (16)
Где R1 - сопротивление жидкостного пограничного слоя;
R2 - сопротивление газового пограничного слоя.
Величины, обратные сопротивлениям в пограничных слоях носят название частных или пленочных коэффициентов десорбции (адсорбции).
Rж=1/R1 - частный коэффициент десорбции жидкостной пленки (Кж);
Rг=1/R2 - частный коэффициент десорбции газовой пленки (Кг);
Численно частный коэффициент десорбции равен количеству газа, передаваемого через единицу площади соприкосновения двух фаз в единицу времени при движущей силе равной единице.
Скорость процесса десорбции и растворенного в воде газа в воздух выражается количеством газа, удаляемого из воды за единицу времени через единицу площади соприкосновения воды и воздуха, т.е.:
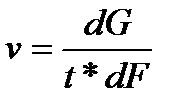 (21)
(21)
где G-количество газа, десорбируемого через площадь dF за время t.
Скорость процесса десорбции газа при малой его концентрации в воде определяется движущей силой ΔС и сопротивлением процессу диффузии в пленке жидкости Кж.
Движущая сила процесса десорбции зависит от разности концентраций удаляемого газа в воде и воздухе:
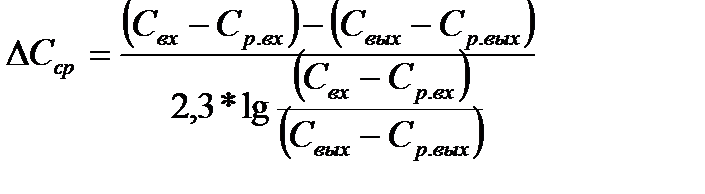 (22)
(22)
где Свх и Свых- концентрации удаляемого газа в воде на входе в дегазатор и на выходе из него;
Ср.вх и Ср.вых- равновесные концентрации удаляемого газа в воде на входе в аппарат и выходе из него.
Отнеся количество десорбированного из воды газа к единице времени, из уравнения (22) получим основное расчетное уравнение аппаратов для удаления из воды растворенных газов десорбцией:
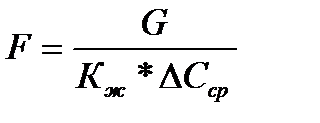 (23)
(23)
где F-площадь поверхности насадки в дегазаторе, в м2;
G - количество удаляемого газа из воды в кг/ч;
ΔСср - средняя движущая сила десорбции в кг/м3;
Кж - коэффициент десорбции в м/ч.
Величина коэффициента десорбции Кж возрастает с увеличением относительной скорости движения воды и воздуха в десорбере, с повышением температуры и увеличением коэффициента диффузии удаляемого газа.
Дата добавления: 2021-07-22; просмотров: 659;











