Объединённый газовый закон. Уравнение Клапейрона. Уравнение Менделеева-Клапейрона.
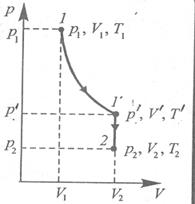 Рассмотрим последовательно изотермический и изохорный процессы (рис.5), переводящие газ из состояния с параметрами (p1,V1, T1) в состояние с параметрами (p2,V2,T2) двумя этапами.
Рассмотрим последовательно изотермический и изохорный процессы (рис.5), переводящие газ из состояния с параметрами (p1,V1, T1) в состояние с параметрами (p2,V2,T2) двумя этапами.
Первый этап – изотермический процесс :
P1V1 = P'V', при чём, 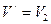 , т.е.
, т.е.
P1V1 = P'V2. (1)
Второй этап – изохорный процесс:
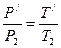 , но
, но 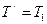 , поэтому
, поэтому 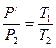 . (10)
. (10)
Выразим из уравнений (1) и (2) давление P/
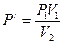 и
и 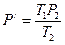 .
.
Рис. 5 Решая систему полученных уравнений, имеем:

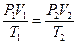 , или
, или 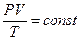 . (11)
. (11)
Полученное уравнение было впервые выведено в 1834г. французским инженером Клапейроном и называется объединённым газовым законом, или уравнением Клапейрона.
Определить эту константу для одного моля идеального газа предложил Менделеев, используя при этом закон Авогадро.
Согласно закону Авогадро: 1 моль любого газа при одинаковых условиях (P и T) занимает одинаковый объём 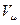 .
.
При нормальных условиях (T0=273K; 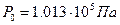 ) молярный объём равен
) молярный объём равен 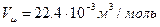 .
.
Подставив приведенные значения P0, 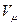 , T0 в основной газовый закон, находим значение постоянной, которая обозначается R =
, T0 в основной газовый закон, находим значение постоянной, которая обозначается R = 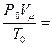 8,31 (Дж/моль К).
8,31 (Дж/моль К).
Для одного моля идеального газа уравнение состояния будет иметь вид:
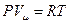 .
.
Для получения уравнения состояния запишем выражения для количества вещества через массу и объём:
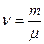 и
и 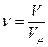 .
.
Откуда
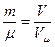 и, далее
и, далее 
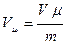 .
.
Подставляя 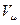 в уравнение Клапейрона, получим уравнение состояния для любой массы идеального газа (уравнениеМенделеева-Клапейрона)
в уравнение Клапейрона, получим уравнение состояния для любой массы идеального газа (уравнениеМенделеева-Клапейрона)

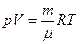 . (12)
. (12)
Дата добавления: 2017-01-16; просмотров: 3973;











