Ионное произведение воды. Водородный показатель.
Электростатическое взаимодействие полярных молекул воды приводит к их самоионизации: 2Н2О↔Н3О++ОН- или в упрощенной форме Н2О↔Н++ОН-;
Константа диссоциации воды весьма мала при 25°С/
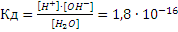
Принимая поэтому концентрацию воды [Н2О] величиной практически постоянной, можно записать К∙ [Н2О]=[Н+] ∙ [ОН-] = 1,8∙10-16[Н2О]. Но концентрация воды равна 1000/18=55,56 моль∙л-1, отсюда получаем [Н+]∙[ОН-] = =1,8∙10-16∙55,56=1∙10-14=Кв.
Произведение концентраций ионов водорода и ионов гидроксида называется ионным произведением воды Кв. Ионное произведение воды
есть величина постоянная при постоянной температуре. В чистой воде и нейтральных растворах[Н+]=[ОН-]=√10-14=10-7 моль∙л-1.
Математически более удобной характеристикой среды является водородный показатель рН, равный десятичному логарифму концентрации водородных ионов, взятому с обратным знаком: рН = -lg[Н+].
Тогда рН различных растворов будут иметь следующие значения:
кислый рН <7;
нейтральный рН = 7;
щелочной рН >7.
Аналогично, отрицательный десятичный логарифм концентрации гидроксо-ионов называется гидроксильным показателем и обозначается рОН. Следовательно,
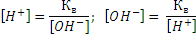
рН + рОН = 14.
Пример 1. Вычисление водородного показателя раствора.
Вычислите водородный показатель рН раствора гидроксида натрия, содержащегося в растворе в концентрации 4,2∙10-3 моль∙л-1 .
Решение. Концентрация ОН- ионов в растворе NaOH равна [0Н-] =4,2∙10-3 моль ∙ л -1. Исходя из ионного произведения воды Кв, находим концентрацию ионов водорода: [Н+] = КВ/[ОН-]=10-14/4,2∙10-3=0,24∙10-11. Водородный показатель раствора NaOH равен: рН= -lg([Н+])=-lg(0,24∙10-11)=11,62.
Пример 2.Определение концентрации ионов Н+ и ОН- в растворах сильных кислот и оснований.
Определите концентрацию ионов водорода и рН в 0,01 М раствора соляной кислоты.
Решение. Соляная кислота - сильный электролит, в растворе полностью диссоциирует на ионы: НС1  Н+ + С1-. Концентрация ионов [Н+] численно равна концентрации НС1. Из 0,01 моль НС1 образуется 0,01 моль иона Н+. Отсюда, [Н+] =0,01∙10-2; рН=-lg(1∙10-2)=2.
Н+ + С1-. Концентрация ионов [Н+] численно равна концентрации НС1. Из 0,01 моль НС1 образуется 0,01 моль иона Н+. Отсюда, [Н+] =0,01∙10-2; рН=-lg(1∙10-2)=2.
Пример 3. Вычисление рН сильного электролита с учетом его коэффициента активности.
Найдите водородный показатель раствора НNO3, если его молярная концентрация равна 0,178 моль∙л-1.
Решение. При значительной концентрации сильного электролита его активная концентрация существенно отличается от истинной. Поэтому в таких случаях нужно вводить поправку на активность электролита. Определяем ионную силу раствора НNO3: J= 1/2∙ (0,176∙I2 + 0,178∙I2) = 0,356/2 = 0,178.
Далее по вычисленной ионной силе находим коэффициент активности иона [Н+]= f(Н+)=0.838. Тогда активность ионов [Н+], а (Н+) =0,83∙0,178=0,148. Водородный показатель раствора НNO3ранен: рН = -lg а(Н+) = -lg 0,148=0,83.
Пример 4. Определение концентрации ионов Н+ и ОН- в растворах слабых кислот и оснований.
Концентрации [Н+] и [ОН-] ионов в растворах слабой кислоты и слабого основания могут быть вычислены, если известны их константы диссоциации. В общем виде формула для вычисления концентрации [Н+] в растворе слабой кислоты: [Н+]=√(Кдкислоты ∙ Скислоты)
Концентрация ионов [Н+]и [ОН-] в растворе слабого основания может быть вычислена по формуле: [ОН-]=√(Кдосн∙ Сосн.); [Н+]= Кв/[ОН-];
[Н+]=Кв/√(Кдосн∙Сосн).
Определите концентрацию[Н+], [ОН-], рН, рОН, в 0,0 М раствора муравьинной кислоты, если Кд(HCOOH)=2,1∙10-4
Решение:
[Н+]=√2,1∙10-4∙3∙10-2 = √6,3∙10-6= 2,5∙10-3 моль∙л-1;
рН= -lg 2,5∙10-3=3-lg 2,5 = 3-0,4= 2,6;
[ОН-]= Кв/[Н+]= 10-14/(2,5∙10-3)=4∙10-12 моль∙л-1;
рОН= 14-рН=14-2,6 = 11,4.
ГИДРОЛИЗ СОЛЕЙ
Под гидролизом понимают реакции обменного взаимодействия вещества с водой. Гидролиз является частным случаем сольволиза - обменного разложения растворенного вещества и растворителя. Процесс гидролиза в большинстве случаев обратим. Он происходит только в тех случаях, когда из ионов соли может образоваться хотя бы одно слабо диссоциирующее или труднорастворимое вещество. Образование такого вещества сопровождается связыванием одного из ионов, на которые диссоциирует вода, при этой происходит смещение равновесия этого процесса в сторону его усиления и изменение рН раствора. Различают три случая гидролиза.
1. Гидролиз по катиону. Характерен для солей, образованных слабым основанием и сильной кислотой (например, NН4Сl, Al(NO2)3, CuSO4 и другие). Рассмотрим гидролиз хлорида аммонияNН4Сl. Анонины Сl, образующиеся при диссоциации NН4Сl= NН4 + + Сl-не связывают ионов водорода, так как НС1 - сильная кислота. Катионы NН4+ связывают ионы ОН- с образованием слабо диссоциирующего основания NН4СН по уравнению NН4+ +НОН  NН4ОН + Н+. При этом освобождаются ионы Н+, обеспечивающие кислую реакцию среды (рН<7).
NН4ОН + Н+. При этом освобождаются ионы Н+, обеспечивающие кислую реакцию среды (рН<7).
Молекулярное уравнение гидролиза записывается в виде
NН4Сl+Н2О  NН4ОН+НСl. Самым слабым электролитом в рассматриваемой системе является вода, поэтому равновесие смещено влево и гидролиз до конца не идет.
NН4ОН+НСl. Самым слабым электролитом в рассматриваемой системе является вода, поэтому равновесие смещено влево и гидролиз до конца не идет.
2. Гидролиз по аниону, Характерен для солей, образованных сильным основанием и слабой кислотой (например, КCN, СН3СООNа, Na2CO3, K2S и др.).
Рассмотрим гидролиз ацетата натрия СН3СООNа. Рассуждая аналогично первому случаю, приходим к выводу, что в данной соли гидролизуется анион СН3СОО- по уравнению:
СН3СОО- + НОН  СН3СООН + ОН-
СН3СООН + ОН-
Реакция среды щелочная (рН> 7).
Молекулярное уравнение реакции записывается следующим образом:
СН3СООNa + Н2О  СН3СООН + NaОН.
СН3СООН + NaОН.
3. Гидролиз по аниону и катиону. Характерен для солей, образованных слабым основаниеми слабой кислотой.
Например, при гидролизе ацетата аммония NH4CH3COO и катион, и анион участвуют в процессе, образуя слабо диссоциирующие основание и кислоту:
NH4+ +CH3COO- + НОН  NH4ОН + CH3COOН.
NH4ОН + CH3COOН.
В этом случае реакция среды определяется относительной силой (константой диссоциации) образующихся основания и кислоты. Если основание и кислота одинаковы по силе, то константы диссоциации их равны и рН=7; если кислота сильнее основания, т.е. константа ассоциации кислоты больше константы диссоциации основания, то реакция среды слабокислая, и наоборот.
В зависимости от основности слабой кислоты, образующей соль, и кислотности слабого основания различают две формы гидролиза: простейший и ступенчатый.
Простейший гидролиз. Характерен для солей, образованных одноосновной слабой кислотой и (или) слабым многокислотным основанием (NH4CN, NH4Cl, NaCl, CH3COONa, KNO2 и другие).
Ступенчатый гидролиз. Характерен для солей, образованных слабой многоосновной кислотой и (или) слабым многокислотным основанием (Na2CO3,K2S, (NH4)2,FeCL3,CuSO4,CuCL2 и другие).
Гидролиз по катиону. Рассмотрим гидролиз FеС13. Катионы Fе3+,
образующиеся при диссоциации молекул соли FеСl3=Fe3+ + 3Cl- связывают ионы ОН- с образованием слабодиссоциирующих частиц, причем присоединение гидроксильных групп происходит постепенно,
по ступеням:
1 ступень: Fе3+ + НОН  FеОН2+ + Н+
FеОН2+ + Н+
2 ступень: FeOH2+ + HOH  Fe(OH)2+ + H+
Fe(OH)2+ + H+
3 ступень: практически не протекает.
Накапливающиеся в системе ионы Н+ обеспечивают кислую реакцию среды и сильно смещают процесс диссоциации воды Н2О ↔ Н+ + ОН-
влево, что приводит к ослаблению гидролиза на ступени 2, а по
ступени 3 гидролиз практически не идет.
Таким образом, гидролиз солей, образованных слабым многокислотным основанием и сильной кислотой, протекает ступенчато с образованием основных солей. Молекулярные уравнения:
1 ступень: FeCl3 + H2O  FeOH2+ + H+
FeOH2+ + H+
2 ступень:FeOHCl2+ H2O  Fe(OH)2Cl + HCl
Fe(OH)2Cl + HCl
3 ступень: практически не идет.
Гидролиз по аниону. Рассмотрим гидролиз соли Na2S. Анионы S2-, образующиеся при диссоциаций соли Na2S  2Na+ + S2-, связывают ионы Н+ с образованием слабо диссоциирующих частиц. Присоединение Н+ происходит постепенно:
2Na+ + S2-, связывают ионы Н+ с образованием слабо диссоциирующих частиц. Присоединение Н+ происходит постепенно:
1 ступень: S2- + НОН  HS- + OH-
HS- + OH-
2 ступень: HS- + HOH  H2S + OH-
H2S + OH-
Накапливающиеся в системе ионы OH- обеспечивают щелочную реакцию среды и ослабляют течение гидролиза по ступени 2.
Таким образом, гидролиз солей, образованных сильным основанием
и слабой многоосновной кислотой, протекает ступенчато с образованием кислых солей. Молекулярное уравнение:
1 ступень: Na2S + H2O  NaHS + NaOH
NaHS + NaOH
2 ступень: практически не идет.
Полный необратимый гидролиз. Некоторые соли, образованные очень слабым основанием и слабой летучей кислотой (Cr2S3, Cr2(CO3)3, Fe2(CO3)3, Al2(CO3)3 и другие), подвергаются полному необратимому гидролизу. При этом образуется слабо диссоциирующие основание и кислота. Оба продукта уходят из сферы реакции в виде осадков и газов. Аналогично гидролизируются смеси солей, одна из которых образована очень слабым основанием и сильной кислотой, а другая - сильным основанием и слабой летучей кислотой (Na2S + CrCl3 Na2CO3 + Al2(SO4)3 и т.п.). Например:
2AlCl3 + 2Na2S + 6H2O = 2Al(CO)3↓+ 3H2S↑ + 6NaCl
Количественными характеристиками процесса гидролиза служат степень и константа гидролиза.
Таблица 5
Примеры сильных и слабых кислот и оснований
| Кислоты | Основания | |||
| Сильные | Средней силы | Слабые | Сильные | Слабые |
| HCL | H3PO4 | HCN | Гидроксиды щелочных металлов (KOH, NaOH, ZiOH), Ba(OH)2 идр. | Na4OHи нерастворимые в воле основания (Ca(OH)2, Zi(OH)2, AL(OH)3 и др. |
| HBr | H2SO3 | HNO2 | ||
| HI | HP | H2CO3 | ||
| HNO3 | H2S | |||
| H2SO4 | CH3COOH | |||
| HMnO4 | HCIO | |||
| HCLO4 |
Константа гидролиза равна отношению произведения концентраций
продуктов гидролиза к концентрации негидролизованной соли.
Пример 1. Вычислить степень гидролиза NH4Cl.
Решение: Из таблицы находим Кд(NH4ОН)=1,8∙10-3, отсюда Кγ=Кв/Кдк= =10-14/1,8∙10-3= 5,56∙10-10.
Пример 2. Вычислить степень гидролиза ZnCl2 по 1 ступени в 0,5 М растворе.
Решение: Ионное уравнение гидролиза Zn2 + H2O  ZnOH+ + H+
ZnOH+ + H+
KдZnOH+1=1,5∙10-9; hγ=√(Кв/ [Кдосн∙Cм]) = 10-14/1,5∙10-9∙0,5=0,36∙10-2 (0,36%).
Пример 3.Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: a) KCN; б) Na2CO3; в) ZnSO4. Определите реакцию среды растворов этих солей.
Решение, а) Цианид калия KCN — соль слабой одноосновной кислоты (см. табл. I приложения) HCN и сильного основания КОН. При растворении в воде молекулы KCN полностью диссоциируют на катионы К+ и анионы CN-. Катионы К+ не могут связывать ионы ОН- воды, так как КОН — сильный электролит. Анионы же CN- связывают ионы Н+ воды, образуя молекулы слабого элекролита HCN. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
CN- + Н2О  HCN + ОН-
HCN + ОН-
или в молекулярной форме
KCN + Н2О  HCN + КОН
HCN + КОН
В результате гидролиза в растворе появляется некоторый избыток ионов ОН-, поэтому раствор KCN имеет щелочную реакцию (рН > 7).
б) Карбонат натрия Na2CO3 — соль слабой многоосновной кислоты и сильного основания. В этом случае анионы соли СО32-, связывая водородные ионы воды, образуют анионы кислой соли НСО-3 , а не молекулы Н2СО3, так как ионы НСО-3 диссоциируют гораздо труднее, чем молекулы Н2СО3. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
CO2-3+H2O  HCO-3 +ОН-
HCO-3 +ОН-
или в молекулярной форме Na2CO3 + Н2О  NaHCO3 + NaOH
NaHCO3 + NaOH
В растворе появляется избыток ионов ОН-, поэтому раствор Na2CO3 имеет щелочную реакцию (рН > 7).
в) Сульфат цинка ZnSO4 — соль слабого многокислотного основания Zn(OH)2 и сильной кислоты H2SO4. В этом случае катионы Zn+ связывают гидроксильные ионы воды, образуя катионы основной соли ZnOH+ .Образование молекул Zn(OH)2 не происходит, так как ионы ZnOН+ диссоциируют гораздо труднее, чем молекулы Zn(OH)2. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза
Zn2+ + Н2О  ZnOН+ + Н+
ZnOН+ + Н+
или в молекулярной форме
2ZnSO4 + 2Н2О  (ZnOH)2SO4 + H2SO4
(ZnOH)2SO4 + H2SO4
В растворе появляется избыток ионов водорода, поэтому раствор ZnSO4 имеет кислую реакцию (рН < 7).
Пример 4.Какие продукты образуются при смешивании растворов A1(NO3)3 и К2СО3? Составьте ионно-молекулярное и молекулярное уравнение реакции.
Решение. Соль A1(NO3)3 гидролизуется по катиону, а К2СО3 — по аниону:
А13+ + Н2О  А1ОН2+ + Н+
А1ОН2+ + Н+
СО2-3 + Н2О  НСО- з + ОН-
НСО- з + ОН-
Если растворы этих солей находятся в одном сосуде, то идет взаимное усиление гидролиза каждой из них, ибо ионы Н+ и ОН-образуют молекулу слабого электролита Н2О. При этом гидролитическое равновесие сдвигается вправо и гидролиз каждой из взятых солей идет до конца с образованием А1(ОН)3 и СО2 (Н2СО3). Ионно-молекулярное уравнение:
2А13+ + ЗСО2-3 + ЗН2О = 2А1(ОН)3 + ЗСО2
молекулярное уравнение: ЗСО2 + 6KNO3
2A1(NO3)3 + ЗК2СО3 + ЗН2О = 2А1(ОН)3
Дата добавления: 2019-09-30; просмотров: 645;











