Математическая формулировка второго начала
Из 4-й формулировки можно (с помощью логики и математики) показать, что у превращения тепла đQ* (элементарное количество тепла, получаемого системой) существует интегрирующий множитель, превращающий его в полный дифференциал:
μ(T, xi) đQ* = dS(T, xi) (II)
где dS – полный дифференциал, а S – функция состояния!!! (зависит от внешних параметров и температуры). Эта функция S(T, xi) не зависит от энергии.
Докажем (для случая трех независимых переменных: T и двух внешних параметров x1 и x2).
Дифференциал внутренней энергией:
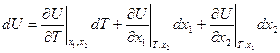 (1)
(1)
Работа:
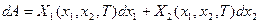 (2)
(2)
Тогда (I) запишем в виде:
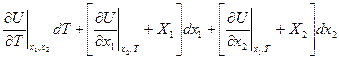 (3)
(3)
Переобозначим для удобства:
T = x; x1 = y; x2 = z, тогда вместо (3) имеем:
đQ* = P(x, y, z)dx + Q(x, y, z)dy + R(x, y, z)dz (4)
это дифференциальная форма Пфаффа от 3-х переменных. Из математики: если
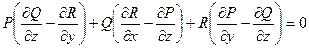 (5),
(5),
то форма (4) интегрируема, т.е. существует интегрирующий множитель μ(x, y, z) такой что
μ(x, y, z)đQ* = dS(x, y, z) (II)
где dS – полный дифференциал, а S – функция состояния, при адиабатическом процессе (т.к. đQ* = 0) S(x, y, z) = const, т.е. все возможные состояния лежат на поверхности (6)
Пример: идеальный газ pV = const => адиабата. Разные адиабата – разные S. Можно показать: const = pVγ = exp{S/CV} (7)
Сравни изотерма pv = RT
Если (5) не выполняется: đQ* = 0 сводится к обыкновенному дифференциальному уравнению с двумя исходными функциями, и допускает большой произвол в поиске решений. Задавая одну из низ в разных видах, можно найти другую, и подобрать кривую, проходящую через любые две точки [x1, y1, z1 (1), x2, y2, z2 (2)] и удовлетворяющую (4) при đQ* = 0, т.е. любые два состояния могут быть связаны адиабатическим процессом. Но это противоречит формулировке 2-го начала. Т.о. доказали (II)
Можно доказать (докажем в статистике), что среди интегрирующих множителей есть такой, который зависит только от температуры. При этом можно выбрать температуру так, что μ = 1/T, где T – абсолютная термодинамическая температура. Тогда II перепишем:
đQ* = TdS(xi, T) (II`)
Это и есть математическая формулировка 2-го начала.
Отсюда
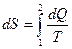 (8)
(8)
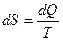 - приведенное количество тепла.
- приведенное количество тепла.
Итак, 3 начала теродинамики:
0-е – принцип температуры (существует температура)
1-е – принцип энергии (1-е начало - ЗСЭ)
2-е – принцип энтропии
Дата добавления: 2021-05-28; просмотров: 109;










