Очистка на синтетических цеолитах.
Высокая поглотительная способность цеолитов при низких концентрациях адсорбируемого вещества и избирательность по отношению к определенным компонентам дают возможность эффективно использовать их для промышленного разделения, очистки и осушки газовых смесей. В большинстве случаев используется высокая адсорбционная избирательность молекулярных сит по отношению к полярным и ненасыщенным соединениям (воде, С02, H2S, сернистому ангидриду и меркаптанам).
Цеолиты являются эффективным средством сероочистки газов, не содержащих кислород. Кроме высокой адсорбционной способности по H2S, цеолиты обладают высокой избирательностью по отношению к H2S в присутствии С02. При мольном соотношении в газе H2S:C02 = 1:1 адсорбированная фаза обогащается H2S до 90 %.
В процессе одновременной очистки от H2S и С02 происходит практически полное удаление обоих компонентов из газа, затем С02 начинает вытесняться из адсорбента H2S и содержание С02 в выходящем потоке газа резко возрастает, причем за счет вытеснения лучше адсорбируемым H2S концентрация С02 даже превосходит его концентрацию в исходном газе. В то же время H2S продолжает количественно поглощаться вплоть до момента проскока. Так как С02 является лишь балластным, а не коррозионным компонентом при транспорте газа, часто эксплуатационные затраты на его удаление превосходят затраты на транспорт. В этом случае целесообразно его не удалять или удалять лишь частично. Изменяя продолжительность адсорбционного процесса, можно получить любую заданную степень извлечения С02.
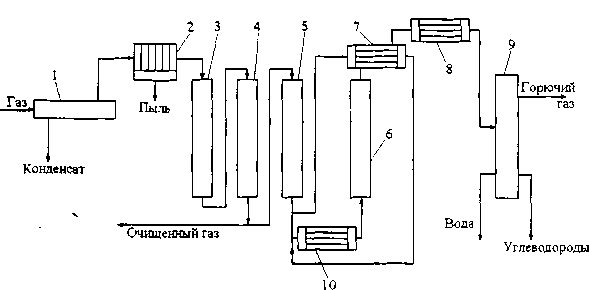 Рис. 7.1. Схема установки для сероочистки природных газов цеолитами 1,9 - сепараторы; 2 - фильтр; 3-6 - адсорберы на стадиях очистки, доулавлива- ния, охлаждения и регенерации соответственно; 7 - теплообменник; 8 - холодильник; 10 - нагреватель
Рис. 7.1. Схема установки для сероочистки природных газов цеолитами 1,9 - сепараторы; 2 - фильтр; 3-6 - адсорберы на стадиях очистки, доулавлива- ния, охлаждения и регенерации соответственно; 7 - теплообменник; 8 - холодильник; 10 - нагреватель
|
Установка очистки природного газа от H2S в стационарном слое синтетических цеолитов (рис. 7.1) состоит из четырех адсорберов. В схеме с открытым циклом сырой природный газ после отделения конденсата в первичном сепараторе 1 и пыли в фильтре 2 последовательно проходит через адсорберы 3 и 4, где очищается от H2S, и поступает в газопровод. Адсорбер 4 выполняет функции доулавливателя, а затем переключается на функции адсорбера 3, после того как тот переведен на стадию регенерации. Часть очищенного газа отбирают и используют сначала для охлаждения адсорбера 5, а затем после нагрева - для десорбции газов из адсорбента в десорбере 6.
В сепараторе 9 из газа регенерации удаляют воду и жидкие УВ, обычно содержащиеся в природном газе. После этого газ регенерации используют в качестве топлива на местные нужды, например, на установках синтеза аммиака. Таким образом в каждом адсорбере последовательно проводятся регенерация, охлаждение, доулавливание, сероочистка.
Из цеолитов общего назначения наилучшими адсорбционными и эксплуатационными свойствами обладают цеолиты типа СаА. Цеолиты типа NaA отличаются низкой скоростью поглощения и десорбции сернистых соединений. Цеолит NaX катализирует реакцию окисления H2S с образованием элементной серы, дезактивирующей адсорбент. Однако это не исключает возможность его применения для сероочистки газов. В случае присутствия в газе кроме H2S сероорганических соединений, например, меркаптанов, целесообразно применять именно цеолит NaX. В этом случае адсорберы с цеолитом устанавливают после установки очистки аминами, в которых удаляется H2S.
7.4. Каталитическая переработка сероводорода в серу
Для переработки H2S, получающегося в результате его десорбции после очистки природного, нефтяного или иного промышленного газа,
используют метод Клауса, заключающийся в окислении H2S кислородом воздуха в элементную серу:
2 H2S + 02 → 2S + 2Н20 + 220 кДж.
В модифицированном варианте схемы (рис.7.2) окисление проводят в две стадии: термической и каталитической. В термической стадии ведут пламенное окисление H2S со стехиометрическим количеством 02 при температурах в топке 900-1350 °С. Однако при этом часть H2S окисляется до S02. В каталитической части идет реакция между H2S и S02 на катализаторе - боксите или активной окиси алюминия при температуре 220-250 °С:
2H2S + S02 → 2Н20 + 3S.
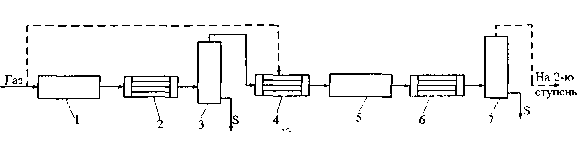 Рис. 7.2. Схема установки для очистки газов от сероводорода методом Клауса
1 - аппарат пламенного окисления; 2,6 - холодильники; 3,7 - сепараторы; 4 - нагреватель; 5 - реактор с бокситом
Рис. 7.2. Схема установки для очистки газов от сероводорода методом Клауса
1 - аппарат пламенного окисления; 2,6 - холодильники; 3,7 - сепараторы; 4 - нагреватель; 5 - реактор с бокситом
|
Как правило, каталитический процесс проводят в две стадии, т.к. в результате реакции сильно повышается температура газов. Для увеличения выхода серы после термической и каждой каталитической ступени реакционные газы охла-
ждают до 140-160 °С и из них выводят образовавшуюся элементную серу. Подогрев газа перед каталитическими ступенями до 250 °С идет за счет тепла сгорания части H2S (15 %) в специальной топке. Продукты сгорания примешиваются к реакционному газу.
В случае содержания H2S в газах менее 30 % переработка его в серу производится без термической ступени, для чего одна треть газов окисляется до S02 полностью, а затем после смешения с остальными двумя частями газа перерабатывается на двух каталитических ступенях. Тепло реакции окисления H2S используют для получения водяного пара, который, как правило, передается на установки извлечения H2S из горючих газов.
Дата добавления: 2016-12-27; просмотров: 3971;











